Clear Sky Science · fr
DKK1 et NEDD4 dérivés des cellules de la crête neurale modulent la signalisation Wnt dans le second champ cardiaque pour orchestrer le développement du tractus de sortie
Pourquoi ces petits bâtisseurs du cœur comptent
Le cœur de l’embryon précoce commence comme un simple tube, mais il doit rapidement se remodeler en un organe complexe qui envoie le sang vers le corps et les poumons. Des étapes subtiles mal gérées pendant cette construction peuvent causer de graves malformations congénitales, y compris des affections nécessitant une chirurgie peu après la naissance. Cette étude révèle comment deux populations cellulaires communiquent entre elles pour façonner la principale voie de sortie du cœur, et met en lumière une erreur moléculaire susceptible de contribuer aux cardiopathies congénitales chez la souris et l’homme.
Deux équipes qui construisent la rampe de sortie du cœur
La portion du cœur qui éjecte le sang des ventricules — le tractus de sortie — se forme à partir d’une zone appelée second champ cardiaque. Les cellules de cette région doivent rester des « progéniteurs » assez longtemps pour être ajoutées au tractus de sortie en croissance, puis se différencier en muscle au bon moment. Juste à côté d’elles circulent les cellules de la crête neurale, une population migratrice qui participe à la formation des grandes artères et des valves. Des travaux antérieurs suggéraient que ces cellules de la crête neurale influençaient d’une certaine façon le second champ cardiaque, mais la nature de ce dialogue restait inconnue. 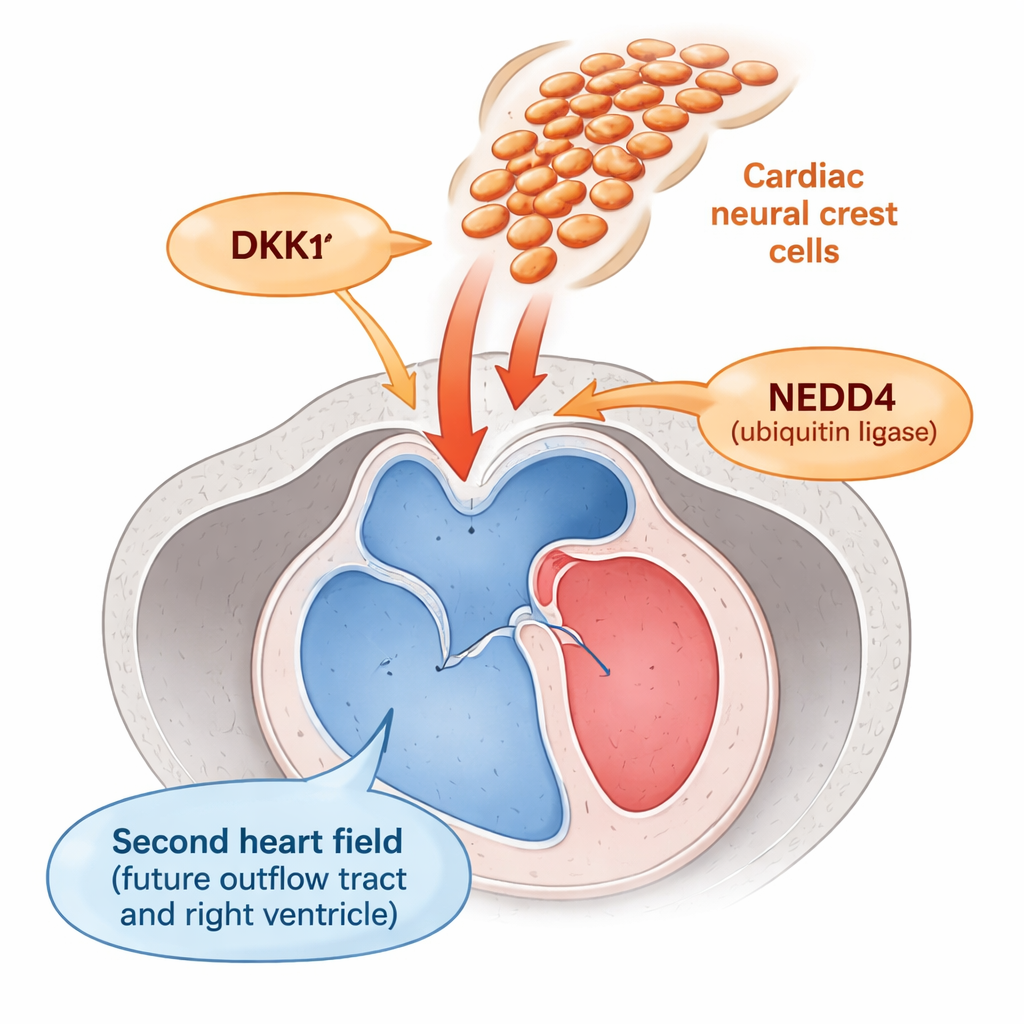
Un variateur moléculaire pour les signaux de croissance
Les auteurs ont découvert que les cellules de la crête neurale agissent comme un variateur pour un signal de croissance clé appelé Wnt, qui maintient les progéniteurs en division et retarde leur maturation. Ils ont constaté que les cellules de la crête neurale sont une source majeure de DKK1, une petite protéine sécrétée qui bloque la signalisation Wnt dans les cellules voisines. DKK1 est lui‑même régulé par NEDD4, une protéine qui marque DKK1 pour sa dégradation. Chez des embryons de souris dépourvus de Nedd4 spécifiquement dans les cellules de la crête neurale, DKK1 s’accumulait à des niveaux anormalement élevés. Cet excès de DKK1 a réduit l’activité Wnt dans le second champ cardiaque adjacent, comme l’attestait une diminution de la β‑caténine nucléaire — un indicateur standard de la signalisation Wnt — et des niveaux plus faibles de plusieurs gènes répondant à Wnt.
Quand le timing déraille, la géométrie du cœur échoue
Trop de DKK1 et trop peu de Wnt ont eu une conséquence nette : les cellules du second champ cardiaque ont commencé à se transformer en muscle cardiaque trop tôt. Des marqueurs du muscle mature sont apparus précocement dans cette zone de progéniteurs, et il restait moins de cellules indifférenciées pour prolonger le tractus de sortie. En suivant les cellules en division au fil du temps, l’équipe a montré que moins de cellules du second champ cardiaque étaient ajoutées au tractus de sortie chez les mutants. En conséquence, le tractus de sortie était plus court et mal orienté, entraînant un désalignement entre les grandes artères et les ventricules. Ces erreurs structurelles ressemblaient à des défauts conotruncaux humains tels que le ventricule droit à double sortie et à des malformations observées chez des souris à knockout complet de Nedd4.
Prouver le rôle du signal et un lien avec la maladie humaine
Pour confirmer que l’altération de la signalisation Wnt était bien la cause de ces problèmes, les chercheurs ont modulé la voie avec des médicaments chez des femelles gestantes. Bloquer Wnt chez des embryons par ailleurs sains les a poussés vers la même différenciation prématurée et les mêmes défauts de rotation observés lors de la perte de Nedd4, tandis que la réduction de la dose génique de Dkk1 dans le contexte déficient en Nedd4 a partiellement restauré la taille et la rotation du tractus de sortie. Enfin, l’équipe a identifié un enfant atteinte d’une tétralogie de Fallot portant une variante rare héréditaire de NEDD4 qui affaiblissait sa capacité à marquer DKK1 pour sa dégradation. Des souris génétiquement modifiées pour porter la même variante de Nedd4 ont développé des défauts pariétaux et septaux du cœur du côté droit, soutenant l’idée qu’un contrôle défaillant de NEDD4–DKK1 peut contribuer aux cardiopathies congénitales humaines.
Ce que cela signifie pour la compréhension des malformations cardiaques
Pour un public non spécialiste, le message clé est que la « rampe de sortie » du cœur dépend d’un timing précis : quand ses éléments cessent de se multiplier et commencent à devenir du muscle. Ce timing est contrôlé non seulement depuis le tissu cardiaque lui‑même, mais aussi par les cellules voisines de la crête neurale qui ajustent finement un signal de croissance via le couple NEDD4–DKK1. Lorsque ce variateur moléculaire reste trop bas, le tractus de sortie est sous‑construit et mal aligné, conduisant à de graves malformations congénitales. En cartographiant cette voie et en la liant à une variante génétique humaine, l’étude fournit de nouveaux indices sur l’origine de certaines cardiopathies congénitales et met en lumière des cibles moléculaires potentielles pour le diagnostic ou l’intervention future.
Citation: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Mots-clés: cardiopathie congénitale, développement cardiaque, cellules de la crête neurale, signalisation Wnt, tractus de sortie cardiaque