Clear Sky Science · fr
Une délétion d’ADN fréquente modifiant la région 3’UTR de mdr1 est associée à une réduction de la sensibilité au méfloquine chez des parasites P. vivax prélevés chez des patients cambodgiens
Pourquoi cette étude sur le paludisme importe
Pour les personnes vivant dans ou voyageant vers des régions endémiques du paludisme, des médicaments efficaces sont une bouée de sauvetage. Mais les parasites du paludisme évoluent sans cesse pour survivre aux traitements. Cette étude se concentre sur Plasmodium vivax, la principale cause de paludisme en dehors de l’Afrique, et met au jour un changement génétique subtil qui pourrait déjà aider le parasite à tolérer un médicament important, la méfloquine. Comprendre cette évolution dès maintenant pourrait aider les responsables de santé publique à prendre de l’avance sur l’émergence d’une résistance aux médicaments.
Un parasite tenace et des options thérapeutiques qui se réduisent
Le paludisme chez l’humain est causé par plusieurs parasites apparentés, mais P. vivax est particulièrement difficile à éliminer. Il peut se cacher dans le foie pendant des mois avant de réapparaître dans le sang, et circule souvent à des niveaux trop faibles pour être détectés par les tests standard. Pendant des décennies, la chloroquine de première ligne était efficace contre P. vivax, mais des signes de résistance se sont multipliés. En conséquence, l’Organisation mondiale de la Santé recommande désormais l’utilisation de thérapies combinées à base d’artémisinine (ACT), qui associent un médicament à action rapide à un partenaire plus persistant comme la méfloquine. Comme la culture en laboratoire de P. vivax est difficile, les scientifiques s’appuient largement sur des échantillons de patients et des indices génétiques pour suivre la réponse du parasite à ces médicaments.
Un tout petit morceau d’ADN manquant dans un gène clé de résistance
Les chercheurs ont séquencé les génomes de 206 échantillons de P. vivax prélevés chez des patients paludéens au Cambodge entre 2021 et 2023. Ils ont recherché des segments d’ADN soit délétés soit dupliqués. Parmi de nombreuses réarrangements, un élément a retenu l’attention : plus de 80 % des parasites portaient une petite délétion d’ADN située juste après la fin de la région codante d’un gène nommé mdr1 (multidrug resistance 1). Ce gène code pour une protéine transporteur capable d’expulser divers composés, y compris des médicaments, à travers une membrane à l’intérieur du parasite. Contrairement à des mutations précédemment rapportées, cette délétion de 837 paires de bases ne modifiait pas la séquence protéique elle‑même. Elle se trouvait plutôt dans la région dite 3’ non traduite (3’UTR), un segment du gène qui n’est pas traduit en protéine mais peut fortement influencer la quantité de protéine finalement produite.
Suppressions indépendantes et messages altérés d’un même gène
Pour vérifier si des changements similaires apparaissaient ailleurs, l’équipe a réanalysé près de 830 génomes de P. vivax provenant de 25 pays. Ils ont découvert une autre délétion plus courte chevauchant la même région en aval de mdr1 chez des parasites d’Amérique du Sud. Des comparaisons détaillées et des tests PCR confirmatoires ont montré que les délétions d’Asie du Sud-Est et d’Amérique du Sud étaient distinctes, ce qui suggère qu’elles sont apparues indépendamment — un indice que la sélection naturelle pourrait favoriser des altérations dans cette région régulatrice. Grâce au séquençage ARN de 95 infections cambodgiennes, les chercheurs ont montré que les parasites porteurs de la délétion produisaient une version alternative de l’ARN messager de mdr1, avec un 3’UTR différent. Après ajustement sur la longueur des transcrits, les parasites portant la délétion présentaient près de deux fois plus d’ARNm de mdr1 que ceux ne la portant pas, ce qui laisse penser que la perte d’ADN ou la nouvelle séquence 3’UTR aide à stabiliser ou augmenter l’expression du gène.
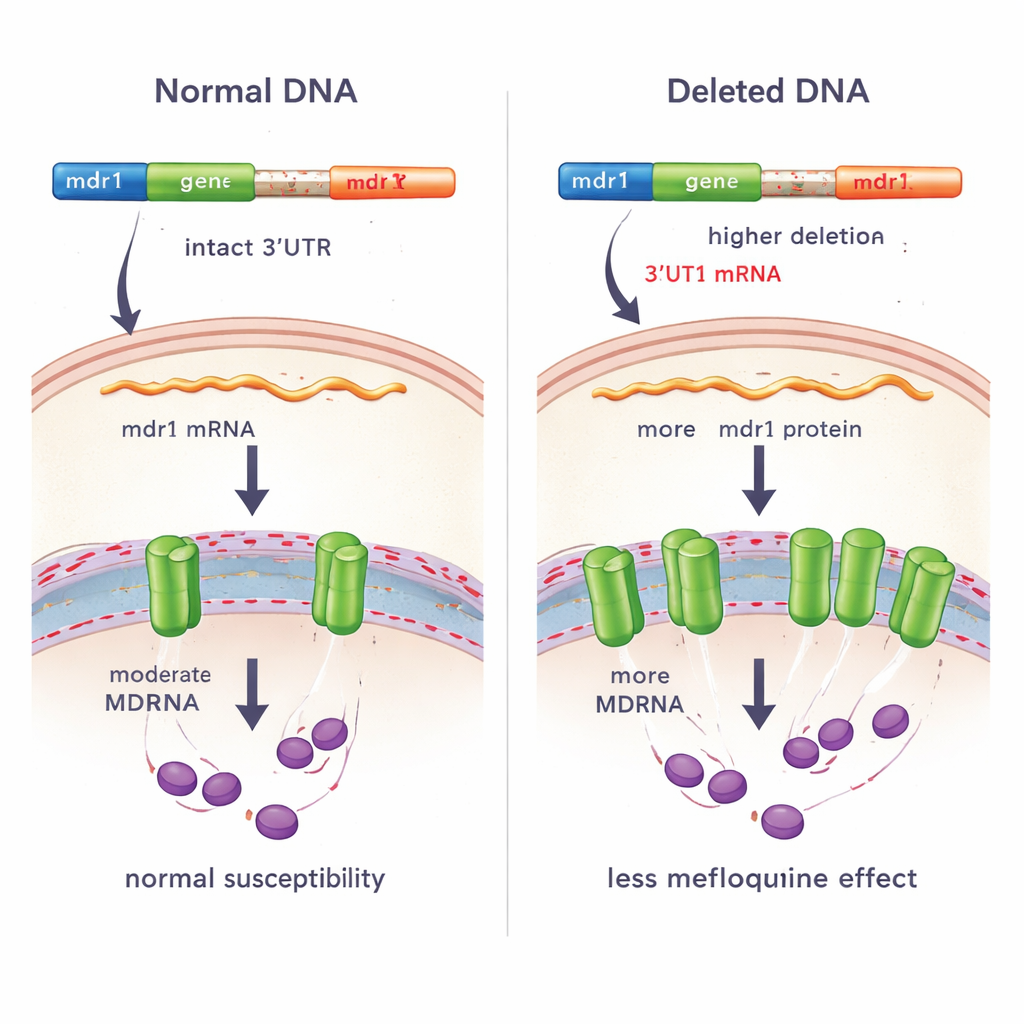
Relier la délétion à la réponse aux médicaments chez les patients et en laboratoire
Étant donné que mdr1 a été impliqué dans la résistance à plusieurs antipaludiques, l’équipe a étudié si la délétion était liée à la réponse des parasites au traitement. Ils ont d’abord comparé la rapidité d’élimination des parasites du sang des patients après un traitement à l’artésunate. Parmi 167 infections, il n’y avait pas de différence significative des taux d’élimination entre les parasites avec et sans la délétion, ce qui suggère que ce changement génétique n’affecte pas directement la sensibilité à l’artésunate en tant que tel. Cependant, dans un sous‑groupe plus restreint de 14 infections où les chercheurs ont mesuré la croissance parasite en présence de méfloquine en dehors du corps, les parasites porteurs de la délétion avaient tendance à présenter des valeurs IC50 plus élevées — ce qui signifie qu’ils nécessitaient davantage de médicament pour inhiber la croissance — que les parasites sans la délétion. Ce schéma est cohérent avec une sensibilité réduite à la méfloquine, bien que la taille de l’échantillon soit limitée.
Une augmentation préoccupante au fil du temps et ce qu’elle pourrait signifier
Pour estimer l’étendue de la diffusion de la délétion, les auteurs ont dépisté 592 échantillons archivés de P. vivax collectés à travers le Cambodge entre 2014 et 2024. Avant l’introduction de la méfloquine dans le cadre des ACT pour le paludisme à vivax vers 2016–2017, environ 30 % des parasites portaient la délétion. Après ce changement, la fréquence est montée au‑dessus de 60 % puis s’est stabilisée, une tendance statistiquement significative qui demeurait même en ne considérant que l’est du Cambodge. La délétion était déjà présente à faible fréquence avant que la méfloquine ne soit largement utilisée contre P. vivax, possiblement en raison d’une exposition indirecte lorsque le médicament était employé contre P. falciparum ou parce que l’altération affecte aussi la réponse à d’autres médicaments. Couplés à des rapports récents d’une élimination un peu plus lente des parasites après traitement à l’artémisinine, ces résultats laissent craindre que P. vivax au Cambodge ne tende vers une diminution de l’efficacité de la combinaison actuelle artésunate–méfloquine.
Ce que cela signifie pour la lutte contre le paludisme
Pour un public non spécialiste, le message essentiel est que même lorsque le gène principal de résistance d’un parasite semble intact, de petits changements dans la « câblerie de contrôle » proche de son ADN peuvent modifier la force d’activation du gène. Dans ce cas, une délétion fréquente dans une région non codante de mdr1 semble augmenter l’activité du gène et est associée à des effets légèrement réduits de la méfloquine sur P. vivax. Bien qu’il n’y ait pas encore de preuve claire d’échec thérapeutique au Cambodge, la fréquence croissante de cette délétion suggère que la pression médicamenteuse pourrait favoriser discrètement les parasites porteurs de ce trait. Reconnaître et surveiller tôt de tels signes génétiques subtils peut aider les autorités sanitaires à ajuster les politiques médicamenteuses, concevoir de meilleurs outils de surveillance et protéger l’arsenal désormais restreint de traitements antipaludiques efficaces.
Citation: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
Mots-clés: Plasmodium vivax, résistance aux médicaments antipaludiques, méfloquine, gène mdr1, Cambodge