Clear Sky Science · fr
Une électrode auto-aérée rendue possible par la régulation d’interface et l’ingénierie d’une gradient de mouillabilité pour l’électrosynthèse industrielle de H2O2
Pourquoi une meilleure façon de produire du peroxyde compte
Le peroxyde d’hydrogène est un désinfectant bien connu des trousses de soins, mais c’est aussi une matière chimique polyvalente pour le traitement de l’eau, la dépollution et la fabrication de nombreux produits du quotidien. Aujourd’hui, presque tout le peroxyde d’hydrogène industriel est produit dans d’immenses usines par un procédé complexe et énergivore qui génère des sous-produits dangereux et concentre la production sur quelques sites centralisés. Cette étude explore une approche très différente : des dispositifs électrochimiques compacts capables de fabriquer le peroxyde d’hydrogène directement à partir de l’air, de l’eau et de l’électricité, ouvrant la voie à une production plus propre, moins chère et plus locale.
Le problème des électrodes inondées
Au cœur de ces dispositifs se trouve une électrode à diffusion de gaz, une feuille mince et poreuse qui doit mettre en contact l’air, l’eau liquide et un solide conducteur électrique pour que la réaction souhaitée ait lieu. Dans les conceptions classiques, un liant de type plastique appelé PTFE est fondu autour des particules de carbone pour empêcher l’eau d’envahir les pores. Mais cette structure « fusionnée » tend à créer des zones scellées et des canaux aléatoires. À forte puissance, l’eau inonde la majeure partie du carbone, l’oxygène ne peut plus atteindre les sites actifs, et l’électrode perd rapidement sa capacité à produire efficacement du peroxyde d’hydrogène.
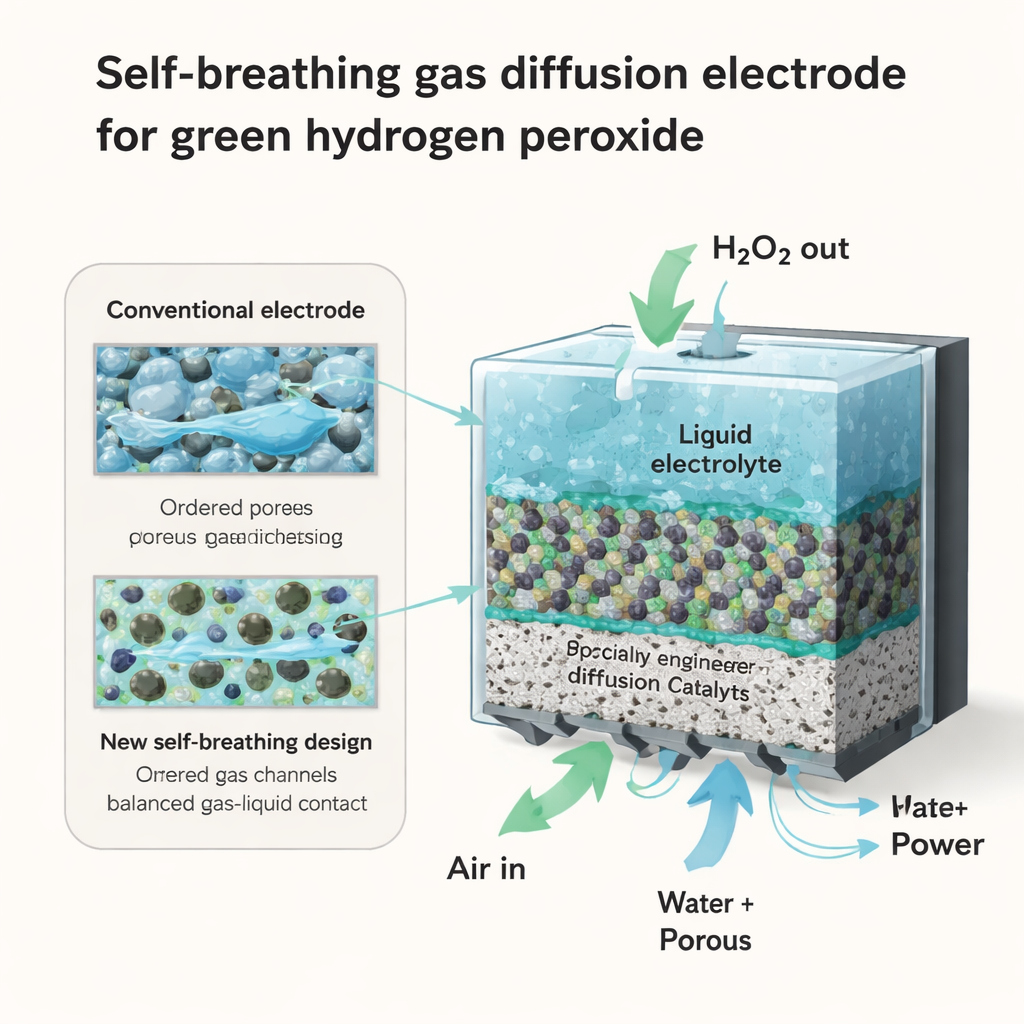
Une nouvelle façon d’assembler les éléments
Les auteurs proposent une architecture différente qu’ils appellent électrode à empilement de particules. Plutôt que de fondre le PTFE en un film continu, ils le conservent sous forme de minuscules particules séparées, intimement mélangées au carbone. Grâce à des imageries 3D avancées et des simulations informatiques, ils montrent que cette structure non fusionnée crée un labyrinthe de pores interconnectés où le PTFE hydrophobe et le carbone hydrophile coexistent côte à côte. Cela génère de nombreux points « trois phases » stables où l’air, le liquide et le solide se touchent simultanément—exactement les micro-environnements où l’oxygène peut être transformé proprement en peroxyde d’hydrogène. Comme les pores restent ouverts et bien connectés, l’oxygène peut se déplacer plus librement et l’inondation est beaucoup moins sévère, même à des courants exigeants.
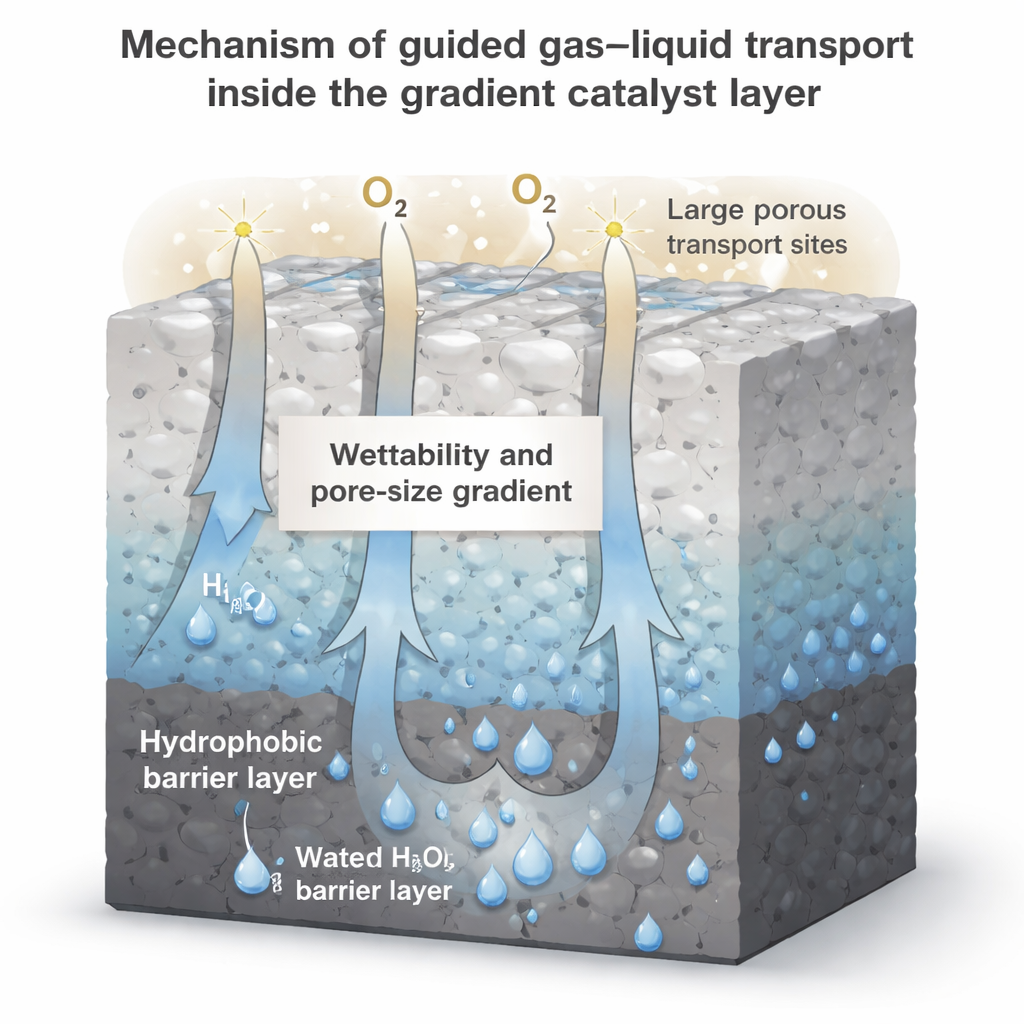
Guider l’eau et le peroxyde par des gradients
S’appuyant sur cette idée, l’équipe va au-delà d’un simple mélange de particules et façonne délibérément à la fois la taille des pores et la mouillabilité de surface à travers l’épaisseur de l’électrode. Ils construisent des revêtements catalytiques en couches où le côté exposé à l’air est très déperlante et finement poreux, tandis que le côté en contact avec le liquide est plus mouillant et contient des canaux plus larges. Des simulations et des expériences microfluidiques montrent que ce gradient agit comme une pompe intégrée : les forces capillaires poussent l’électrolyte et le peroxyde d’hydrogène nouvellement formé vers la région plus ouverte et hydrophile, tout en laissant des voies sèches pour l’oxygène ailleurs. Cette combinaison d’un « bouclier » hydrophobe et d’un « drain » directionnel aide l’électrode à résister à l’inondation et à évacuer en continu le produit des sites de réaction.
Du concept de laboratoire au matériel opérationnel
Les électrodes construites selon ce design en gradient conservent une haute sélectivité pour le peroxyde d’hydrogène—plus de 80 à 85 pour cent du courant électrique est dirigé vers le produit souhaité—à des densités de courant pertinentes pour l’industrie de 300 à 400 milliampères par centimètre carré, et ce pendant des centaines d’heures sans apport externe d’oxygène. Les auteurs intègrent ensuite plusieurs de ces électrodes dans une pile de quatre cellules à peu près de la taille d’un petit placard. Avec des pompes intégrées, la gestion thermique et l’électronique de puissance, le système produit en continu des solutions concentrées de peroxyde d’hydrogène en aspirant l’oxygène directement de l’air. Une analyse des coûts suggère que le peroxyde peut être produit pour bien moins d’un dollar par kilogramme, compétitif avec les méthodes à grande échelle actuelles mais dans un format beaucoup plus petit et plus flexible.
Ce que cela signifie pour l’usage courant
Pour les non-spécialistes, le message clé est que ce travail transforme un ajustement matériel abstrait en une machine pratique : en organisant soigneusement de minuscules pores et en adaptant la façon dont l’eau mouille — ou ne mouille pas — ces pores, les chercheurs créent une électrode qui « respire » d’elle-même et continue de fonctionner à des débits élevés. De telles électrodes auto-aérées pourraient alimenter des générateurs de peroxyde d’hydrogène sur site pour des usines, des exploitations agricoles ou des stations d’épuration qui se branchent simplement sur de l’électricité renouvelable et l’air ambiant. Si elle était largement déployée, cette approche pourrait réduire l’empreinte environnementale d’un produit courant mais critique tout en rendant des oxydants propres disponibles partout où ils sont nécessaires.
Citation: Tian, Y., Pei, L., Wang, S. et al. A self-breathing electrode enabled by interface regulation and gradient wettability engineering for industrial H2O2 electrosynthesis. Nat Commun 17, 1735 (2026). https://doi.org/10.1038/s41467-026-68436-x
Mots-clés: peroxyde d’hydrogène, électrode à diffusion de gaz, synthèse électrochimique, gradient de mouillabilité, chimie décentralisée