Clear Sky Science · fr
Polarisation du CO2 induite par champ électrique et blocage protons bio-inspiré débloquent la réduction du CO2 en milieu acide fort sans cations métalliques
Transformer un gaz problématique en un ingrédient utile pour les carburants
Le dioxyde de carbone (CO2) est le principal gaz à effet de serre responsable du changement climatique, mais il peut aussi servir de matière première pour fabriquer des carburants et des produits chimiques à partir d’électricité renouvelable. L’un des principaux obstacles est que le CO2 est très peu réactif, notamment en milieux fortement acides où se forme préférentiellement le gaz hydrogène indésirable. Cette étude montre comment un nanomatériau d’or habilement façonné, enveloppé d’un revêtement bio-inspiré, peut surmonter ces difficultés et convertir efficacement le CO2 en monoxyde de carbone (CO) dans des conditions acides sévères, sans recourir aux sels métalliques dissous qui provoquent habituellement des dépôts et du gaspillage.

Pourquoi travailler en milieu acide fort importe
La plupart des appareils qui convertissent électriquement le CO2 fonctionnent dans des liquides neutres ou alcalins. Là, toutefois, le CO2 a tendance à réagir avec le liquide pour former des carbonates et des bicarbonates, gaspillant une grande partie du gaz et réduisant la durée de vie des dispositifs par accumulation solide. Réaliser la réaction en milieu acide fort pourrait éviter ces pertes et mieux valoriser chaque molécule de CO2. Le problème est qu’en milieu acide, les ions hydrogène positifs sont omniprésents et se combinent facilement pour former de l’hydrogène, concurrençant le CO2 pour les électrons à la surface de l’électrode. Parallèlement, les molécules neutres de CO2 n’adhèrent pas facilement aux surfaces métalliques. Les auteurs ont cherché à concevoir un catalyseur et un environnement entourant qui attireraient et activeraient le CO2 tout en tenant les protons à distance, le tout dans une solution acide sans cations métalliques.
Triangles d’or pointus qui suralimentent le CO2
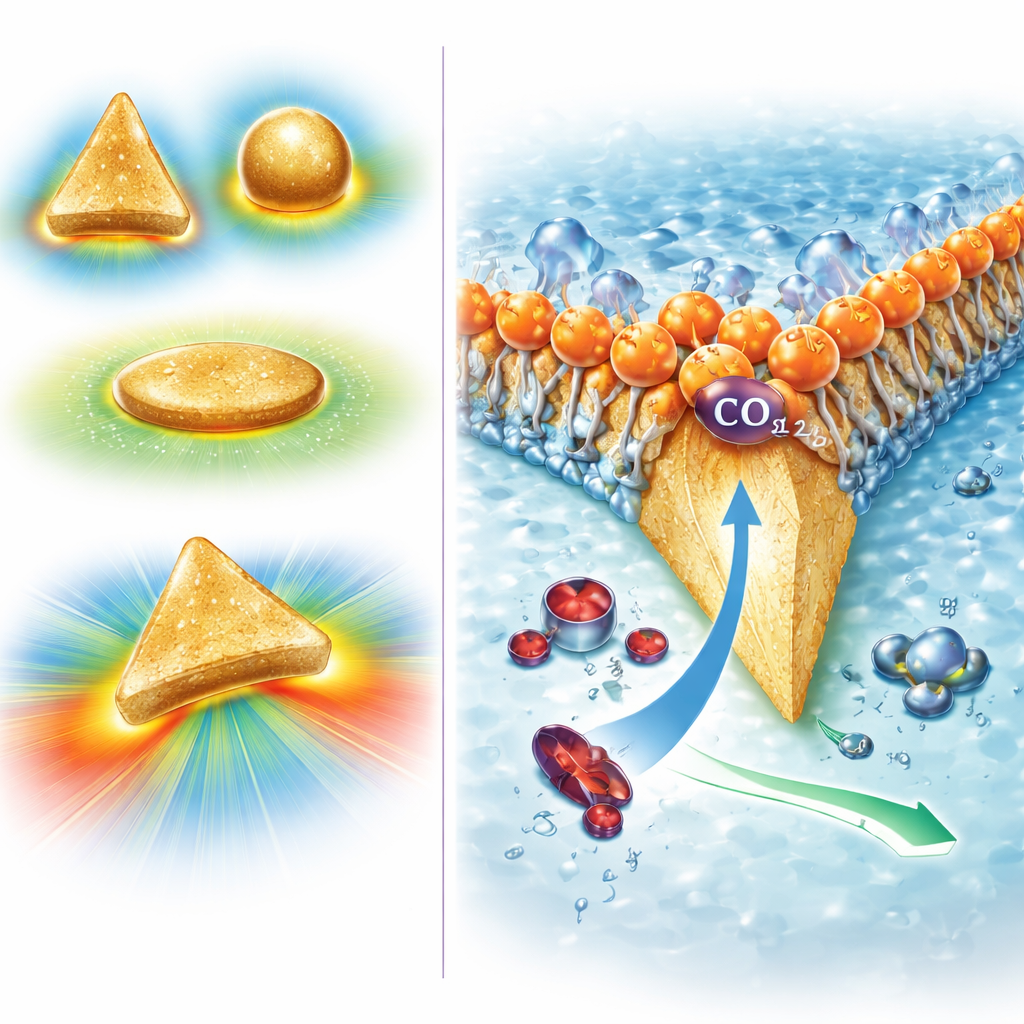
L’équipe a créé de minuscules triangles plats en or d’environ 70 nanomètres de côté, dotés d’angles très aigus. Des simulations informatiques ont montré que lorsqu’une tension est appliquée, la charge électrique se concentre aux pointes acérées, produisant des champs électriques locaux extrêmement intenses — environ dix fois plus forts que sur des particules à bords arrondis. Ces champs intenses déforment la densité électronique des molécules de CO2 voisines, les transformant d’espèces non polaires et symétriques en espèces polarisées avec un dipôle mesurable. Cette déformation étire et plie légèrement les liaisons carbone–oxygène, facilitant l’adsorption et la transformation des molécules à la surface de l’or. Calculs et expériences indiquent que cet effet de champ rend l’adsorption du CO2 pratiquement spontanée et abaisse la barrière énergétique pour la première étape clé de sa conversion en CO, de sorte que la réaction est plus rapide et demande moins d’énergie.
Un revêtement bio‑inspiré qui bloque les protons
Pour résoudre le second problème — la formation excessive d’hydrogène — les chercheurs se sont inspirés des aquaporines, protéines des membranes cellulaires de certains micro-organismes acidophiles. Les aquaporines laissent passer les molécules d’eau neutres tout en bloquant les protons grâce à des charges positives précisément positionnées. En imitant cette idée, les auteurs ont recouvert leurs nanotriangles d’or d’une couche d’un tensioactif chargé positivement appelé CTAC. Cette couche forme une enveloppe douce et ordonnée dont les groupes tête chargés repoussent les protons entrants sans gêner le CO2 neutre. Les expériences ont montré que lorsque ce revêtement cationique est présent, presque tout le courant électrique est consacré à produire du CO plutôt qu’à l’hydrogène, alors que l’or nu ou recouvert différemment produit beaucoup plus d’hydrogène. Des modèles informatiques ont confirmé que la couche chargée ralentit le transport des protons, élève le pH local immédiatement à côté du catalyseur et supprime ainsi la réaction parasite.
Des performances durables
Lorsqu’on a testé les triangles d’or pointus coiffés de CTAC dans un électrolyseur à flux à pH 1, ils ont produit du CO avec une sélectivité proche de 100 % sur une large plage de tensions et ont continué à fonctionner pendant au moins 100 heures à densité de courant élevée. Le rendement énergétique a atteint environ 60 %, ce qui est compétitif voire supérieur à de nombreux systèmes qui s’appuient sur des sels métalliques en milieux moins acides. Les comparaisons avec des formes d’or plus lisses et avec des versions aux pointes arrondies ont montré que la forme triangulaire bidimensionnelle et, surtout, les coins très aigus sont nécessaires pour atteindre ces performances. Le travail démontre une véritable synergie : les champs électriques amplifiés par la géométrie attirent et activent le CO2, tandis que le revêtement chargé bio‑inspiré façonne la chimie locale pour tenir les protons à l’écart.
Ce que cela signifie pour les futurs appareils d’énergie propre
Pour les non-spécialistes, le message principal est que cette recherche propose une nouvelle recette pour convertir le CO2 en une matière première utile dans des conditions qui semblaient auparavant défavorables. En empruntant des idées à la biologie et en exploitant la physique des pointes acérées, les auteurs montrent qu’il est possible d’effectuer la conversion du CO2 en milieu acide fort sans ions métalliques ajoutés, évitant l’accumulation de sels et améliorant l’usage du CO2. Si ces catalyseurs sont mis à l’échelle et intégrés à une énergie renouvelable, ils pourraient aider à transformer le CO2 d’un déchet en un élément de base pour des carburants et produits chimiques neutres en carbone, tout en rendant les dispositifs électrochimiques plus robustes et plus faciles à exploiter.
Citation: Chen, L., Guo, Z., Huang, HZ. et al. Electric-field-driven CO2 polarization and bioinspired proton blocking unlock CO2 reduction in strong acid without metal cations. Nat Commun 17, 1734 (2026). https://doi.org/10.1038/s41467-026-68435-y
Mots-clés: électroréduction du CO2, électrolyseur acide, nanocatalyseur en or, amplification du champ électrique, blocage des protons