Clear Sky Science · fr
Amélioration de l’extinction de gènes in vivo avec une haute spécificité grâce à des ARNg Cas12a multiplexés
Éditer les gènes de façon plus fiable
L’édition génomique ouvre de nouvelles façons d’étudier la biologie, de traiter des maladies et même de contrôler des ravageurs, mais chez les animaux vivants elle fonctionne souvent moins proprement que ne le laissent entendre les gros titres. De nombreuses cellules échappent à l’édition ou ne sont que partiellement modifiées, ce qui peut brouiller les résultats expérimentaux et limiter les usages pratiques. Cet article décrit une nouvelle méthode basée sur CRISPR chez la drosophile qui rend les extinctions de gènes plus complètes et plus précises, offrant une feuille de route pour une édition du génome plus fiable dans des organismes complexes.
Pourquoi le CRISPR classique fait souvent défaut
Les outils CRISPR traditionnels comme Cas9 coupent l’ADN en un point choisi en utilisant un seul ou quelques ARN guides. Dans les animaux vivants, cette approche rencontre plusieurs obstacles. Certains guides fonctionnent tout simplement mal ; certains sites cibles sont difficiles d’accès pour l’enzyme ; et la machinerie de réparation de la cellule restaure souvent la cassure par de petites modifications qui laissent le gène fonctionnel. Le résultat est un mosaïque : des cellules voisines dans un même tissu peuvent porter des mutations différentes, ou n’en porter aucune. Cette hétérogénéité rend difficile d’observer l’effet d’une véritable mise hors service d’un gène, et pose un défi pour des applications comme la thérapie génique ou les drives génétiques qui doivent agir efficacement dans la plupart des cellules.
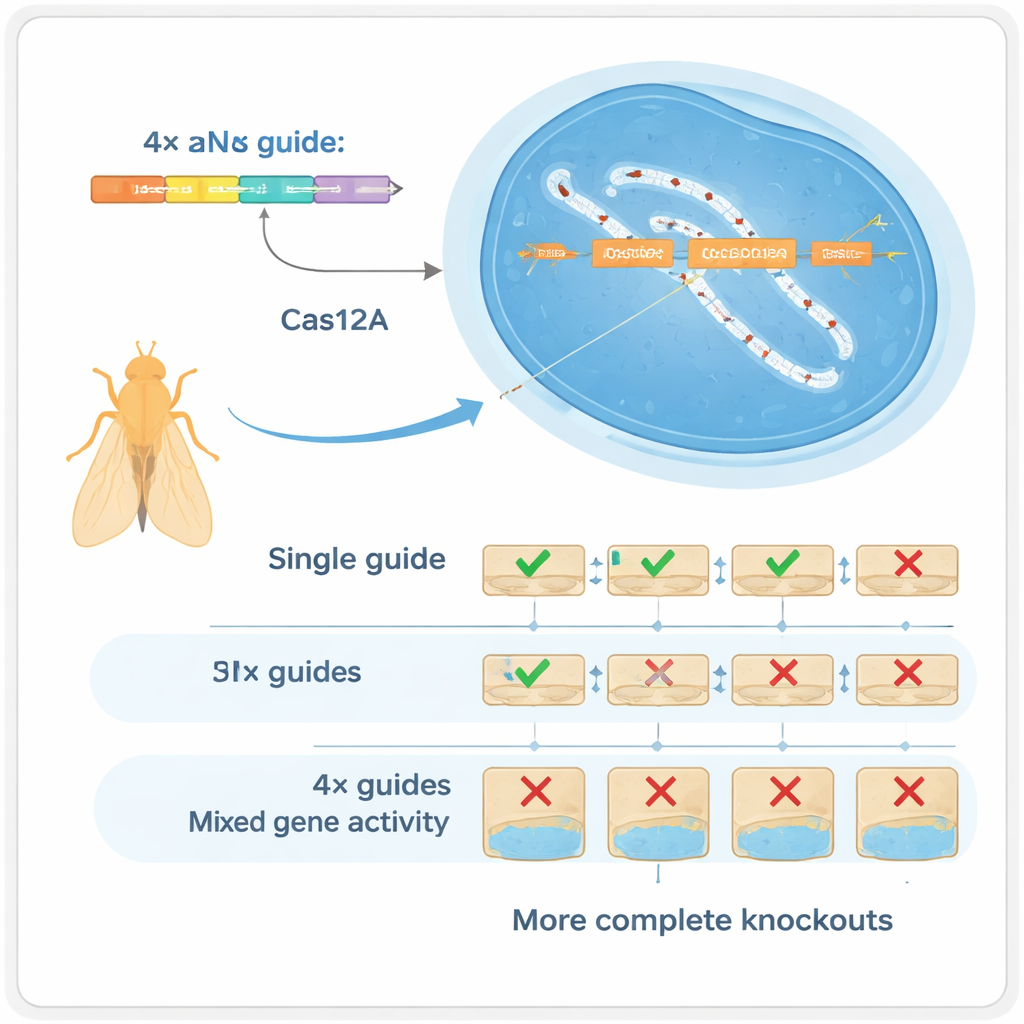
Quatre guides valent mieux qu’un
Les auteurs se sont tournés vers une autre enzyme CRISPR, Cas12a, qui peut traiter des bancs compacts de guides bien plus aisément que Cas9. Ils ont développé une boîte à outils pour Drosophila dans laquelle chaque gène est ciblé par un ensemble de quatre ARN guides, tous codés sur un petit fragment d’ADN unique qui peut être produit en masse. Dans des tests soigneusement contrôlés, ils montrent que l’utilisation de quatre guides par gène modifie radicalement les types de changements d’ADN produits : au lieu de petites insertions ou délétions isolées en un seul site, le système génère fréquemment de plus grandes délétions entre sites de coupure qui détruisent presque toujours la fonction du gène. Ce « multiplexage » agit de deux manières : si un guide échoue, d’autres peuvent encore faire le travail (redondance), et lorsque plusieurs coupent simultanément ils peuvent retirer de plus gros fragments du gène (synergie).
Haute efficacité sans dommages collatéraux supplémentaires
Créer plus de cassures de l’ADN soulève des questions évidentes de sécurité. Plusieurs coupures dans une même région pourraient-elles effacer accidentellement des gènes voisins ? Des guides pourraient-ils mal cibler d’autres régions du génome plus fréquemment ? Pour répondre à ces questions, les chercheurs ont mesuré la mortalité cellulaire, évalué les effets sur les gènes voisins, et inventé un test astucieux pour visualiser les événements de réparation chromosomique appelé perte d’hétérozygotie sur de larges étendues d’ADN. Ils ont constaté que regrouper quatre coupures au sein d’un même gène était bien toléré : cela n’augmentait pas la mortalité cellulaire par rapport aux approches Cas9 conventionnelles et perturbait rarement les gènes voisins, sauf si un guide atterrissait extrêmement près d’un élément régulateur. Des criblages à grande échelle utilisant plus de 2 000 guides sur un tiers du génome de la mouche ont montré que plus de 99 % des ensembles de guides étaient actifs sur leur cible prévue, tandis que l’activité hors cible reproductible était inférieure à 1 %, indiquant une très haute spécificité même en configuration multiplexée.
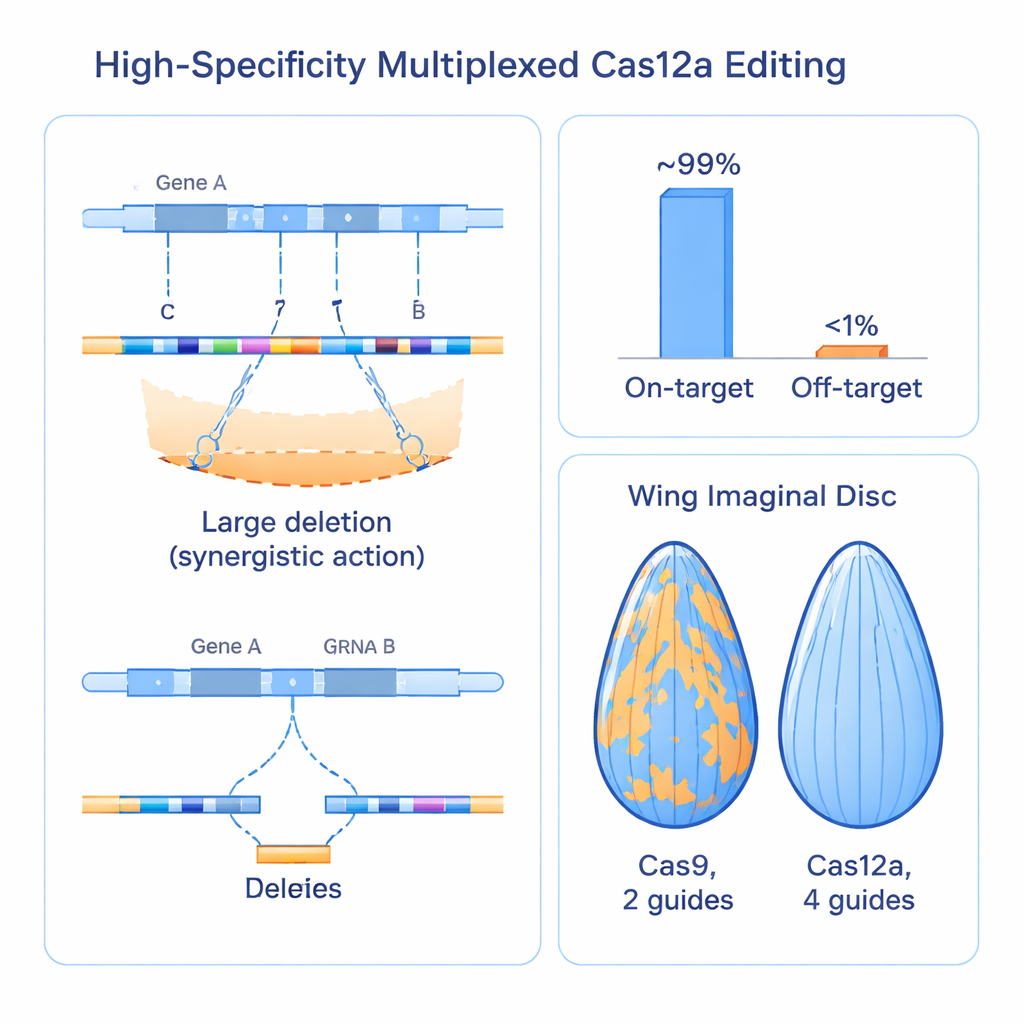
Devancer les systèmes Cas9 établis dans des tissus réels
Pour vérifier si ces améliorations moléculaires se traduisent par une biologie plus nette, l’équipe a comparé son système Cas12a à quatre guides directement aux ressources Cas9 largement utilisées, en ciblant plus de 100 gènes chez la mouche. Dans des tissus tels que l’œil, l’intestin et l’aile en développement, l’approche Cas12a a produit des pertes de fonction plus fortes et plus uniformes que Cas9, qui laissait souvent des zones visibles de tissu non édité et normal. Lorsqu’ils ont utilisé la taille de l’aile comme mesure quantitative, le nouveau système a régulièrement généré des défauts de croissance plus importants et plus reproductibles pour des régulateurs connus, révélant que certains gènes auparavant classés comme faibles ou non essentiels avaient en fait été manqués parce que les anciens outils ne les inactivaient pas suffisamment. La puissance accrue de la méthode a même mis en évidence un rôle essentiel jusqu’alors inconnu d’un gène appelé trade embargo dans le développement et la survie de l’aile.
Ce que cela signifie pour l’avenir de l’édition génique
En termes simples, ce travail montre comment transformer CRISPR, parfois perçu comme un scalpel imparfait, en un interrupteur plus décisif pour éteindre les gènes chez des animaux vivants. En combinant Cas12a avec quatre guides par gène, les auteurs obtiennent des extinctions quasi complètes avec des effets non voulus très faibles, le tout dans un format pratique à déployer sur des centaines de gènes. Bien que développé chez la drosophile, les principes sous-jacents — utiliser plusieurs guides pour la redondance et la synergie, et vérifier soigneusement les effets chromosomiques secondaires — sont largement applicables. Cette stratégie pourrait améliorer la recherche fondamentale, affiner les criblages génétiques et éclairer des conceptions plus sûres pour de futures applications médicales et écologiques de l’édition génique.
Citation: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Mots-clés: CRISPR, Cas12a, extinction de gène, Drosophile, spécificité de l’édition du génome