Clear Sky Science · fr
Utilisation dynamique des allèles des gènes liés à l’X atténue les phénotypes de maladies neurodéveloppementales dans des organoïdes cérébraux
Comment le chromosome X « silencieux » aide à protéger le cerveau
Chaque cellule d’une femme porte deux chromosomes X, mais pendant des décennies les manuels de biologie ont présenté l’un d’eux comme largement éteint — comme un livre de réserve laissé fermé sur une étagère. Cette étude montre que, surtout dans le cerveau en développement, ce X « silencieux » ressemble davantage à une bibliothèque de secours dynamique. Il peut être sollicité quand c’est nécessaire, et cette flexibilité supplémentaire pourrait aider à expliquer pourquoi de nombreux troubles du développement cérébral touchent davantage les hommes que les femmes.
Un système de secours caché sur le chromosome X
Chez les mammifères femelles, un chromosome X par cellule est désactivé tôt au cours du développement pour éviter un double dosage des gènes liés à l’X. Pourtant, les scientifiques savent depuis longtemps que certains gènes peuvent « échapper » à cette extinction. Le travail nouveau pose une question plus profonde : cet échappement est‑il fixé, ou peut‑il changer au fur et à mesure du développement cellulaire ? En utilisant des cellules souches humaines et de petits tissus cérébraux appelés organoïdes, les chercheurs ont suivi quelle copie de chaque gène lié à l’X — maternelle ou paternelle — était utilisée lorsque les cellules mûrissaient, passant de cellules souches à des neurones. Ils ont constaté que de nombreux gènes sur le X supposé inactif s’allument et s’éteignent selon des stades et des types cellulaires spécifiques, plutôt que de suivre une règle simple marche/arrêt.
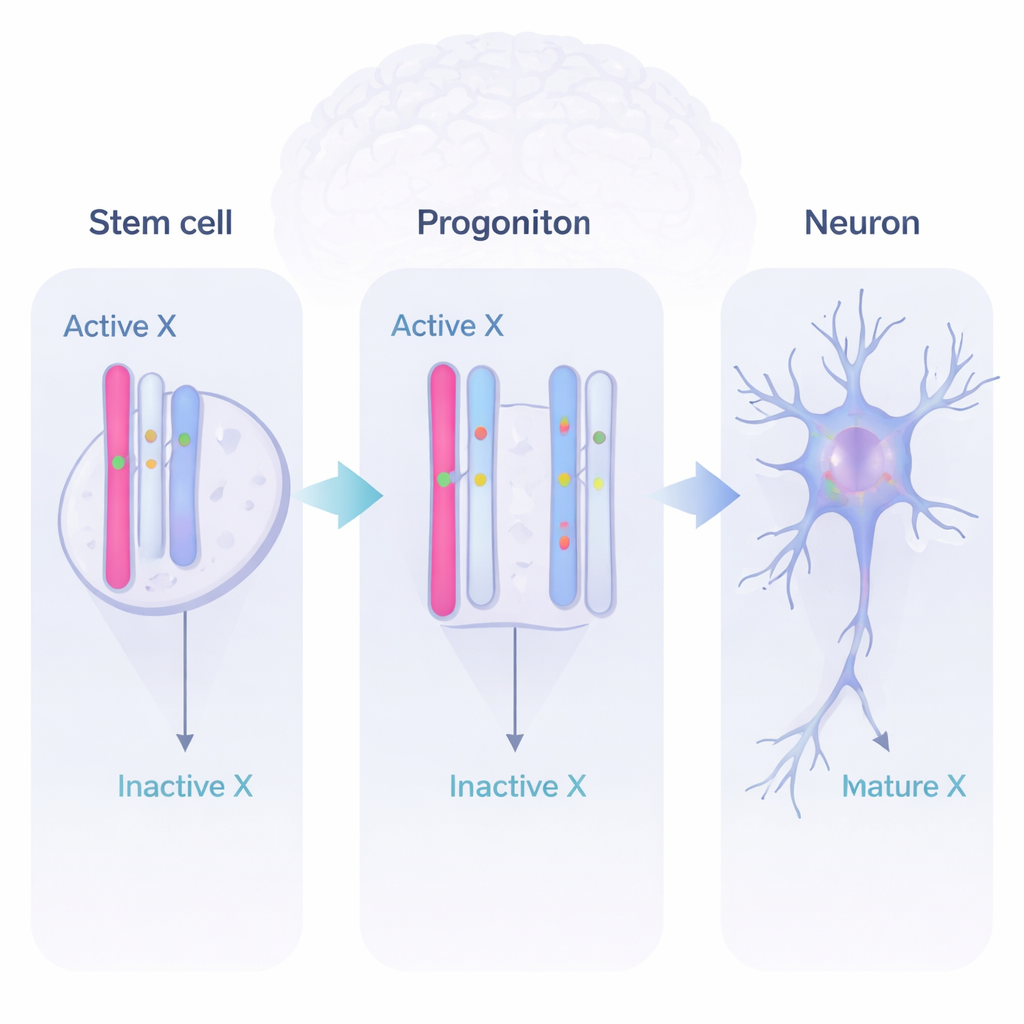
Utilisation dynamique des gènes durant le développement cérébral
En lisant l’ARN (les messages produits à partir des gènes) et en distinguant les deux copies parentales, l’équipe a identifié trois comportements majeurs. Certains gènes restaient pour l’essentiel éteints sur le X inactif, comme prévu. D’autres étaient des « échappés complets », actifs à partir des deux copies du X à tous les stades. Plus intrigant, un groupe important de gènes montrait un comportement dynamique. Ces gènes étaient silencieux sur le X inactif dans les cellules souches, s’activaient depuis les deux chromosomes X dans les progéniteurs neuronaux et les premiers neurones, puis certains se rééteignaient plus tard. Cela montre que le X inactif n’est pas un cimetière statique de gènes mais un réservoir flexible que le cerveau en développement peut exploiter lorsque une activité génique supplémentaire est utile.
Motifs conservés et liens avec les troubles cérébraux
Lorsque les chercheurs ont comparé leurs données humaines à des études chez la souris et à des marques chimiques sur l’ADN de tissus cérébraux fœtaux, ils ont trouvé que cet échappement dynamique à l’inactivation du X se retrouve chez d’autres mammifères et est lié aux états de la chromatine — des caractéristiques de l’emballage de l’ADN qui contrôlent la facilité d’activation des gènes. Les gènes se réactivant avaient tendance à se regrouper dans certaines régions du chromosome X et portaient des signatures épigénétiques d’ADN actif spécifiquement dans le tissu cérébral féminin. D’un point de vue médical, ces gènes dynamiquement réactivés étaient exceptionnellement riches en gènes de risque connus pour des troubles du neurodéveloppement tels que la déficience intellectuelle et les troubles du spectre autistique, ce qui suggère que cette flexibilité a évolué comme un mécanisme protecteur.
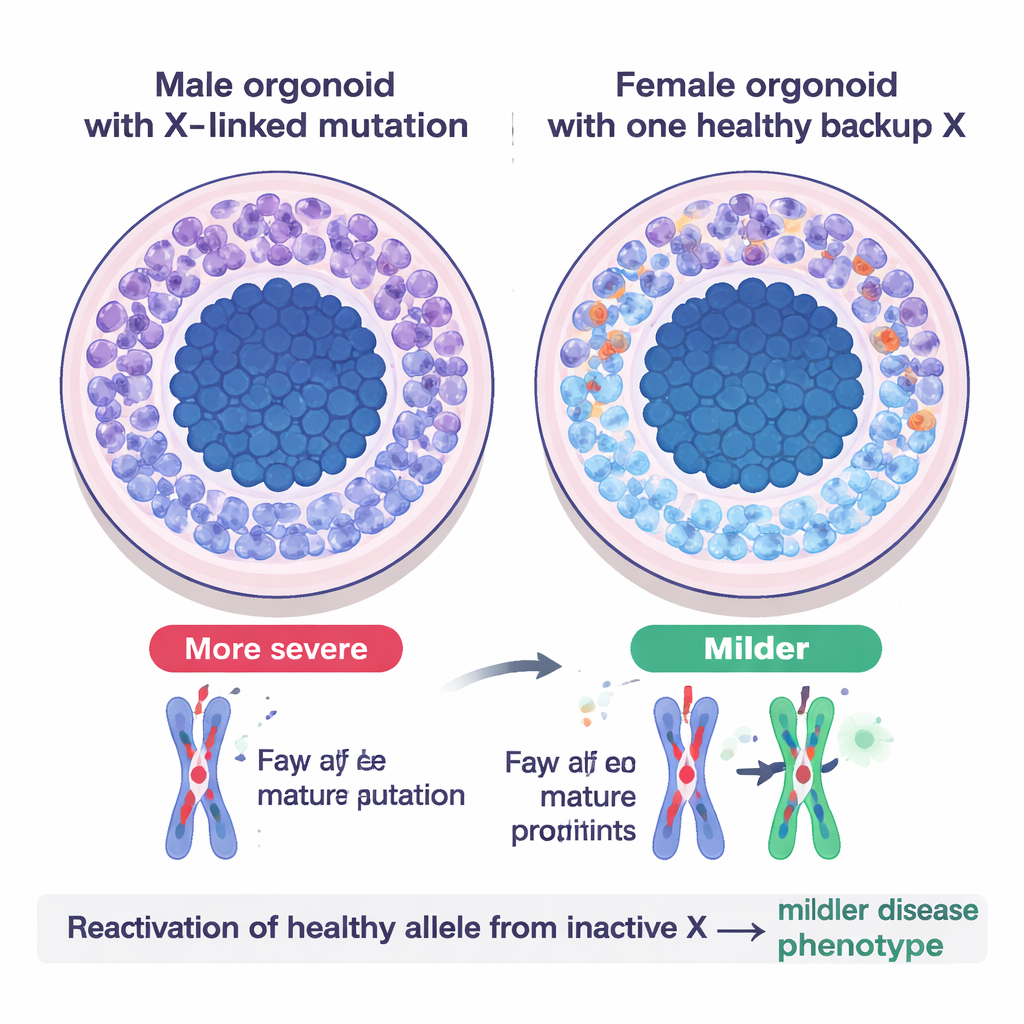
Un test concret : le syndrome Opitz BBB/G
Pour voir comment ce système de secours se manifeste en maladie, l’équipe a modélisé le syndrome Opitz BBB/G, une affection liée à l’X rare qui affecte les structures médianes du cerveau et provoque souvent un retard de développement. Le trouble est causé par des mutations délétères dans un gène appelé MID1 sur le chromosome X. Dans des organoïdes cérébraux cultivés à partir de cellules de patients masculins — où il n’y a qu’une seule copie du X — les neurones étaient rares et les cellules souches neurales restaient trop longtemps dans un état de division, reflétant l’hypoplasie cérébrale observée chez les patients. Les organoïdes féminins portant la même mutation sur leur X actif, mais une copie saine sur le X inactif, semblaient nettement en meilleure santé : ils produisaient plus de neurones et présentaient des défauts moins marqués. Lorsque les scientifiques ont modifié des lignées féminines pour que les deux copies du X portent la mutation, les organoïdes ont développé des problèmes sévères, semblables à ceux observés chez les mâles, confirmant que l’allèle sain précédemment inactif avait été réactivé et contribuait à compenser.
Ce que cela signifie pour les différences entre sexes dans les maladies cérébrales
L’étude révèle que le deuxième chromosome X « silencieux » chez les femelles n’est pas simplement une masse génétique inerte. Durant des fenêtres clés du développement cérébral, des gènes sélectionnés sur ce X inactif s’activent dans des types cellulaires spécifiques, augmentant le nombre de copies géniques fonctionnelles. Pour des gènes comme MID1, cruciaux pour la construction du cerveau, cette réactivation dynamique peut atténuer l’impact de mutations délétères et produire des symptômes féminins plus légers et plus variables. En d’autres termes, le cerveau féminin dispose d’un système de secours interne qu’il peut moduler au fil du temps, ce qui aide à expliquer pourquoi de nombreux troubles neurodéveloppementaux liés à l’X sont moins fréquents ou moins graves chez les filles que chez les garçons.
Citation: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Mots-clés: inactivation du chromosome X, organoïdes cérébraux, troubles du neurodéveloppement, dosage génique, différences entre sexes dans la maladie