Clear Sky Science · fr
Shigella flexneri échappe à l’immunité cellule-autonome médiée par les septines via l’ADP-riboxanation des protéines
Comment certaines bactéries intestinales contournent notre système de sécurité interne
La diarrhée sévère causée par les bactéries Shigella reste un problème majeur dans le monde, en particulier chez les jeunes enfants. Nos cellules ne sont pas sans défense : elles disposent d’outils intégrés capables d’attraper et de détruire les microbes envahisseurs. Cette étude révèle comment Shigella flexneri, une cause principale de dysenterie, utilise des ruses moléculaires pour démanteler l’un de ces dispositifs, facilitant la dissémination de la bactérie de cellule en cellule dans l’intestin.
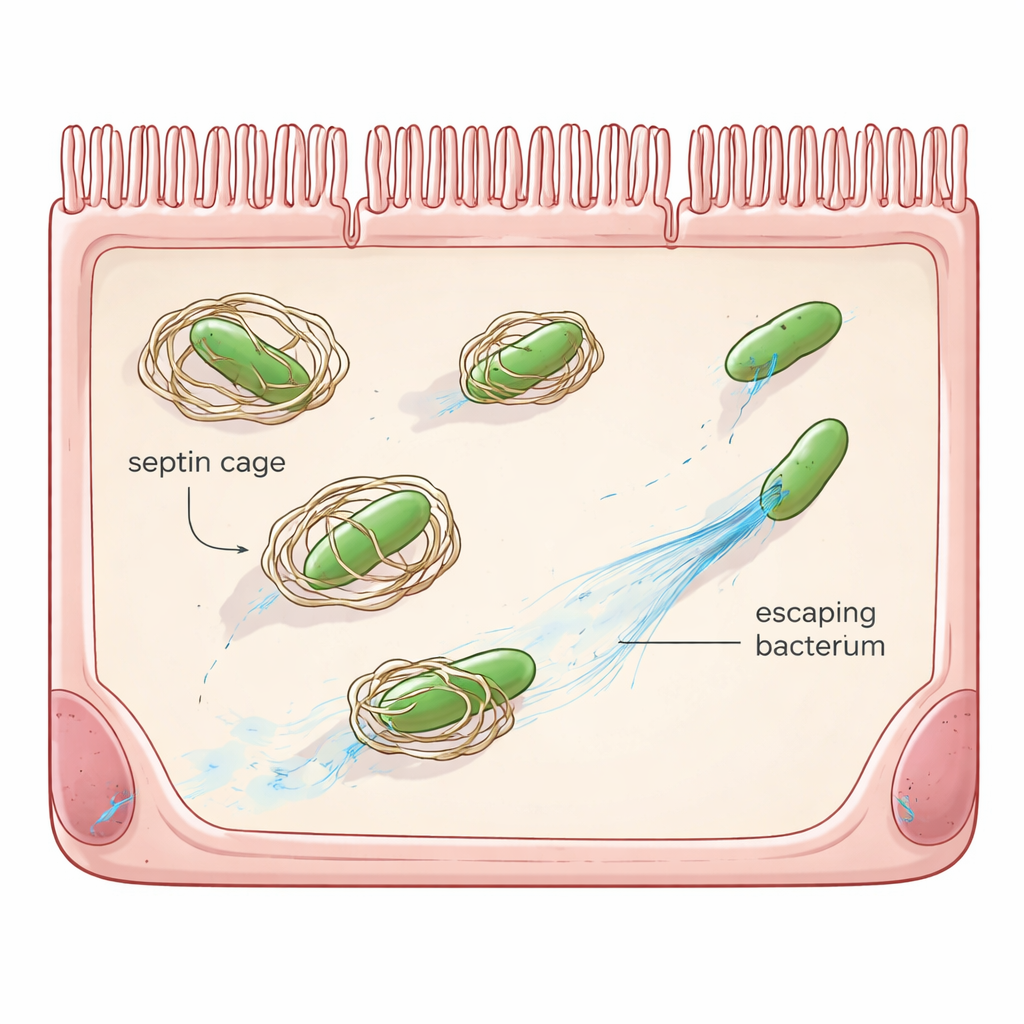
La défense « faites-le vous-même » de la cellule
Au-delà des globules blancs et des anticorps, de nombreuses cellules ordinaires possèdent leurs propres systèmes de sécurité d’urgence, appelés immunité cellule-autonome. Un de ces systèmes repose sur les septines, une famille de protéines échafaudage qui forment des anneaux et des structures en forme de cage. Lorsque Shigella pénètre dans une cellule et s’échappe dans le cytosol visqueux, les septines peuvent s’assembler autour de la bactérie, empêchant sa mobilité et signalant sa destruction par les voies de recyclage cellulaires. Des travaux antérieurs avaient montré que Shigella dispose déjà d’une contre-mesure, une protéine appelée OspG, qui marque les septines pour élimination. Pourtant, même en l’absence d’OspG, la majorité des bactéries échappent toujours à la mise en cage, laissant penser que Shigella possède d’autres stratagèmes.
Démasquer un second saboteur bactérien
Les auteurs se sont intéressés à un autre groupe de protéines de Shigella, connu sous le nom de famille OspC. En utilisant une approche globale de cartographie des protéines dans des cellules humaines, ils ont recherché les protéines hôtes qui subissaient des modifications chimiques en présence des protéines OspC. Outre des cibles connues impliquées dans la synthèse protéique, ils ont trouvé que plusieurs septines, en particulier une appelée SEPT9, étaient systématiquement marquées. Des tests biochimiques détaillés ont montré que trois protéines OspC peuvent directement fixer une petite étiquette riche en énergie, dérivée de la molécule NAD, sur de nombreux sites des septines. Cette modification chimique, appelée ADP-riboxanation, est une variante spéciale et irréversible d’une modification protéique plus courante.
Démanteler l’échafaudage protéique de l’intérieur
Pour comprendre comment cette étiquette chimique affaiblit les défenses cellulaires, l’équipe s’est concentrée sur SEPT9. Les septines forment normalement des chaînes ordonnées de huit unités, qui s’alignent ensuite en filaments puis se consolident en cages autour des bactéries. Les chercheurs ont découvert qu’une position particulière de SEPT9, un acide aminé nommé arginine 561, constitue le site principal d’ADP-riboxanation durant l’infection. Des études structurelles et des expériences de reconstitution avec des protéines purifiées ont montré que ce site se situe à une surface de contact critique où deux unités de SEPT9 s’emboîtent. Lorsque cette arginine est chimiquement modifiée — ou remplacée par un résidu qui imite la charge négative ajoutée — les chaînes octamériques se désagrègent en fragments plus petits et ne peuvent plus assembler des filaments stables.
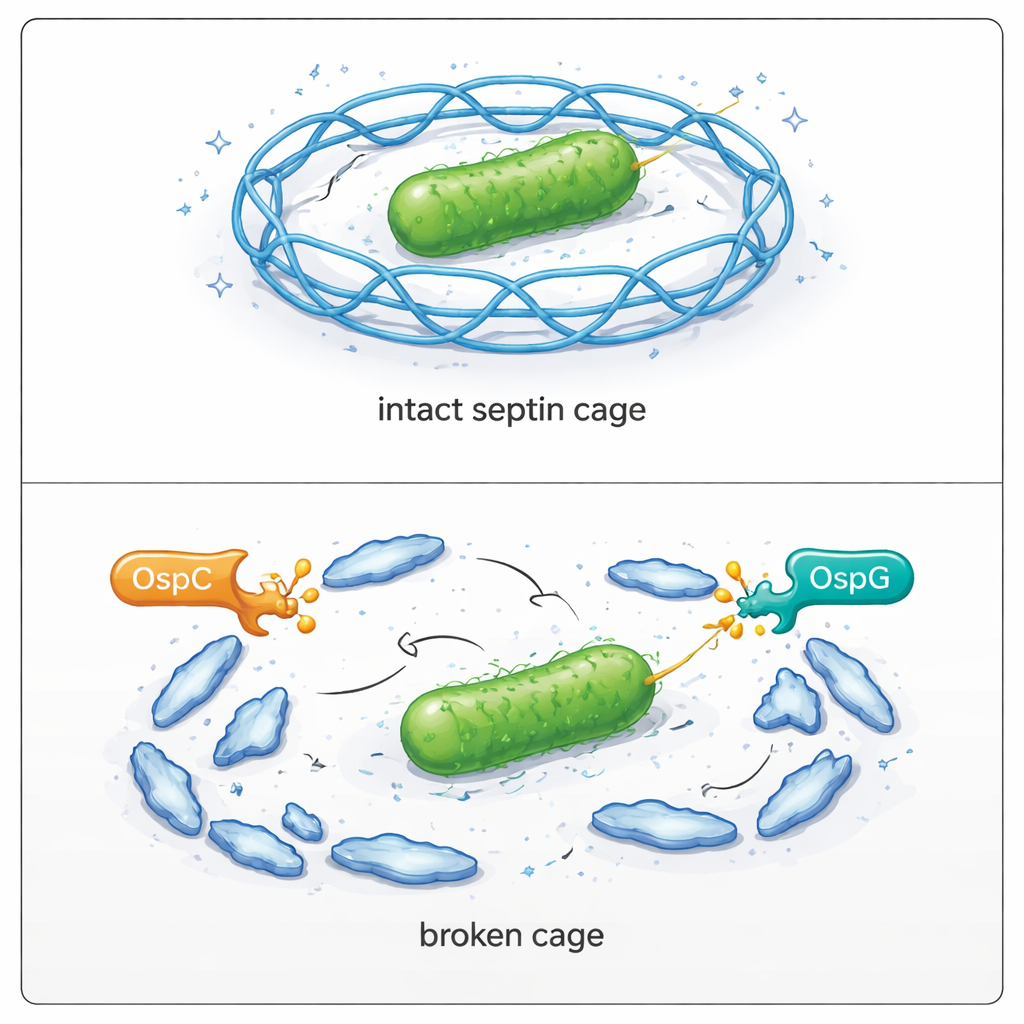
Observer l’échec des cages dans des cellules infectées
L’équipe est ensuite retournée dans des cellules vivantes pour observer les conséquences. Dans des cellules humaines infectées par Shigella sauvage, seule une minorité de bactéries se retrouvent enfermées dans des cages de septines. Lorsque toutes les protéines OspC sont supprimées génétiquement, la proportion de bactéries mises en cage double presque. La suppression d’OspG produit un effet similaire, et la suppression conjointe d’OspC et d’OspG augmente encore la formation de cages et compromet fortement la capacité des bactéries à se propager à travers une couche cellulaire. La réintroduction de protéines OspC actives dans les souches mutantes a rétabli leur capacité à échapper aux cages ainsi qu’à se répliquer et former de grandes plaques. La microscopie a confirmé que lorsque SEPT9 ne peut pas être modifié à l’arginine 561, il s’intègre efficacement aux cages ; lorsqu’il est altéré par OspC, la formation de cages autour des bactéries chute fortement.
Quelles implications pour lutter contre Shigella
En termes accessibles, ce travail montre que Shigella possède une paire coordonnée d’outils moléculaires destinée à briser les barreaux d’une « prison » intracellulaire. OspC affaiblit directement les éléments protéiques nécessaires à la construction des cages de septines, tandis qu’OspG favorise leur élimination par une autre voie chimique. Ensemble, ces stratégies permettent aux bactéries de s’échapper, de se déplacer à l’intérieur des cellules et d’envahir les voisines. La compréhension de ces mécanismes d’évasion précis enrichit non seulement notre connaissance du fonctionnement de l’immunité intrinsèque des cellules, mais indique aussi de nouvelles pistes thérapeutiques : des médicaments qui bloquent OspC ou protègent les contacts clés des septines pourraient aider à restaurer la capacité naturelle des cellules à piéger et éliminer ce pathogène dangereux.
Citation: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Mots-clés: Shigella, cages de septines, immunité cellule-autonome, facteurs de virulence bactériens, ADP-ribosylation