Clear Sky Science · fr
Produits naturels peptidiques ciblant ClpC1 déréglent différemment le protéome de Mycobacterium tuberculosis
Pourquoi perturber les équipes de nettoyage bactériennes importe
La tuberculose reste l’une des maladies infectieuses les plus meurtrières au monde, et les souches résistantes de Mycobacterium tuberculosis compliquent de plus en plus le traitement. La plupart des antibiotiques actuels ciblent la paroi bactérienne, la production d’énergie ou la réplication de l’ADN. Cette étude explore une faiblesse très différente : l’« équipe de nettoyage » interne de la cellule qui maintient la santé des protéines. En comprenant comment de nouvelles molécules dérivées de produits naturels perturbent ce système de ménage, les scientifiques espèrent concevoir de futurs médicaments capables d’éliminer les bactéries responsables de la tuberculose de façons nouvelles et plus durables.
Le centre de gestion des protéines de la cellule
Comme toutes les cellules vivantes, la bactérie de la tuberculose construit, replie, répare et recycle en permanence ses protéines. Un acteur central de ce réseau de gestion protéique est une grande machinerie nommée complexe ClpC1–ClpP1P2. Une partie (ClpC1) agit comme une chaperonne, reconnaissant et attirant les protéines endommagées ou inutiles, tandis que l’autre partie (ClpP1P2) les découpe en fragments pour le recyclage. Ce système est essentiel à la survie de la bactérie, surtout en condition de stress comme la chaleur ou l’attaque par des antibiotiques. Plusieurs peptides naturels — l’ecumicine, les ilamycines (rufomycines) et les cyclomarines — sont déjà connus pour se lier à ClpC1 et présenter une forte activité anti‑TB, ce qui suggère que ce complexe pourrait constituer une cible médicamenteuse puissante. 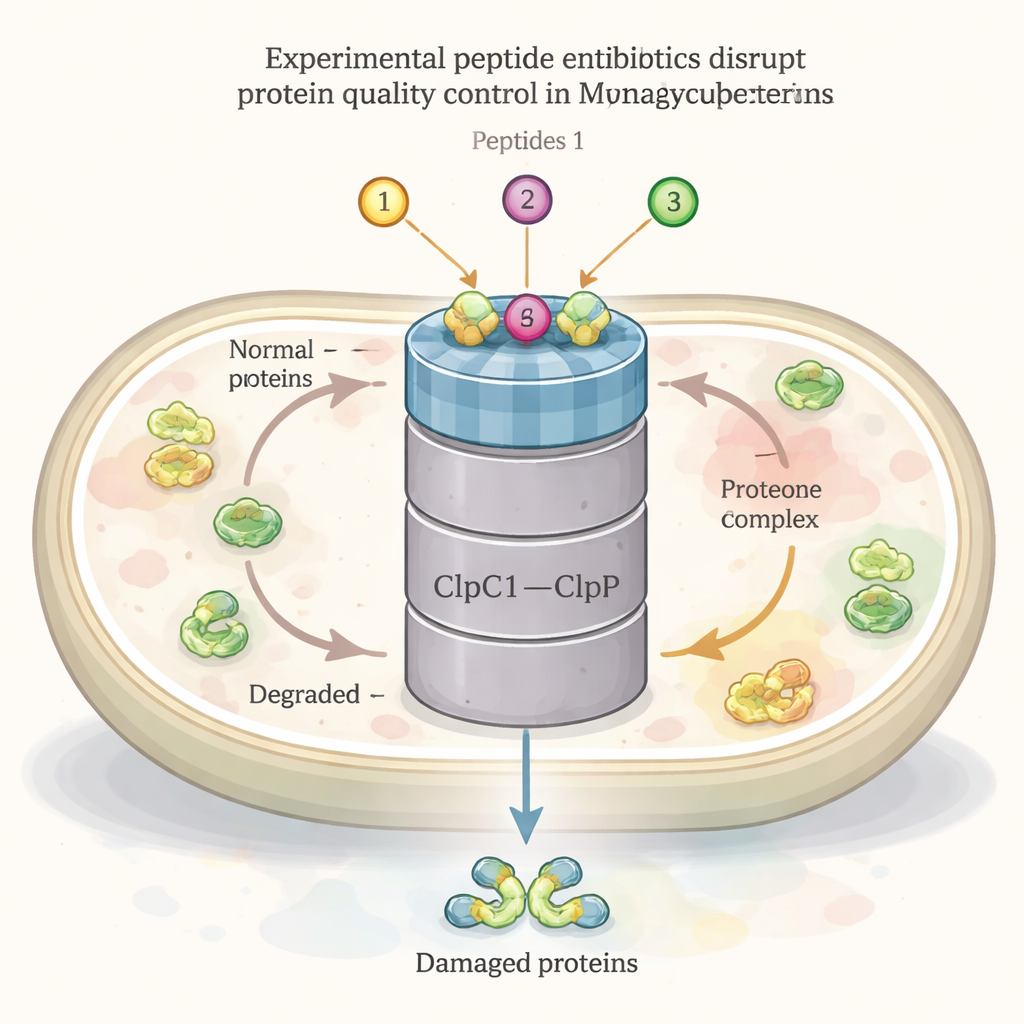
Trois médicaments apparentés, trois impacts différents
Les chercheurs ont examiné un représentant de chacune des trois familles peptidiques : un analogue d’ecumicine (Ecu*), l’ilamycine E (IlaE) et un dérivé de cyclomarine (desoxycyclomarine, dCym). Bien que les trois se fixent sur la même région de ClpC1, ils ne se comportent pas de la même manière à l’intérieur de la cellule. En utilisant la protéomique quantitative — une approche qui mesure des milliers de protéines simultanément — ils ont constaté que Ecu* provoquait la perturbation la plus large, modifiant de façon significative près de 17 % de l’ensemble des protéines bactériennes. IlaE affectait environ 12 % et dCym environ 7 %. Seules 72 protéines étaient systématiquement touchées par les trois composés, et la plupart d’entre elles voyaient leur abondance diminuer. Cela montre que chaque molécule oriente la machine ClpC1 dans une direction différente, remodelant le paysage protéique de la cellule de façons distinctes plutôt que de simplement « éteindre la machine ».
Boucher le broyeur versus couper l’alimentation
Pour mettre ces effets en perspective, l’équipe a comparé les peptides au bortézomib, un médicament anticancéreux qui bloque largement les enzymes responsables de la dégradation des protéines. Chez la bactérie de la TB, le bortézomib entraînait une accumulation générale de nombreuses protéines, comme attendu lorsque les broyeurs sont désactivés. En revanche, les peptides produisaient des profils plus sélectifs : certaines cibles connues de ClpC1 s’accumulaient, d’autres étaient appauvries, et on n’observait pas une inhibition globale de toutes les voies de dégradation protéique. Des tests détaillés en laboratoire avec des composants purifiés ont montré que chaque peptide modifiait la façon dont des substrats spécifiques étaient traités. Par exemple, les trois interférèrent avec la destruction d’une protéine régulatrice (PanD), mais seul Ecu* bloquait la dégradation d’une protéine modèle désordonnée, et seul dCym altérait la dégradation de la protéine protectrice contre le stress Hsp20. Ces différences suggèrent que la conformation globale et la flexibilité de chaque protéine cible influencent la manière dont elle est affectée lorsque ClpC1 est « déréglé » par un composé donné. 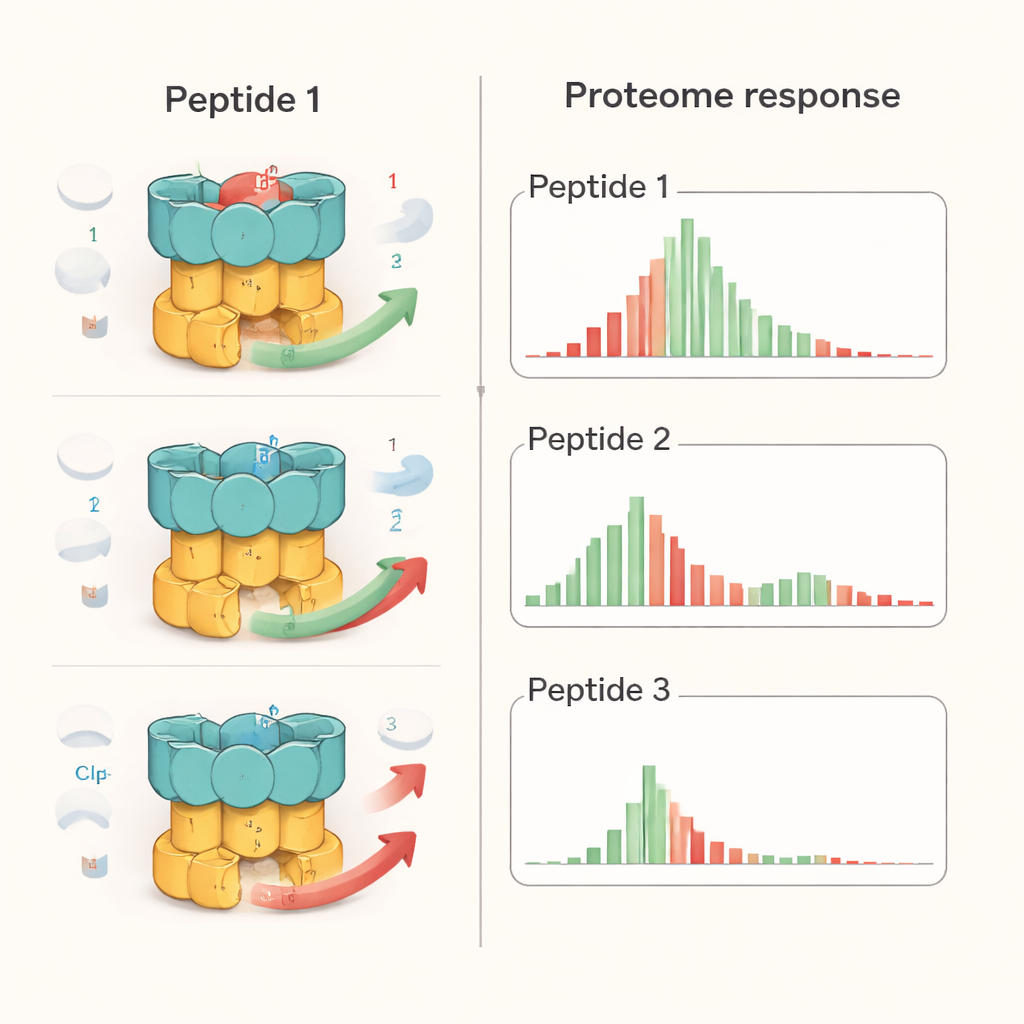
Répondeurs au stress et auto‑sauvetage bactérien
La bactérie de la TB dispose de systèmes de secours pour faire face quand les dommages protéiques submergent la machinerie principale de nettoyage. L’un de ces systèmes implique une autre chaperonne, ClpC2, qui peut se lier à des molécules de type cyclomarine et en réduire l’impact sur ClpC1. Cette étude a montré que, bien que les trois peptides puissent se lier à ClpC2 in vitro, seul le dérivé de cyclomarine (dCym) déclenchait réellement une augmentation des niveaux de ClpC2 dans des bactéries vivantes et devenait plus puissant lorsque ClpC2 était réduit expérimentalement. En revanche, Ecu* et IlaE restaient efficaces même lorsque ClpC2 était diminué, ce qui suggère qu’ils contournent en grande partie cette voie d’auto‑sauvetage. L’équipe a également découvert un lien fort et spécifique aux composés avec Hsp20, une petite protéine qui aide à prévenir la formation d’amas toxiques : Ecu* (et dans une moindre mesure IlaE) provoquait des augmentations spectaculaires du niveau de Hsp20 et Ecu* se liait directement à Hsp20, révélant une nouvelle connexion entre ces candidats‑médicaments et le réseau de réponse au stress de la cellule.
Transformer le stress en avantage thérapeutique
Parce que le système ClpC1 est particulièrement important en condition difficile, les chercheurs ont testé les médicaments alors que les bactéries subissaient un stress thermique léger, ce qui augmente la charge de protéines mal repliées. Dans ces conditions, Ecu* et dCym devenaient beaucoup plus létaux, atteignant une toxicité comparable à celle du bortézomib, bien qu’ils agissent de manière plus sélective. Cela démontre que cibler finement la machinerie de contrôle qualité des protéines peut être aussi efficace que d’éteindre l’ensemble des protéases majeures, mais avec un contrôle potentiellement plus précis. Le travail a également montré que nombre des changements induits par Ecu* dans les niveaux protéiques ne se limitaient pas à refléter des variations de l’activité génique, soulignant que la perturbation de ClpC1 affecte principalement la régulation post‑traductionnelle.
Ce que cela signifie pour les traitements futurs de la TB
Pour les non‑spécialistes, le message clé est que les bactéries de la TB dépendent d’un système interne d’entretien et de réponse au stress finement équilibré pour survivre. Les trois peptides dérivés de produits naturels testés ici ciblent tous la même machinerie centrale mais la poussent dans des modes différents, entraînant des distorsions diverses et très spécifiques de la composition protéique de la bactérie. Fait important, les composés de type ecumicine et ilamycine évitent un mécanisme de secours bactérien qui peut atténuer l’effet des cyclomarines, tout en paralysant l’agent pathogène sous stress. Ces propriétés font d’eux des échafaudages prometteurs pour de futurs médicaments antituberculeux, y compris des molécules conçues pour forcer les cellules de la TB à détruire sélectivement leurs propres protéines vitales ou à être intégrées dans des « chimères dirigeant les protéines » pour orienter précisément l’autodigestion bactérienne.
Citation: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Mots-clés: tuberculose, qualité des protéines, ClpC1, résistance aux antibiotiques, antibiotiques issus de produits naturels