Clear Sky Science · fr
Profilage épigénomique simultané et mesure de l’activité régulatrice avec e2MPRA
Lire les interrupteurs cachés de la cellule
Toutes les cellules de votre corps portent essentiellement le même ADN, pourtant une cellule cérébrale et une cellule hépatique se comportent très différemment. Le secret réside dans de courtes séquences d’ADN qui agissent comme des variateurs d’intensité pour les gènes, les augmentant, les diminuant ou les éteignant. Cette étude présente un nouvel outil puissant, appelé e2MPRA, qui permet aux scientifiques de tester des milliers de ces interrupteurs simultanément tout en observant comment l’ADN est emballé et marqué à l’intérieur de la cellule — des étapes clés pour comprendre le développement, le risque de maladie et pourquoi certaines variantes génétiques ont de l’importance tandis que d’autres n’en ont pas.
Des cartes de l’ADN à sa fonction
Au cours de la dernière décennie, les chercheurs ont dressé d’immenses cartes d’éléments régulateurs « candidats », connus sous le nom d’éléments cis-régulateurs. Ils utilisent des méthodes qui montrent où l’ADN est faiblement empaqueté (chromatine ouverte), quelles protéines y sont liées et quelles marques d’histones décorent l’ADN environnant. Ces cartes sont impressionnantes, mais essentiellement descriptives : le fait qu’une protéine se lie ou qu’une marque apparaisse ne prouve pas qu’une séquence contrôle réellement l’activité d’un gène. Les essais rapporteurs massivement parallèles traditionnels (MPRAs) peuvent tester si des milliers de fragments d’ADN stimulent ou répriment un gène rapporteur, mais ils ne disent pas quelles protéines s’y lient ni quels changements épigénétiques accompagnent cette activité.
Un test deux-en-un pour l’activité et les marques épigénétiques
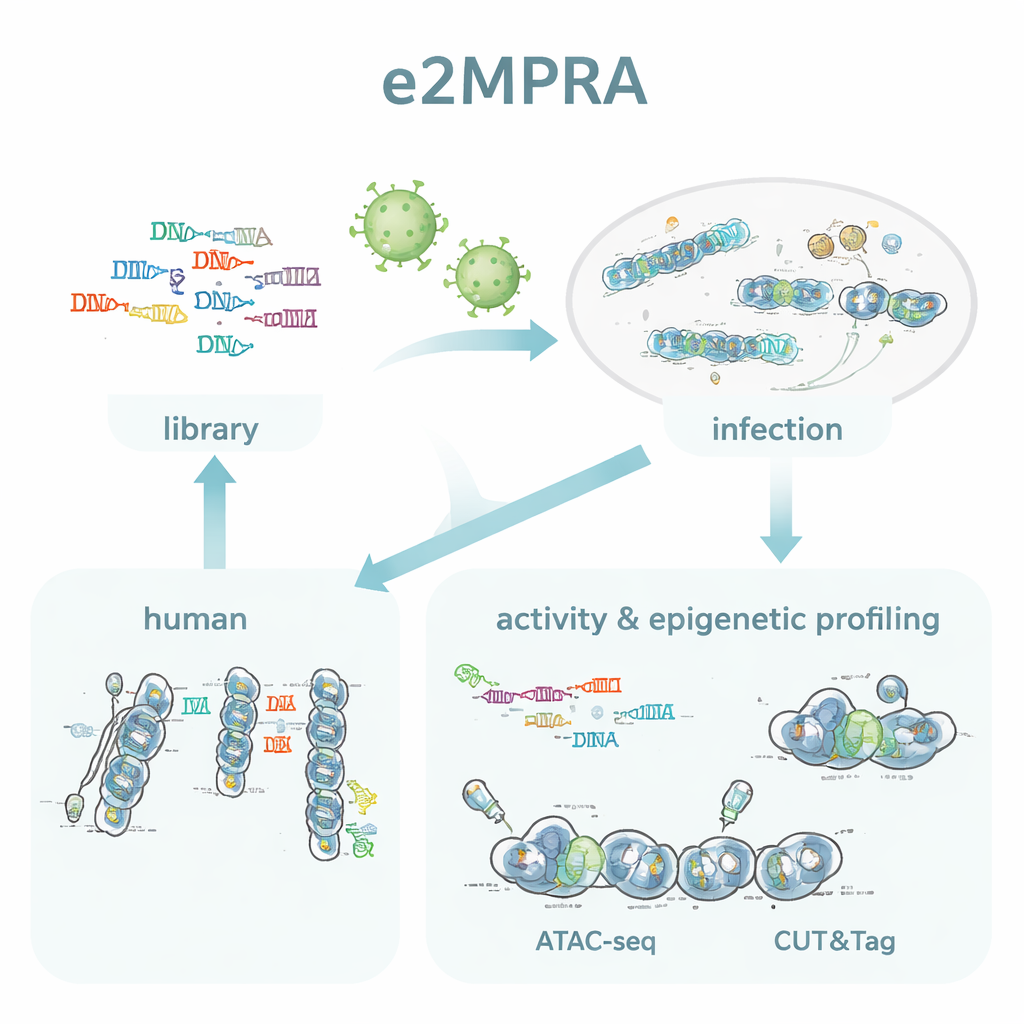
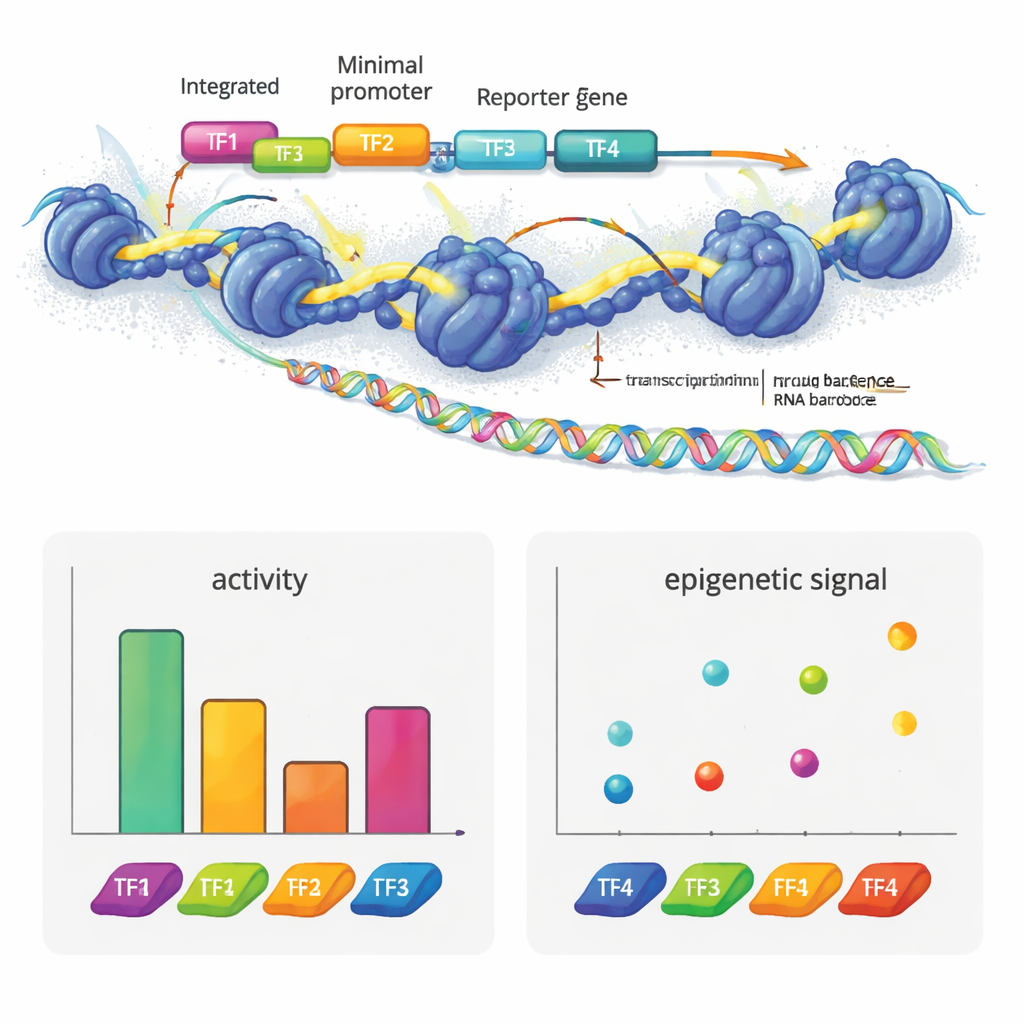
Les auteurs ont créé e2MPRA en combinant un MPRA lentiviral avec deux techniques épigénomiques, ATAC-seq et CUT&Tag. D’abord, ils construisent une bibliothèque d’ADN dans laquelle chaque séquence régulatrice candidate est liée à un court code-barres et placée à côté d’un promoteur minimal et d’un gène rapporteur. Cette bibliothèque est ensuite conditionnée en lentivirus et intégrée à de multiples exemplaires dans les génomes de cellules humaines en culture. À partir du même pool de cellules, ils lisent les codes-barres dans l’ARN pour mesurer l’activité régulatrice, et ils utilisent ATAC-seq et CUT&Tag pour mesurer l’ouverture de la chromatine et une marque d’histone clé (H3K27ac) spécifiquement au niveau des séquences insérées. En normalisant ces signaux par la fréquence d’intégration réelle de chaque séquence, ils obtiennent des mesures côte à côte de la « force on/off » et de l’état épigénétique pour des milliers d’éléments dans une seule expérience.
Décoder la coopération des motifs de facteurs de transcription
Pour montrer ce que cette technologie peut révéler, l’équipe a construit des enhancers synthétiques à partir de motifs de facteurs de transcription connus utilisés dans les cellules hépatiques. Ils ont disposé ces motifs en différents nombres et ordres sur des matrices d’ADN neutres. Certains facteurs, comme HNF1A et XBP1, se comportaient en activateurs classiques : ajouter plus de copies augmentait le signal rapporteur. D’autres, comme HNF1A et ONECUT1, stimulaient principalement l’accessibilité de la chromatine, correspondant à leur rôle de facteurs « pionniers » qui ouvrent l’ADN fermé. PPARA présentait un profil différent, modifiant fortement la chromatine et les marques d’histone sans activer la transcription par lui-même, mais coopérant avec d’autres facteurs pour augmenter l’activité génique. REST, un répresseur connu, atténuait l’activité lorsqu’il était placé à côté d’activateurs. Fait frappant, le simple réarrangement de quatre motifs pouvait modifier substantiellement la puissance d’un enhancer, et les activateurs avaient tendance à mieux fonctionner lorsqu’ils étaient plus proches du promoteur, révélant une sorte de grammaire dans l’agencement de ces motifs.
Localiser les bases sensibles dans les enhancers de pluripotence
Les chercheurs se sont ensuite tournés vers des enhancers importants pour l’identité des cellules souches, en se concentrant sur des régions liées aux facteurs de pluripotence POU5F1 (aussi appelé OCT4) et SOX2. Ils ont créé des bibliothèques de mutations denses dans lesquelles chaque base d’enhancers de 100 paires de bases était systématiquement modifiée, ainsi que de petites fenêtres de six bases brouillées aléatoirement. En utilisant e2MPRA dans des cellules souches pluripotentes induites, ils ont pu voir quelles mutations affaiblissaient ou renforçaient l’activité rapporteur et comment elles affectaient l’ouverture de la chromatine et l’acétylation. La perturbation du motif de liaison POU5F1::SOX2 réduisait souvent à la fois l’activité génique et les marques épigénétiques, confirmant son rôle central. Dans un enhancer bien étudié proche du gène POU5F1, ils ont aussi trouvé que la modification d’un motif YY1 augmentait la transcription mais réduisait l’ouverture de la chromatine, suggérant que certains facteurs peuvent favoriser un état ouvert tout en restreignant néanmoins l’expression.
Ce que cela signifie pour les gènes et la maladie
e2MPRA ne reproduit pas parfaitement toutes les nuances de l’architecture 3D naturelle du génome, mais il offre une manière pratique de comparer des milliers de séquences régulatrices et de variantes dans des conditions identiques. En couplant une lecture fonctionnelle (à quel point un segment d’ADN active un gène) avec des lectures épigénétiques (comment cet ADN est emballé et marqué), cette méthode aide à expliquer pourquoi certains motifs de facteurs de transcription, combinaisons et positions sont si cruciaux. À long terme, des outils comme e2MPRA peuvent faciliter l’interprétation des variantes génétiques non codantes liées aux maladies, la conception d’enhancers synthétiques pour la thérapie génique et la construction d’un « code régulateur » plus complet reliant la séquence d’ADN au comportement cellulaire.
Citation: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Mots-clés: régulation génique, enhancers, épigénétique, facteurs de transcription, génomique fonctionnelle