Clear Sky Science · fr
Les ligases ubiquitine E3 gardiennes ciblent les désaminases APOBEC3 associées au cancer pour les dégrader afin de préserver l’intégrité du génome humain
Protéger notre ADN du feu ami
Nos cellules mobilisent des enzymes puissantes pour endommager l’ADN viral, ce qui nous aide à repousser les infections. Mais certaines de ces mêmes enzymes, si elles ne sont pas contrôlées, peuvent par erreur marquer notre propre génome et contribuer au cancer. Cette étude révèle comment les cellules humaines surveillent ces enzymes risquées, mettant au jour un système de « contrôle qualité » intégré qui étiquette les variantes dangereuses pour les détruire avant qu’elles ne puissent réécrire notre ADN.
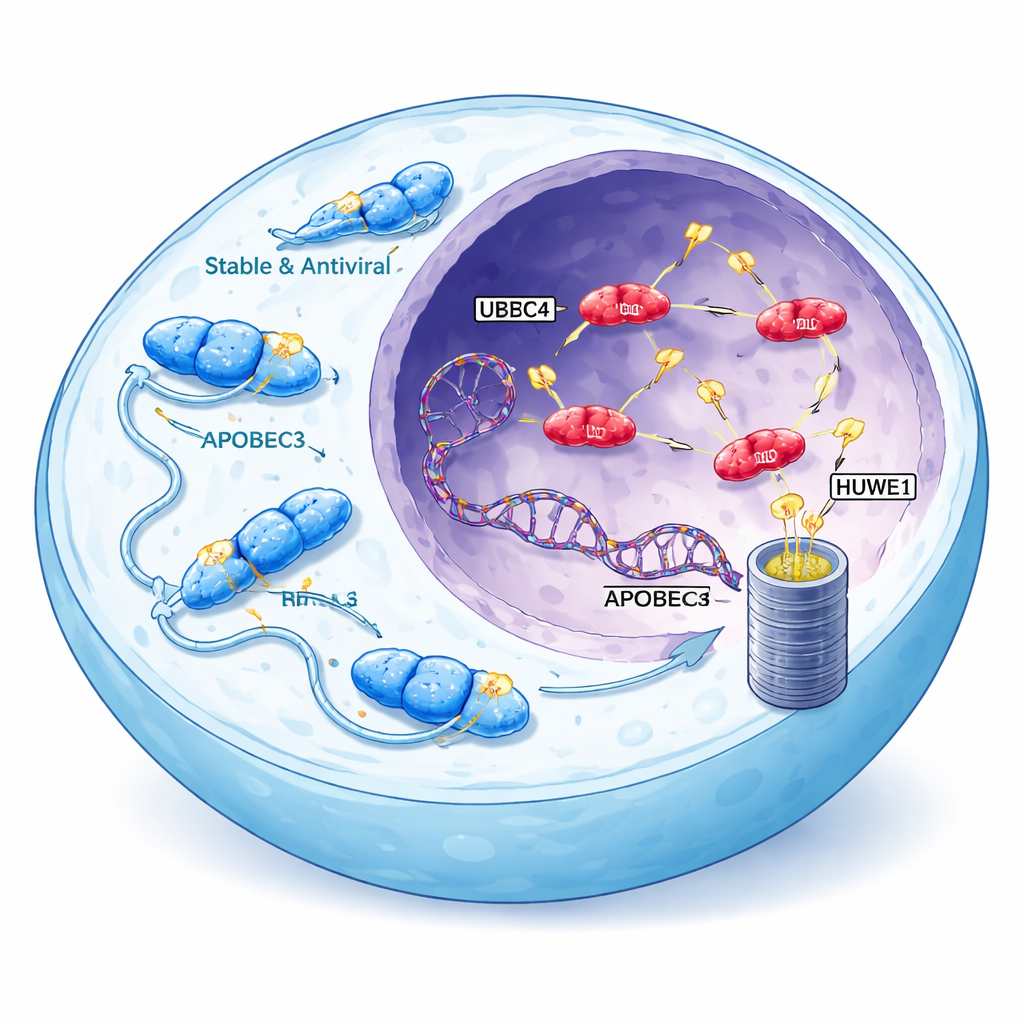
Des combattants viraux qui peuvent se retourner contre nous
La famille d’enzymes APOBEC3 aide normalement à lutter contre des virus comme le VIH en modifiant chimiquement l’ADN viral, provoquant des erreurs fatales. L’humain possède sept variantes d’APOBEC3, et trois d’entre elles — A3A, A3B et une forme d’A3H appelée haplotype I (A3H-I) — sont fortement associées aux profils de mutations observés dans de nombreux cancers. Ces enzymes particulières peuvent pénétrer dans le noyau cellulaire, où se trouvent nos chromosomes, et introduire des grappes caractéristiques de mutations dans le génome. Ces signatures liées aux APOBEC apparaissent dans plus de la moitié des cancers humains, en particulier dans les tumeurs du sein, du poumon et de la vessie, où elles augmentent le réservoir de changements génétiques dont les tumeurs peuvent tirer parti pour s’adapter et résister aux traitements.
Pourquoi les formes les plus dangereuses sont étonnamment instables
De manière curieuse, les enzymes APOBEC3 les plus fortement liées au cancer sont aussi les moins stables. Contrairement à leurs homologues cytoplasmiques, qui s’accumulent à des niveaux élevés et bloquent efficacement les virus, A3A, A3B et A3H-I sont rapidement dégradées et généralement présentes à de faibles concentrations dans le noyau. Les chercheurs ont émis l’hypothèse que cette instabilité pourrait être délibérée : si les cellules limitent activement les niveaux de protéines APOBEC3 nucléaires, toute défaillance de ce contrôle pourrait déclencher des poussées de mutagenèse. En prenant A3H-I comme modèle, ils ont montré que les APOBEC3 associées au cancer sont principalement détruites par le protéasome, le broyeur protéique de la cellule, après avoir été marquées par de petits « drapeaux » moléculaires appelés ubiquitine sur plusieurs sites d’acides aminés.
Identifier les gardiens cellulaires
Pour localiser la machinerie responsable d’étiqueter A3H-I et A3B, l’équipe a combiné un criblage CRISPR avec une cartographie de proximité protéique. Ils ont conçu des cellules qui brillent différemment selon la stabilité d’A3H-I et de sa variante inoffensive A3H-II, puis ont systématiquement perturbé des gènes impliqués dans la dégradation des protéines. Trois ligases ubiquitine — UBR4, UBR5 et HUWE1 — se sont distinguées. L’inactivation de chacune de ces ligases augmentait sélectivement les niveaux d’A3H-I nucléaire instable sans affecter l’A3H-II cytoplasmique stable. Ces mêmes ligases ont indépendamment augmenté les niveaux d’A3B endogène dans des lignées cellulaires coliques et immunitaires, et la suppression simultanée des trois a produit une hausse additive de l’abondance d’A3B. Des expériences biochimiques ont en outre montré que UBR5 et HUWE1 se lient physiquement à A3B et A3H-I et attachent directement des chaînes d’ubiquitine, tandis qu’UBR4 semble se spécialiser dans l’allongement de ces chaînes pour rendre les protéines plus efficacement éliminables.
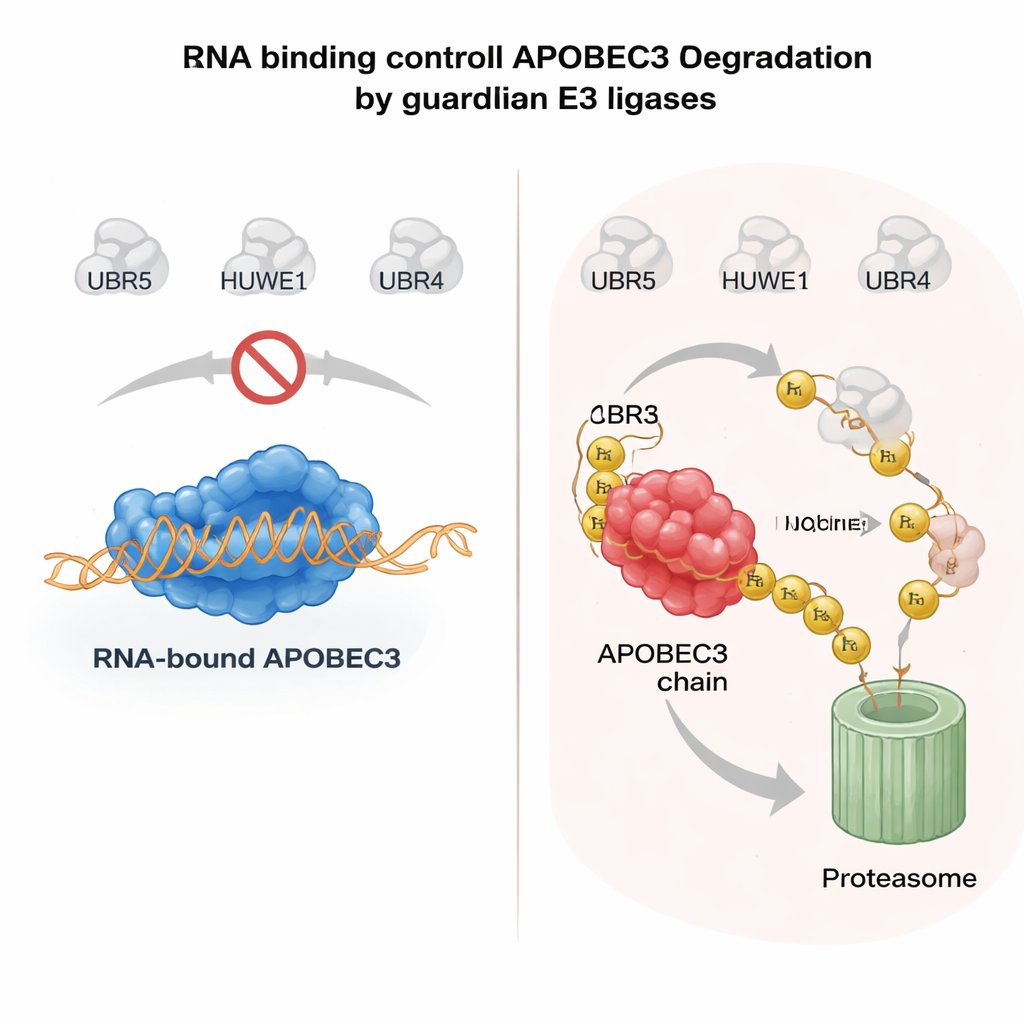
L’ARN comme ceinture de sécurité pour des enzymes risquées
Qu’est-ce qui détermine si une enzyme APOBEC3 est épargnée ou détruite ? Un indice clé vient de la façon dont les protéines APOBEC3 se lient aux molécules d’ARN dans le cytoplasme. Lorsqu’A3H ou un autre membre de la famille, A3G, se lie à l’ARN, il a tendance à rester dans de grands complexes dans le cytosol et est relativement stable. Des mutations qui affaiblissent la liaison à l’ARN font que ces enzymes dérivent vers le noyau, perdent leurs partenaires protecteurs et deviennent très instables. Les auteurs ont montré que lorsque les protéines APOBEC3 ne sont pas liées à l’ARN, UBR5 et HUWE1 reconnaissent des surfaces exposées de l’enzyme, les décorent d’ubiquitine et les dirigent vers la dégradation nucléaire. Dans des systèmes purifiés, l’ajout d’ARNase pour éliminer l’ARN a fortement augmenté la capacité de ces ligases à se lier et à ubiquitiner les APOBEC3, confirmant que la liaison à l’ARN agit comme un bouclier moléculaire. Ce mécanisme permet aux cellules de maintenir actives les APOBEC3 antivirales dans le cytoplasme tout en éliminant rapidement la fraction non liée et menaçante pour le génome qui se trouve dans le noyau.
Quand les gardiens échouent : liens avec les mutations cancéreuses
Si UBR4, UBR5 et HUWE1 font office de gardiens, leur perte devrait augmenter le niveau de mutations. Les chercheurs ont testé cela en désactivant chaque ligase dans des cellules de cancer du côlon et en suivant les changements d’ADN au fil du temps à l’aide d’une méthode de séquençage sensible qui lit les « signatures » mutationnelles. La suppression de ces ligases, en particulier dans des cellules exprimant A3H-I, a amplifié les profils de mutations spécifiques aux APOBEC — exactement le type retrouvé dans les tumeurs humaines. En élargissant l’analyse aux données de patients, ils ont examiné des milliers de génomes cancéreux et constaté que les tumeurs porteuses de mutations dans UBR5 ou HUWE1 présentaient une fraction significativement plus élevée de signatures de mutation liées aux APOBEC que les tumeurs avec des ligases intactes, même après prise en compte de la charge mutationnelle globale. Cela suggère que des ligases gardiennes défectueuses chez les patients peuvent permettre aux APOBEC3 associées au cancer de se déchaîner et de remodeler le génome tumoral.
Ce que cela signifie pour la prise en charge future du cancer
Pour un non-spécialiste, la conclusion est que nos cellules disposent d’un système de surveillance sophistiqué pour empêcher que des enzymes antivirales utiles ne sabotent par erreur notre propre ADN. UBR4, UBR5 et HUWE1 agissent comme des gardiens qui détectent lorsque les enzymes APOBEC3 ne sont plus fixées en toute sécurité à l’ARN et, surtout dans le noyau, les envoient vers le broyeur cellulaire. Lorsque ce système de contrôle est affaibli — par des mutations des ligases ou par des médicaments qui bloquent la dégradation des protéines — l’activité des APOBEC3 peut alimenter le chaos génétique qui propulse l’évolution tumorale et la résistance aux traitements. Comprendre ce réseau de gardiens ouvre la voie à de nouveaux marqueurs diagnostiques, tels que des mutations des ligases ou les niveaux de protéines APOBEC, et suggère qu’une modulation prudente de cette voie pourrait un jour aider à limiter les poussées de mutations nocives dans les tumeurs sans compromettre nos défenses antivirales.
Citation: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Mots-clés: APOBEC3, stabilité du génome, ligase ubiquitine, mutagenèse cancéreuse, dégradation des protéines