Clear Sky Science · fr
La mise en espace de la contractilité par un gradient d’activité mécanogène auto-organisé sous-tend la gastrulation de Drosophila
Comment les tissus se sculptent
Les embryons précoces transforment, d’une manière ou d’une autre, de simples feuillets cellulaires en formes tridimensionnelles complexes. Cette étude pose une question fondamentale derrière ce tour de magie : comment les cellules coordonnent-elles où se contracter et se plier pour qu’un tissu se replie au bon emplacement et dans la bonne direction ? En observant des embryons de mouche à haute résolution, les auteurs identifient un signal chimique qui agit comme un « morphogène mécanique », modulant directement où les cellules se contractent pour provoquer un événement de pliage crucial du développement.
Une onde qui replie l’embryon
Chez la mouche du vinaigre Drosophila, une étape clé du développement précoce est la gastrulation, quand une couche plane de cellules se courbe vers l’intérieur pour commencer à former l’intestin. À l’arrière de l’embryon, une zone de cellules appelée primordium de l’endoderme postérieur initie ce processus en se contractant sur leur face apicale. Ce pli initial lance une onde voyageuse d’invagination tissulaire qui balaie les cellules voisines. Les auteurs montrent que cette onde dépend d’un signal nommé Fog, une molécule sécrétée qui active une famille de récepteurs connus sous le nom de GPCRs, lesquels déclenchent à leur tour la machinerie contractile de la cellule composée de la protéine motrice Myosin‑II.
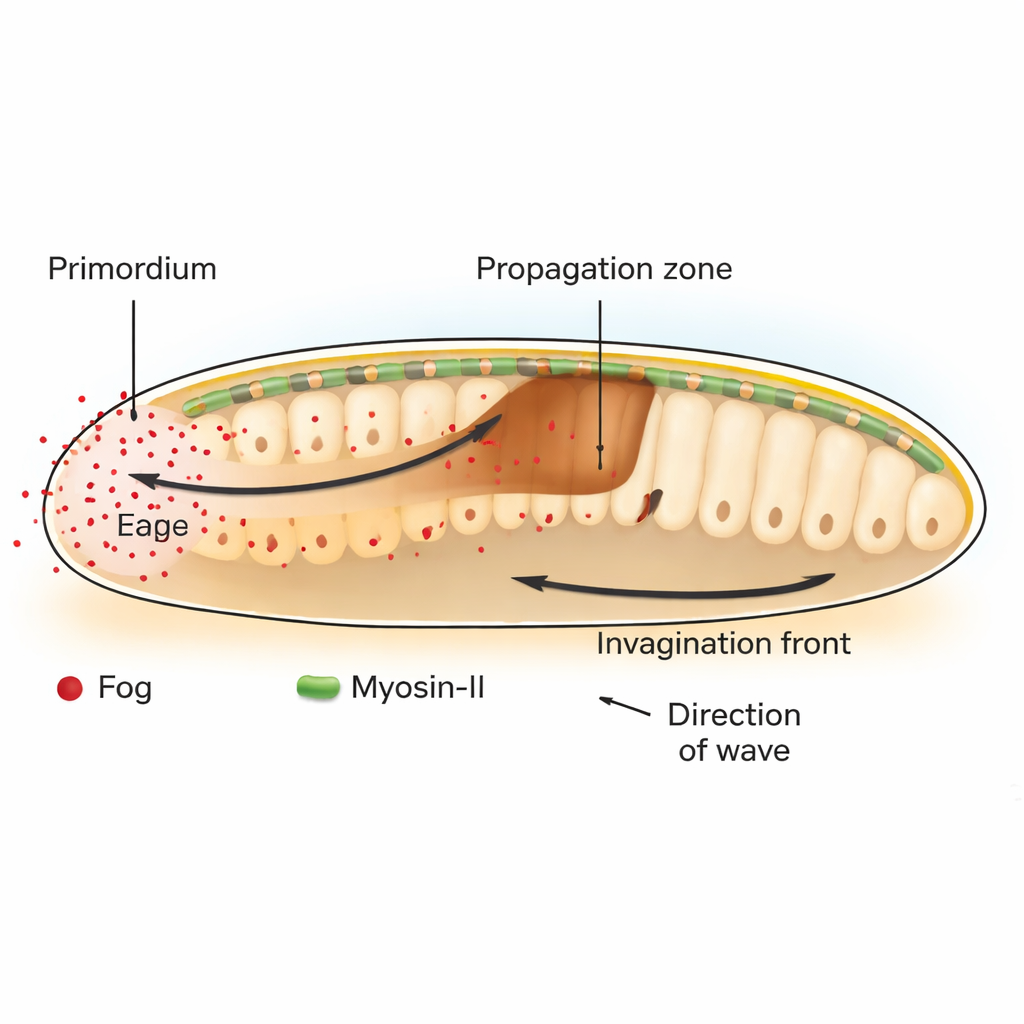
Un chimique qui distribue la force, pas le destin
Classiquement, les biologistes du développement se sont concentrés sur les « morphogènes », des molécules diffusantes dont le gradient de concentration informe les cellules de l’identité qu’elles doivent adopter. Ici, Fog se comporte différemment. Plutôt que de modifier le type de cellule qu’une région deviendra, Fog règle directement l’intensité des contractions cellulaires. En restaurant ou en bloquant sélectivement Fog et son messager en aval Gα seulement dans certaines régions, les chercheurs montrent que Fog produit dans le primordium est à la fois nécessaire et suffisant pour déclencher l’activation de la Myosin‑II et le pliage tissulaire à distance dans la zone de propagation adjacente. Lorsqu’on ancre Fog pour qu’il ne puisse pas se diffuser, seules les cellules productrices se contractent et l’onde d’invagination s’arrête après une ou deux rangées cellulaires.
Un gradient caché à la surface cellulaire
Une idée naturelle est que Fog pourrait former un gradient de concentration classique à l’extérieur des cellules. En utilisant une version fluorescentement marquée de Fog et des mesures de fluorescence sensibles, l’équipe trouve le contraire : dans la fine couche fluide entre le tissu et son enveloppe (la membrane vitelline), Fog est remarquablement uniforme. Pourtant, l’activité de la Myosin‑II forme clairement un gradient voyageur abrupt, le plus fort juste devant le pli progressif et s’estompant à quelques diamètres cellulaires. L’élément manquant est que Fog n’agit pas comme un simple indice de concentration en vrac ; au lieu de cela, une petite fraction de Fog devient momentanément piégée à la surface cellulaire, se liant à ses récepteurs GPCR et formant un gradient d’activité lié à la surface même si les molécules libres de Fog restent uniformément mélangées dans le fluide.
Récepteurs, endocytose et adhérence façonnent l’onde
Les auteurs montrent que ce Fog lié à la surface, avec ses récepteurs, s’auto‑organise en motif. Là où Fog rencontre à plusieurs reprises des récepteurs, il favorise le regroupement et l’activation des récepteurs, ce qui recrute davantage de Myosin‑II. Un processus cellulaire de « nettoyage » — l’endocytose des GPCR — élimine ensuite les complexes actifs, empêchant une activation incontrôlée et aidant à régler la distance de propagation du signal. Lorsque cette endocytose est ralentie génétiquement, le gradient de Myosin‑II devient plus haut et plus large. Un second acteur clé est un ensemble de molécules d’adhérence appelées intégrines. À mesure que le tissu se plie, les cellules en avant du pli pressent contre la membrane vitelline ; ce contact active localement les intégrines, qui à leur tour renforcent l’efficacité de la signalisation Fog–GPCR. La zone d’engagement fort des intégrines correspond à l’étendue du gradient de Myosin‑II, et sans intégrines l’onde devient faible et de courte portée même si la signalisation Fog est par ailleurs renforcée.
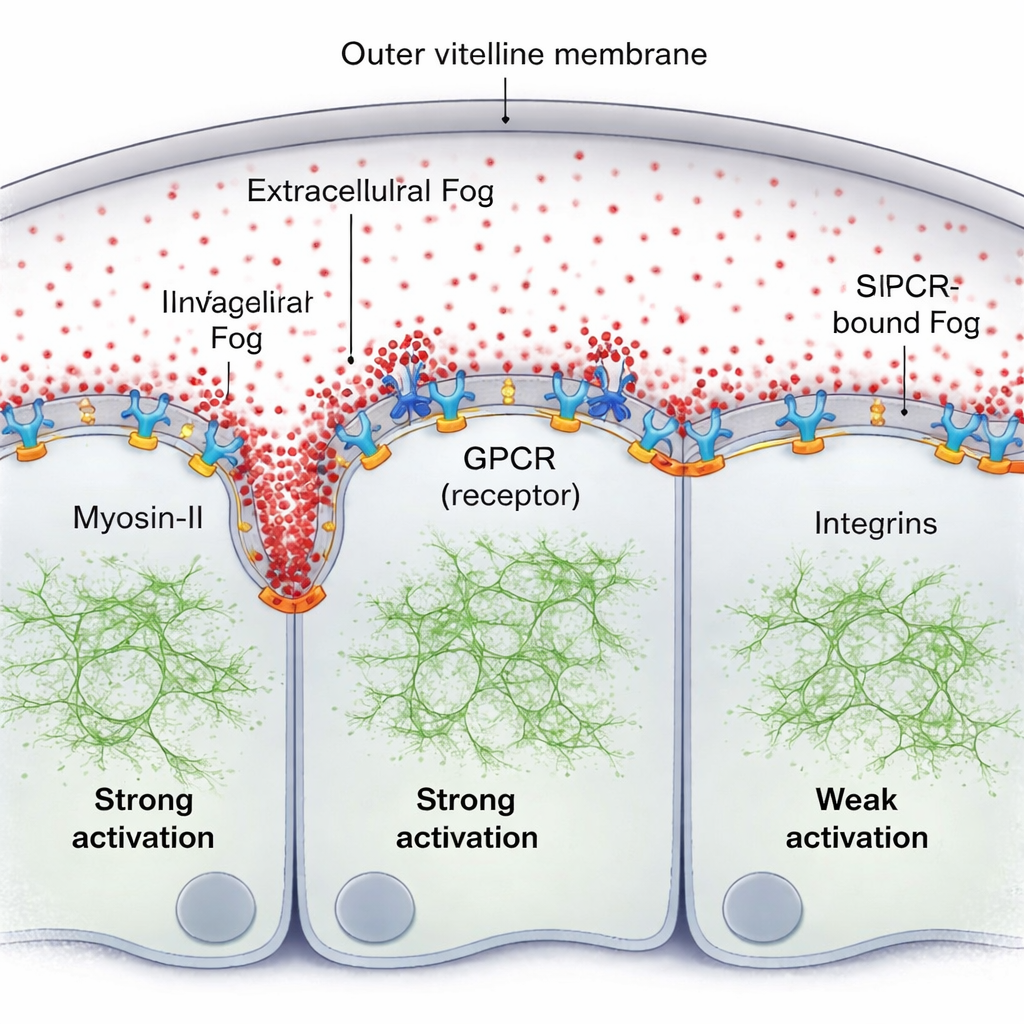
Un motif mécanique auto-renouvelé
Pour un non‑spécialiste, le message principal est que l’embryon ne s’appuie pas uniquement sur des cartes chimiques préétablies pour décider où se plier. Il construit plutôt un motif mobile d’activité mécanique à la volée. Fog se répand de manière uniforme, mais son action effective est sculptée à la surface cellulaire par le regroupement des récepteurs, l’élimination des récepteurs et la géométrie tissulaire changeante lorsque les cellules appuient contre leur environnement. Cela crée un gradient voyageur auto‑organisé de force contractile qui tire le tissu vers l’intérieur dans une onde coordonnée. Ce travail offre un exemple concret d’un « mécanogène » théorisé de longue date : une molécule diffusante qui module directement les forces physiques dans un tissu, aidant à expliquer comment les organismes vivants se sculptent de façon si fiable pendant le développement.
Citation: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Mots-clés: gastrulation, mécanogène, embryon de Drosophila, mécanique tissulaire, signalisation Fog