Clear Sky Science · fr
La configuration des extrémités d’ADN dicte la formation du complexe synaptique lors du rapprochement des extrémités par NHEJ
Quand l’ADN se casse, la cellule doit réagir vite
Chaque jour, l’ADN de nos cellules est éraflé, sectionné et sollicité par le métabolisme normal et des stress environnementaux. Parmi les blessures les plus dangereuses figurent les cassures double-brin, où les deux brins de l’hélice d’ADN se rompent. Si ces cassures ne sont pas réparées rapidement et avec précision, les cellules peuvent mourir ou, pire, évoluer vers un état cancéreux. Cette étude examine comment la forme exacte et la chimie des extrémités d’ADN rompues déterminent si une voie de réparation clé, appelée jonction non-homologue (NHEJ), réunit ces extrémités efficacement et avec un minimum d’erreurs.
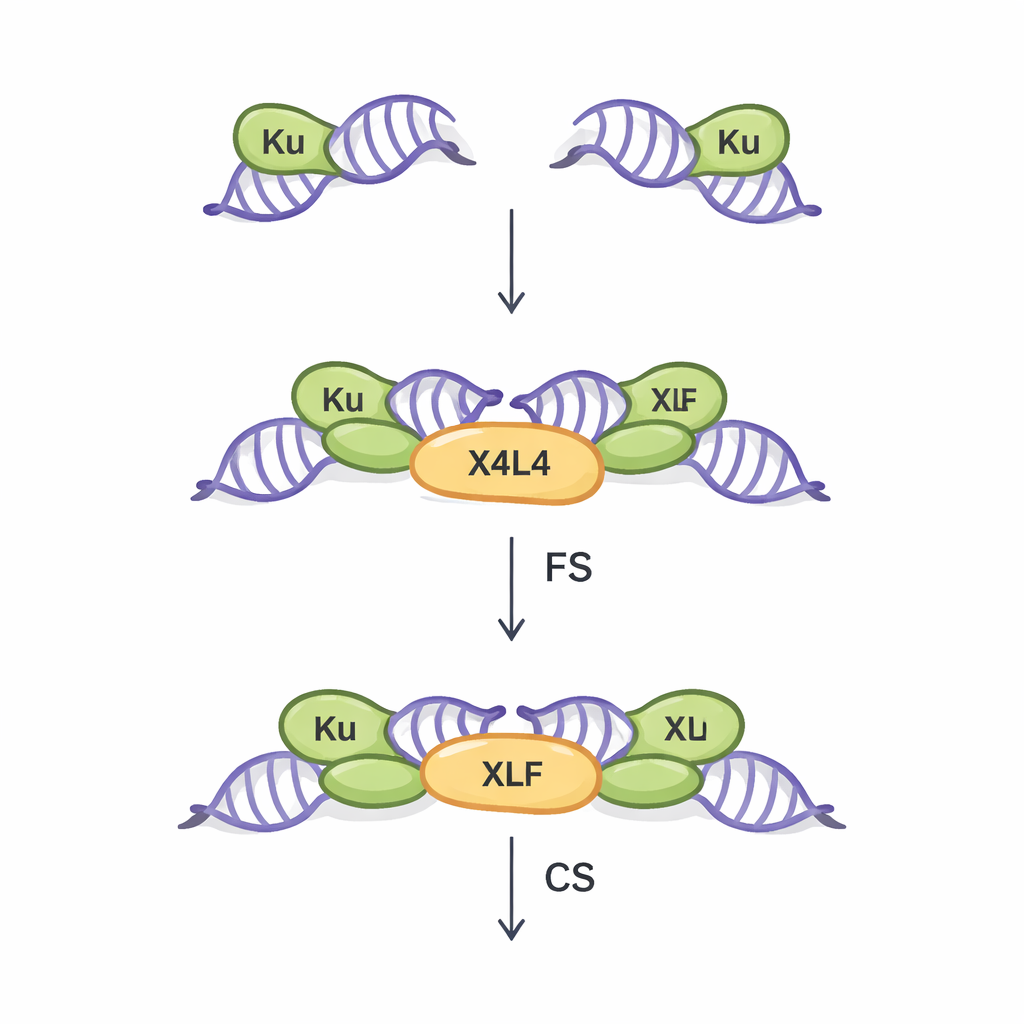
Deux manières de rapprocher des bris d’ADN
La NHEJ est la principale voie de réparation des cassures double-brin dans la plupart des cellules de notre organisme. Elle fonctionne sans avoir besoin d’un modèle d’ADN apparié, ce qui la rend rapide mais un peu sujette aux erreurs. La première étape cruciale de cette voie s’appelle la synapsis : le rapprochement physique des deux extrémités d’ADN rompues afin qu’elles puissent ensuite être reliées. Des travaux antérieurs, principalement réalisés avec des extrémités d’ADN idéales et franches, ont révélé deux types d’assemblages synaptiques. Dans l’état « synapse flexible » (FS), les extrémités sont maintenues à proximité et peuvent bouger, explorant des possibilités d’appariement. Dans l’état « synapse rapprochée » (CS), les extrémités s’alignent bout à bout et sont prêtes à être scellées par une ligase. Trois protéines centrales — Ku, XRCC4–Ligase IV (appelées ensemble X4L4) et XLF — coordonnent ce processus, mais on ne comprenait pas bien comment des extrémités d’ADN irrégulières rencontrées en conditions réelles influencent l’état synaptique qui se forme.
La forme des extrémités et de courts appariements orientent la voie de réparation
Les chercheurs ont utilisé le FRET mono-moléculaire, une technique de fluorescence qui suit des distances à l’échelle du nanomètre, pour observer des molécules d’ADN individuelles au fur et à mesure qu’elles étaient rapprochées par les protéines de la NHEJ. Ils ont comparé des extrémités franches simples à des extrémités plus réalistes portant de courts surplombs — de petites queues simple brin susceptibles de s’apparier entre elles. Ils ont constaté que lorsque les surplombs sont complémentaires, même sur seulement quelques bases, la probabilité de former un complexe synaptique rapproché augmente fortement. En fait, trois bases appariées de « microhomologie » au niveau de la cassure suffisaient pour que Ku et X4L4 seuls créent un complexe CS stable, sans nécessiter XLF. Cela montre que l’ADN lui-même peut fournir une partie de l’énergie et de l’orientation normalement apportées par des protéines auxiliaires.
Comment de petites languettes d’ADN stabilisent le pont
En analysant des signatures FRET distinctes, l’équipe a mis au jour au moins deux configurations structurelles de l’état synaptique rapproché pour des extrémités à surplomb. Dans l’une, les tout-petits embouts des surplombs s’apparentent entre eux, formant une jointure nickée ou avec des lacunes. Dans l’autre, les jonctions où l’ADN double brin rencontre les surplombs simple brin se pressent en ligne, tandis que les surplombs se rabattent vers l’extérieur comme de petites languettes. Ces languettes permettent toujours l’appariement des bases et maintiennent les extrémités en très proche proximité, ce qui stabilise probablement le complexe et laisse la place aux enzymes pour élaguer ou allonger l’ADN au besoin avant le scellage final. Fait intéressant, des dommages oxydatifs courants dans les surplombs, tels que la 8-oxoguanine, n’affectent que modestement ce processus, soulignant la robustesse de la NHEJ face à certaines formes de lésion.
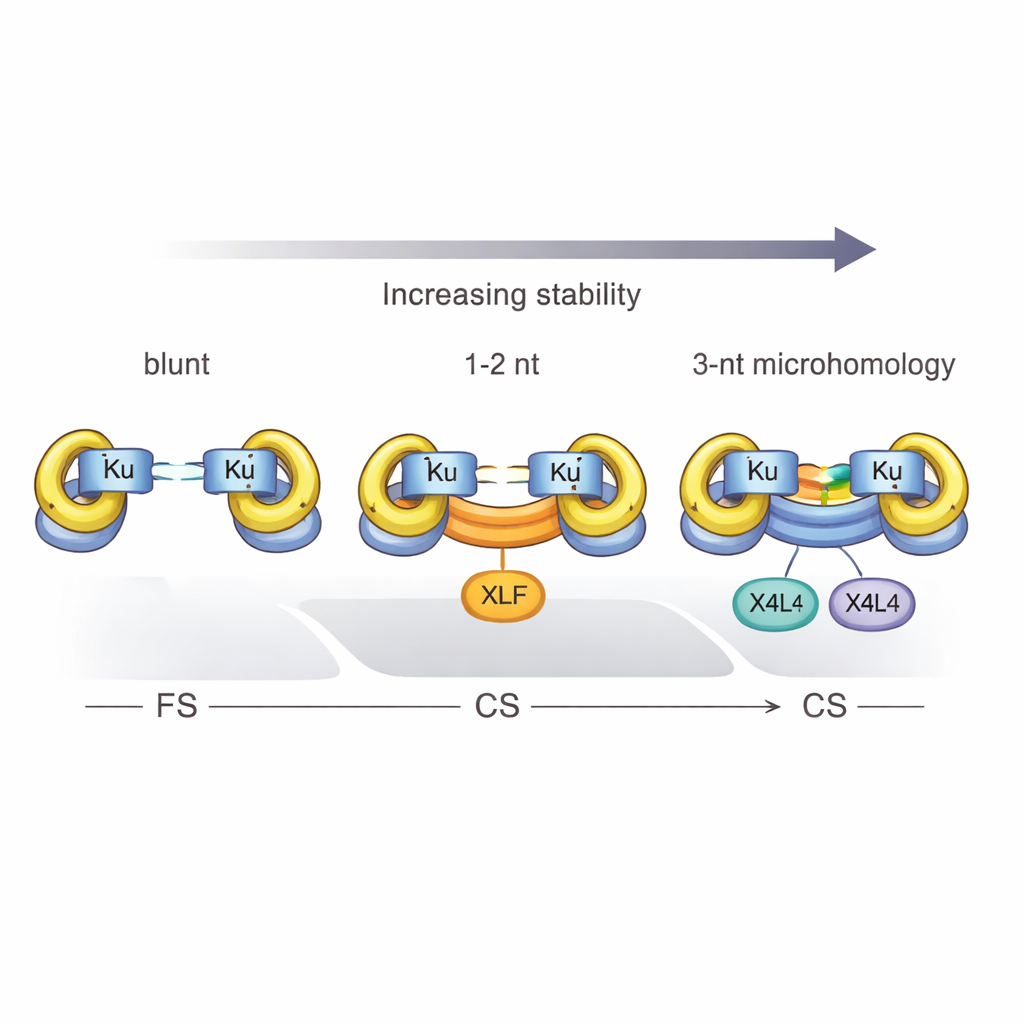
Protéines, phosphates et le pouvoir du trio
L’étude a également défini un seuil net : au moins trois paires de bases complémentaires sont requises pour que Ku et X4L4 convertissent de façon fiable un complexe flexible en un complexe rapproché. Avec seulement une ou deux correspondances, le système reste majoritairement bloqué dans l’état flexible, sauf si XLF intervient pour aider à serrer les extrémités. Les détails chimiques comptent aussi. Lorsque l’ADN rompu porte un groupement phosphate en 5′ — caractéristique normale de nombreuses cassures physiologiques — la synapsis devient plus efficace, et les complexes rapprochés sont plus susceptibles d’être véritablement ligaturés, transformant un pont temporaire en une réparation permanente. Cependant, ce renfort apporté par le phosphate ne remplace pas totalement l’effet stabilisant de l’appariement des bases au niveau de la cassure.
Pourquoi cela compte pour la santé et l’édition du génome
En termes simples, ce travail montre que les extrémités d’ADN rompues ne sont pas des victimes passives attendant d’être réparées. Leurs formes exactes, de petites zones de séquence appariée et des étiquettes chimiques guident activement la manière dont les protéines de réparation saisissent, alignent et reconnectent ces extrémités. Quand trois bases ou plus sont appariées, les extrémités d’ADN aident elles-mêmes à verrouiller la cassure dans une configuration prête à être réparée, rendant parfois certaines protéines auxiliaires optionnelles. Quand ces appariements sont rares, des facteurs protéiques supplémentaires deviennent essentiels. Ces connaissances aident à expliquer pourquoi certaines cassures sont réparées proprement tandis que d’autres entraînent de petites mutations ou des réarrangements. Elles offrent aussi des pistes pour améliorer des outils d’édition du génome comme CRISPR, où des cassures d’ADN intentionnelles sont réparées par la même machinerie NHEJ. En ajustant les extrémités de ces cassures, les scientifiques pourraient mieux contrôler la manière dont le génome est remodelé.
Citation: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Mots-clés: réparation des cassures double-brin de l’ADN, jonction non-homologue, synapsis de l’ADN, microhomologie, stabilité du génome