Clear Sky Science · fr
Un basculement d’une valine en leucine empêche la liaison d’AP2-G de Plasmodium falciparum à l’ADN et révèle le rôle de GDV1 dans l’activation d’ap2-g
Comment les parasites du paludisme prennent une décision cruciale de vie ou de mort
Les parasites du paludisme présents dans notre sang font constamment face à un choix déterminant : continuer à se multiplier chez un hôte unique ou se transformer en une forme capable de passer au prochain hôte via la piqûre d’un moustique. Cette étude révèle comment un tout petit changement dans une protéine parasitaire peut bloquer totalement cette phase infectieuse prête pour le moustique, offrant de nouvelles pistes pour interrompre la transmission du paludisme.
La bifurcation du parasite
Dans le plasma sanguin, Plasmodium falciparum privilégie majoritairement une croissance rapide, responsable de la maladie. Mais une petite minorité se transforme en formes sexuelles appelées gamétocytes, les seules stades que les moustiques peuvent prélever et transmettre. Pourquoi seuls quelques parasites effectuent ce basculement reste une énigme de longue date. Des travaux antérieurs ont montré que deux protéines parasitaires, GDV1 et une protéine liant l’ADN appelée AP2-G, sont au cœur de cette décision. GDV1 aide à réveiller le gène ap2-g normalement silencieux, et AP2-G active à son tour un ensemble de gènes qui conduisent au développement sexuel. L’étude actuelle visait à explorer une autre protéine, une kinase nommée STK2, mais a mis au jour un résultat beaucoup plus spectaculaire concernant AP2-G lui‑même.
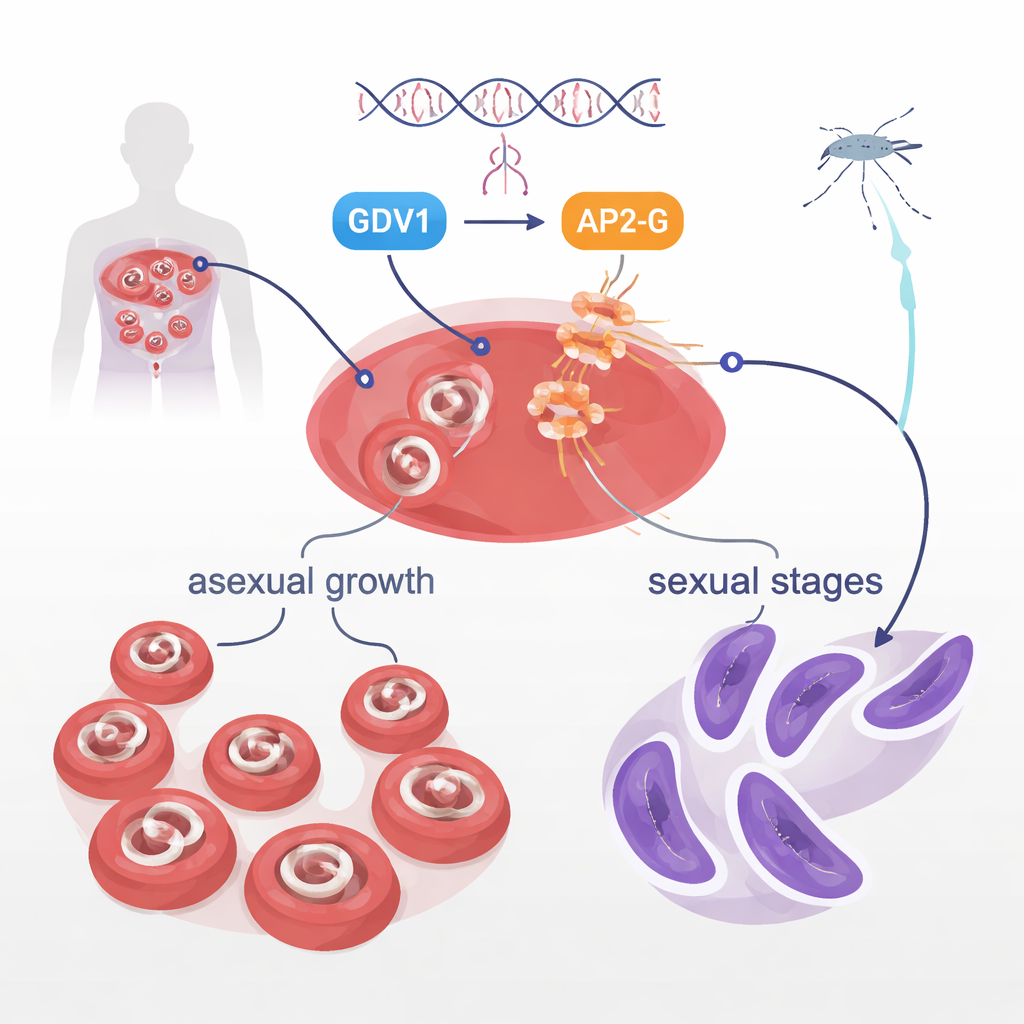
Un seul acide aminé qui bloque la transmission
En supprimant le gène stk2 dans une souche de laboratoire, les chercheurs ont observé que ces parasites perdaient complètement leur capacité à produire des gamétocytes, tout en conservant une croissance asexuée normale. De manière surprenante, des manipulations similaires dans une autre souche n’affectaient pas la formation des gamétocytes. Le séquençage complet du génome a révélé le coupable caché : une variation d’une seule « lettre » dans le gène ap2-g, substituant une valine par une leucine très semblable à la position 2163. Cette position se situe au tout début du domaine de liaison à l’ADN d’AP2-G, la portion qui saisit physiquement des motifs d’ADN spécifiques pour activer des gènes. Ce minuscule remplacement valine→leucine suffisait à abolir la formation des gamétocytes. Quand les scientifiques ont introduit cette mutation dans des parasites autrement normaux, les gamétocytes ont disparu ; en la ramenant à la valine, le développement sexuel a été entièrement restauré.
Comment le basculement casse la serrure moléculaire
Pour comprendre pourquoi ce changement subtil est si dévastateur, l’équipe a combiné modélisation informatique et expériences en laboratoire. Les prédictions de structure suggéraient que le remplacement de la valine par la leucine déplace et déstabilise la conformation précise du domaine de liaison à l’ADN d’AP2. Dans des essais in vitro avec des protéines purifiées, l’AP2-G normal se liait fortement à sa séquence d’ADN préférée, un court motif contenant « GnGTAC ». En revanche, l’AP2-G mutant portant la leucine en position 2163 ne se liait pas du tout à cette séquence. Sans liaison stable à l’ADN, AP2-G ne pouvait plus activer son propre gène (une boucle de rétroaction positive appelée autorégulation) ni déclencher des dizaines de gènes en aval nécessaires pour pousser les parasites vers la voie sexuelle. Fonctionnellement, les parasites mutants devenaient « stériles » : incapables de produire les formes infectant les moustiques, alors qu’ils prospéraient toujours dans les globules rouges.
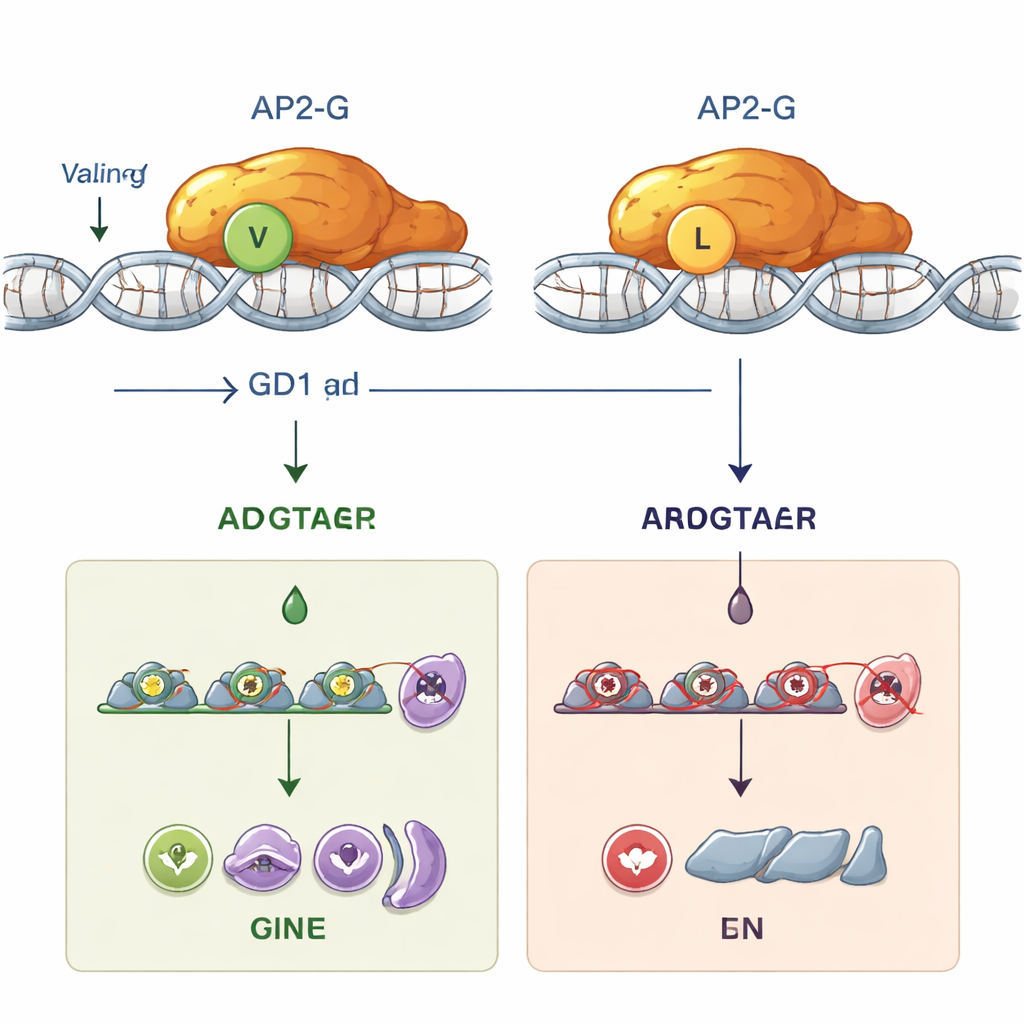
Le rôle discret de GDV1 avant que AP2-G n’entre en scène
La mutation a aussi fourni aux chercheurs un outil unique : des parasites dans lesquels le gène ap2-g peut être activé, mais où AP2-G ne peut pas se lier à l’ADN. Grâce à des marqueurs fluorescents et bioluminescents, ils ont suivi l’action des différents acteurs au cours du cycle parasitaire de 48 heures dans les globules rouges. Ils ont constaté que la protéine GDV1 apparaît en premier, tôt pendant une phase appelée schizogonie, et qu’elle est essentielle pour relancer l’expression d’ap2-g depuis son état silencieux. Cette activation précoce se produisait que ap2-g code une AP2-G normale ou la version mutante. Ce n’est que plus tard, lorsque suffisamment d’AP2-G fonctionnelle s’était accumulée, que la boucle d’auto‑amplification et l’activation des autres gènes « sexuels » surviennent. Un marqueur clé, une protéine appelée MSRP1, s’allumait seulement dans les parasites avec AP2-G fonctionnelle, fournissant un moyen pratique de distinguer les parasites engagés sexuellement tôt et tard. Dans les lignées mutantes portant la substitution leucine, GDV1 pouvait toujours réveiller ap2-g, mais l’AP2-G défaillante ne pouvait pas poursuivre le processus, si bien que le développement sexuel s’arrêtait.
Conséquences pour l’arrêt de la propagation du paludisme
Pour le lecteur général, la conclusion est simple : les parasites du paludisme dépendent d’une serrure moléculaire extrêmement sensible pour décider s’ils deviendront transmissibles. Cette étude montre que changer un seul « dent » de cette serrure — une unique valine dans la région de liaison à l’ADN d’AP2-G — empêche le parasite de produire les stades infectieux pour les moustiques. Parallèlement, elle clarifie qu’une autre protéine, GDV1, intervient plus tôt comme la clé qui déverrouille d’abord le gène ap2-g silencieux, avant qu’AP2-G n’amplifie sa propre production et n’enclenche un programme sexuel plus large. En cartographiant cette séquence d’événements et en créant des lignées rapporteurs de parasites qui s’illuminent à chaque étape, le travail fournit des outils puissants pour criblage de médicaments ou d’éléments humains qui perturbent l’engagement sexuel. À long terme, cibler la région de liaison à l’ADN d’AP2-G ou l’étape d’activation pilotée par GDV1 pourrait fonder de nouvelles stratégies qui ne se contentent pas de guérir un patient, mais coupent complètement la chaîne de transmission.
Citation: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Mots-clés: transmission du paludisme, Plasmodium falciparum, développement des gamétocytes, AP2-G, GDV1