Clear Sky Science · fr
Des mécanismes hiérarchiques contrôlent l’élimination de l’ARN polymérase II bloquée par des lésions de l’ADN
Quand les machines de copie des gènes rencontrent un obstacle
Chaque seconde, des millions de petites machines moléculaires appelées ARN polymérase II parcourent notre ADN pour recopier les gènes en ARN. Mais quand l’ADN est endommagé — par exemple par les ultraviolets (UV) du soleil — ces machines peuvent s’immobiliser. Si des polymérases bloquées s’accumulent, les cellules ne peuvent plus lire correctement leurs gènes, ce qui est particulièrement dangereux pour les cellules cérébrales et peut mener à des maladies rares comme le syndrome de Cockayne. Cette étude détaille comment nos cellules détectent ces machines bloquées et les redémarrent ou les éliminent avant qu’elles n’entraînent des dommages durables.
Une nouvelle façon d’observer les embouteillages cellulaires
Pour comprendre comment les cellules dégagent les polymérases bloquées, les chercheurs ont construit une « caméra de circulation » temporelle pour la transcription. Ils ont utilisé un médicament qui permet aux molécules d’ARN polymérase II déjà engagées de continuer leur trajet mais empêche de nouvelles initiations, puis ont créé une minuscule zone de dommage UV à l’intérieur de chaque noyau cellulaire. En suivant un marqueur chimique spécifique de la forme active de la polymérase, ils ont pu observer à quelle vitesse elle disparaissait de la zone endommagée comparée au reste du génome. En parallèle, ils ont développé un test complémentaire mesurant la quantité totale de polymérase active dans des extraits cellulaires, révélant non seulement quand les polymérases quittaient l’ADN, mais aussi quand elles étaient dégradées par le système d’élimination de la cellule.
Baliser les machines bloquées pour les éliminer
L’équipe s’est concentrée sur la réparation liée à la transcription, un système spécialisé qui répare les lésions sur les gènes en cours de lecture. Ils ont utilisé une série de lignées cellulaires humaines appariées, chacune déficiente pour un facteur de réparation différent. Deux protéines, CSB et CSA, sont apparues comme des gardiens décisifs. Lorsqu’elles faisaient défaut, la polymérase II s’accumulait et restait obstinément sur les sites endommagés, et la cellule n’arrivait pas à la dégrader. Biochimiquement, ces cellules ne parvenaient pas non plus à ajouter de petites étiquettes ubiquitine à un site clé de la polymérase. En revanche, les cellules dépourvues de protéines intervenant plus tard dans la réparation — celles qui excisent et remplacent l’ADN endommagé — débarrassaient toujours la polymérase normalement. Cela montre que le marquage initial par l’ubiquitine de la polymérase bloquée est le déclencheur critique pour décider de son sort.
Deux équipes de nettoyage : une rapide, une de secours
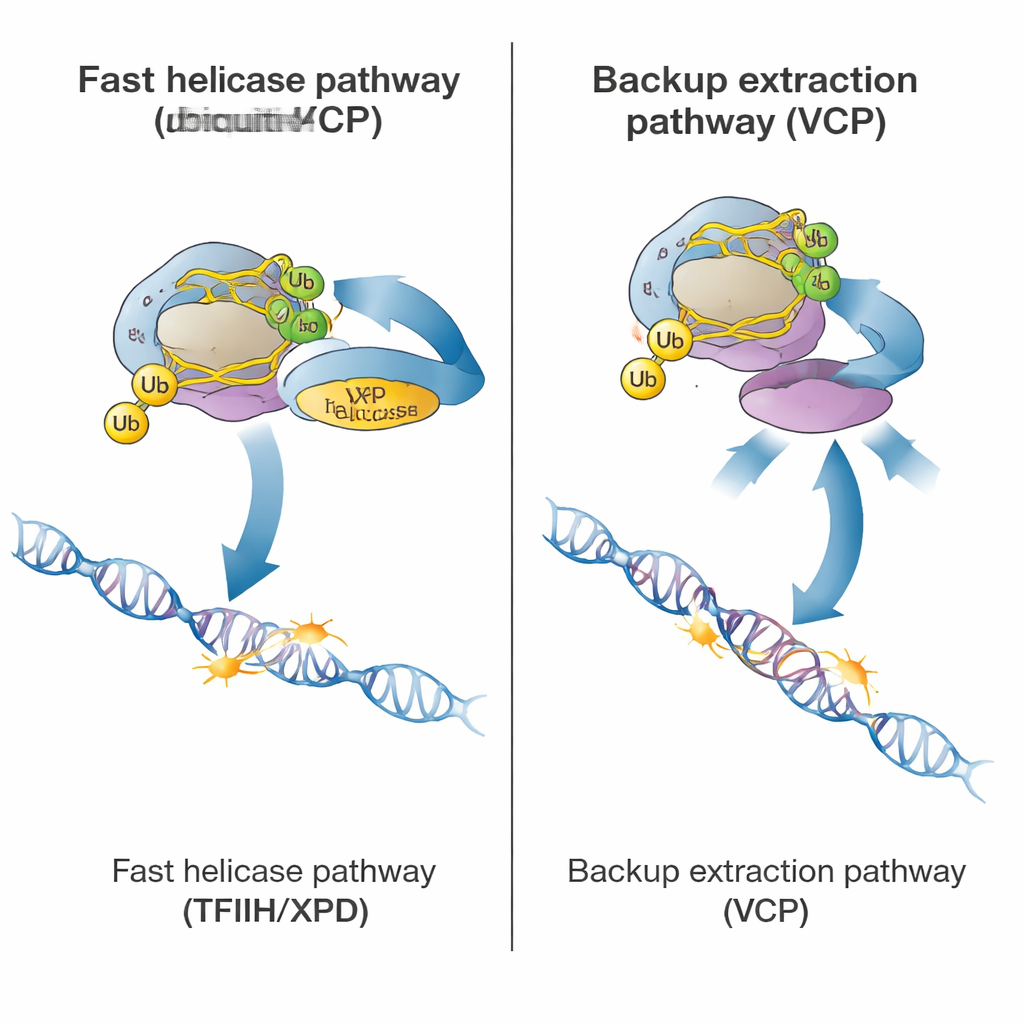
Une fois la polymérase marquée, la cellule peut choisir entre deux voies pour l’éliminer. La voie principale et rapide repose sur un grand complexe de réparation appelé TFIIH, et en particulier sur sa sous-unité hélicase XPD, qui utilise de l’énergie pour dérouler l’ADN. Des protéines auxiliaires, notamment ELOF1, UVSSA et STK19, amènent TFIIH vers la polymérase bloquée et positionnent XPD sur l’ADN juste en amont. À l’aide de nouveaux tests dans des cellules de patients portant une mutation rendant XPD inactif en tant qu’hélicase, les auteurs ont montré que lorsque XPD ne peut pas dérouler l’ADN, l’élimination de la polymérase ralentit fortement, même si le reste de la machinerie de réparation est présent. Cela indique que l’action mécanique de XPD est ce qui « décroche » normalement la polymérase de la lésion pour permettre aux enzymes de réparation d’accéder au site endommagé.
Un plan B lent mais essentiel
L’étude a également mis en évidence une voie de secours, plus lente, pour dégager la polymérase bloquée. Cette voie dépend de VCP (également appelé p97), une protéine qui reconnaît les marques d’ubiquitine et peut extraire de force des protéines de la chromatine. Dans des cellules saines avec TFIIH pleinement fonctionnel, bloquer VCP n’a qu’un effet mineur. Mais dans des cellules où TFIIH était absent, mal positionné ou porté par une XPD hélicase-inactive, l’élimination de la polymérase devenait presque entièrement dépendante de VCP. Dans ces situations, VCP pouvait encore arracher la polymérase marquée de l’ADN, même lorsque la réparation normale ne pouvait pas se dérouler. Crucialement, cette voie de secours requérait toujours un certain marquage par l’ubiquitine, ce qui explique pourquoi les cellules dépourvues de CSB ou CSA — et donc de marques d’ubiquitine — échouaient à la fois dans la voie principale et dans la voie de secours.
Pourquoi cela compte pour la santé et la maladie
Dans l’ensemble, ce travail décrit un programme de sécurité hiérarchique que les cellules mettent en œuvre chaque fois que l’ARN polymérase II rencontre des dommages à l’ADN. D’abord, CSB et CSA marquent la machine bloquée par l’ubiquitine. Si tout fonctionne correctement, TFIIH et son hélicase XPD dégagent rapidement la polymérase pour que la lésion soit excisée et réparée. Si TFIIH ne peut pas accomplir sa tâche, VCP intervient pour extraire la polymérase et l’envoyer à la dégradation, empêchant qu’elle n’encombre l’expression des gènes même si le dommage persiste. Ce cadre aide à expliquer pourquoi les défauts héréditaires de CSB ou CSA entraînent des troubles neurologiques particulièrement sévères : sans marquage par l’ubiquitine, les cellules perdent à la fois la voie principale menée par la réparation et la voie de secours d’extraction, laissant les polymérases bloquées sur des gènes endommagés et la transcription bloquée de façon chronique.
Citation: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Mots-clés: réparation de l’ADN liée à la transcription, ARN polymérase II, dommages à l’ADN induits par les UV, ubiquitination des protéines, syndrome de Cockayne