Clear Sky Science · fr
Modification de l’ADN par phosphorothioation par les systèmes BREX de type 4 dans le microbiome intestinal humain
Retouches chimiques cachées chez nos bactéries intestinales
Au cœur de l’intestin humain, des trillions de bactéries échangent sans cesse des gènes, combattent des virus et réagissent à la chimie de notre alimentation. Cette étude révèle que nombre de ces microbes réécrivent discrètement l’échafaudage de leur propre ADN en substituant des atomes de soufre, créant une marque particulière appelée phosphorothioate. Le travail met au jour une nouvelle version de ce système, associée à un ensemble de défense bactérienne nommé BREX de type 4, et explore l’étendue de ces marques soufrées chez les bactéries intestinales susceptibles d’influencer la santé et la maladie.
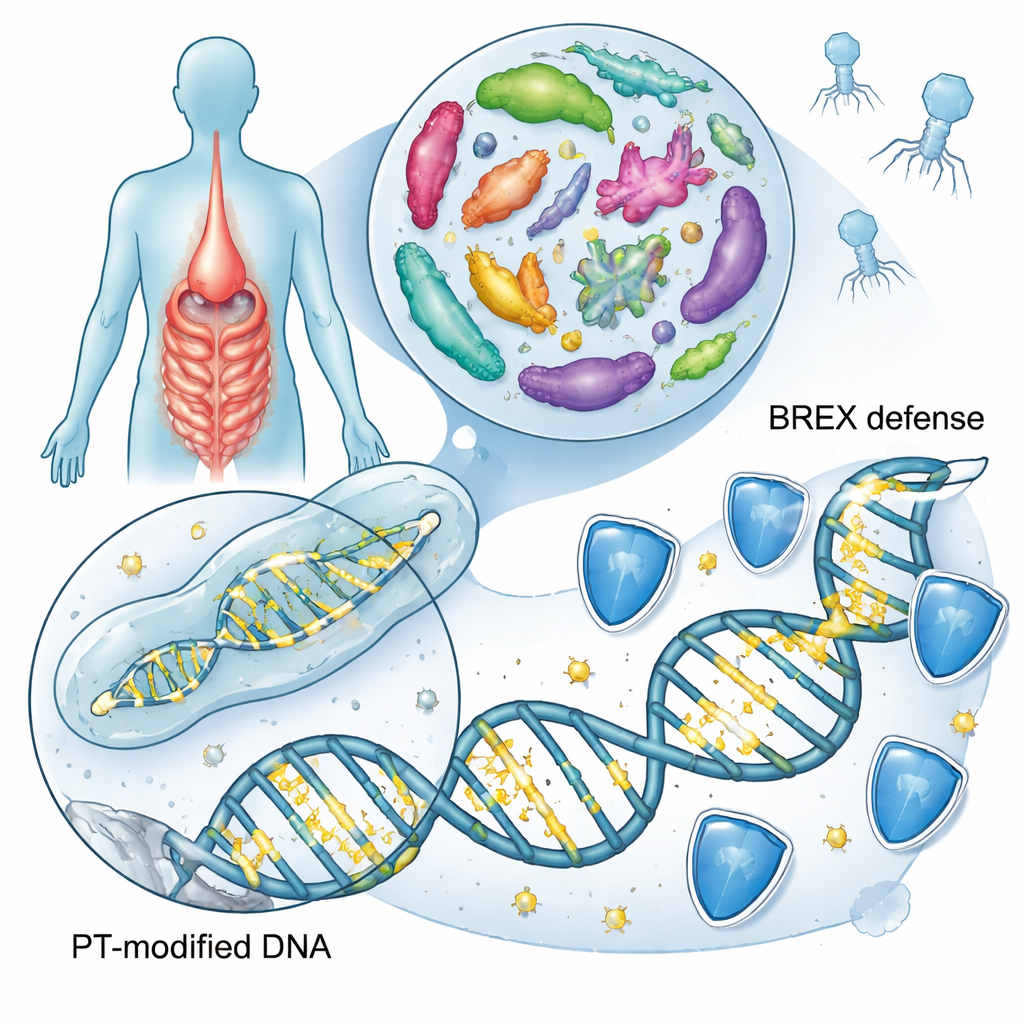
Une autre forme de marque sur l’ADN
La plupart des gens ont entendu parler des lettres de l’ADN — A, T, C et G — modifiées par de petites étiquettes chimiques comme les groupes méthyle, un élément clé de l’épigénétique. Ici, l’attention se porte sur quelque chose de beaucoup plus radical : certaines bactéries remplacent l’un des atomes d’oxygène de l’échafaudage de l’ADN par du soufre. Cet ajustement de la colonne vertébrale, appelé phosphorothioation, modifie le comportement de l’ADN sans altérer le code génétique. Des études antérieures avaient identifié deux familles principales de gènes, nommées dnd et ssp, qui installent ces marques soufrées chez environ une bactérie ou archée sur dix. Ces marques aident les bactéries à reconnaître leur propre ADN, à repousser les virus envahisseurs appelés phages, et peuvent aussi participer à la réponse au stress oxydatif et à l’inflammation.
Analyse de milliers de génomes intestinaux
Pour évaluer la fréquence de l’ADN marqué au soufre dans nos intestins, les chercheurs ont exploré 13 663 génomes bactériens issus de trois grandes collections de microbes humains intestinaux. Ils ont recherché des signatures génétiques clés suffisantes pour installer les marques soufrées : des ensembles de gènes dnd, ssp, ou un nouvel ensemble candidat nommé brx, faisant partie de BREX, un système anti-phage connu. Environ 6,3 % des génomes intestinaux portaient au moins un de ces systèmes, principalement dans les groupes courants du microbiote tels que Bacteroidota, Bacillota et Pseudomonadota. Par rapport à un catalogue plus large de bactéries provenant de divers environnements, l’intestin présentait un enrichissement net de la version BREX de type 4, suggérant que cette défense basée sur le soufre est particulièrement favorisée dans l’écosystème intestinal.
Un nouveau système de défense à base de soufre
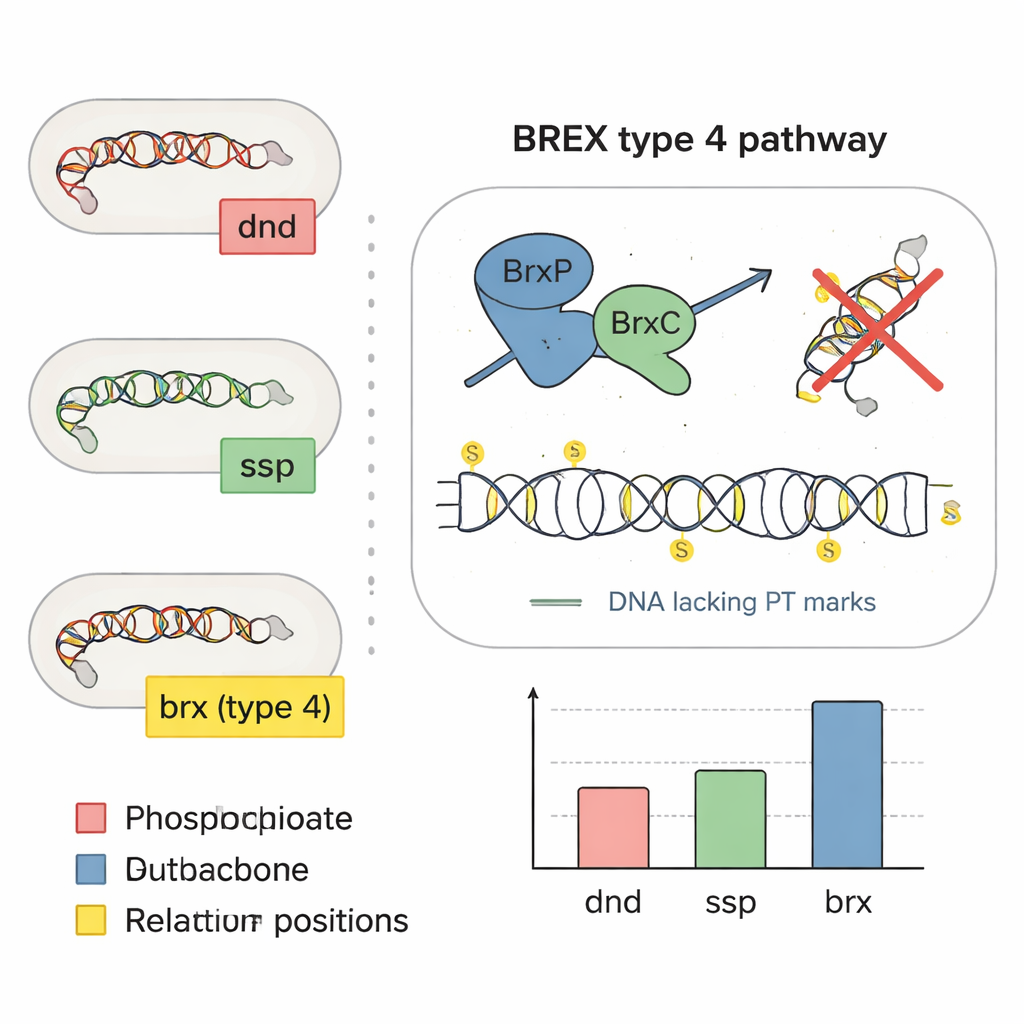
En examinant l’agencement des gènes le long des chromosomes bactériens, l’équipe a repéré des gènes de type dnd nichés parmi des gènes de défense BREX, laissant penser que certains systèmes BREX pourraient installer directement des marques soufrées. Ils se sont concentrés sur un ensemble de quatre gènes centraux, brxP, brxC, brxZ et brxL, et ont montré par analyse de séquences que BrxP et BrxC ressemblent aux protéines manipulant le soufre des systèmes ssp. Des expériences dans la bactérie intestinale humaine Bacteroides salyersiae ont confirmé l’hypothèse : lorsque les chercheurs ont supprimé le gène brxC, l’ADN modifié par le soufre a disparu ; lorsqu’ils ont réintroduit brxC sur un plasmide, les marques soufrées sont réapparues. Ils ont aussi transféré des gènes BREX clés dans une autre bactérie intestinale dépourvue de ces systèmes et ont montré qu’elle commençait à produire le même motif d’ADN marqué au soufre, démontrant que la machinerie BREX de type 4 peut, à elle seule, créer des marques de phosphorothioate.
Cartographier l’emplacement du soufre sur le génome
Identifier les marques soufrées ne suffit pas ; connaître précisément où elles se déposent le long de l’ADN est crucial pour comprendre leur fonction. Les chercheurs ont combiné une spectrométrie de masse sensible avec une méthode de séquençage personnalisée appelée PT-seq, qui coupe sélectivement l’ADN aux sites modifiés par le soufre puis lit la séquence environnante. Sur 226 isolats bactériens intestinaux, ils ont identifié huit « blocs » dinucléotidiques distincts contenant du soufre, et à partir de souches représentatives ont déduit des motifs courts complets où le soufre a tendance à se placer. De façon intrigante, les bactéries porteuses de systèmes dnd, ssp ou BREX produisaient des ensembles différents de motifs soufrés, comme des dialectes distincts d’un même langage chimique. Les marques n’étaient pas réparties aléatoirement : elles étaient enrichies dans les gènes d’ARN ribosomique et généralement évitaient les débuts et fins des gènes codants, ce qui suggère que les bactéries peuvent diriger le soufre loin de régions de contrôle sensibles.
Quelles implications pour notre santé
Pour un non-spécialiste, ces résultats montrent que les bactéries intestinales font bien plus que se nourrir de notre alimentation — elles réécrivent activement la chimie de leur propre ADN de façons qui influent sur leur lutte contre les virus et leur réponse aux conditions oxydantes souvent associées à l’inflammation. En identifiant BREX de type 4 comme un nouveau système d’apposition de marques soufrées et en montrant qu’environ un microbe intestinal sur treize possède une forme de machinerie de phosphorothioation, ce travail pose les bases pour explorer comment ces marques d’ADN inhabituelles affectent la stabilité du microbiome, la résistance aux infections et possiblement l’évolution de maladies comme la maladie inflammatoire intestinale. À plus long terme, comprendre et éventuellement manipuler ces systèmes épigénétiques à base de soufre pourrait offrir de nouvelles stratégies pour moduler le microbiome intestinal en faveur de la santé humaine.
Citation: Yuan, Y., DeMott, M.S., Byrne, S.R. et al. Phosphorothioate DNA modification by BREX type 4 systems in the human gut microbiome. Nat Commun 17, 1717 (2026). https://doi.org/10.1038/s41467-026-68412-5
Mots-clés: microbiome intestinal, épigénétique bactérienne, phosphorothioation de l’ADN, système de défense BREX, bactériophages