Clear Sky Science · fr
Visualisation in situ de l'hétérogénéité phénotypique et de la morphologie cellulaire individuelle de Clostridioides difficile pendant l’infection intestinale
Pourquoi les microbes intestinaux ne se comportent pas tous de la même façon
Clostridioides difficile, souvent appelé C. difficile, est un germe nosocomial redouté pouvant provoquer une diarrhée sévère, parfois mortelle, après que des antibiotiques ont perturbé la flore intestinale normale. Pourtant, même lorsque ces bactéries sont génétiquement identiques et partagent le même environnement, des cellules individuelles peuvent se comporter très différemment. Cette étude révèle, avec un niveau de détail sans précédent, comment des cellules uniques de C. difficile activent ou désactivent la production de toxines et modifient même leur forme lors d’une infection du côlon de souris, offrant des indices sur la persistance et la difficulté de traiter cette maladie.
Suivre en temps réel un envahisseur intestinal dangereux
Pour comprendre le comportement des cellules individuelles de C. difficile à l’intérieur de l’organisme, les chercheurs devaient les voir clairement au milieu de la communauté dense et diversifiée des microbes intestinaux. Ils ont conçu des souches de C. difficile qui brillent en permanence en couleurs vives au microscope, en utilisant des protéines fluorescentes spéciales qui n’affectent pas la capacité des bactéries à croître ou à provoquer la maladie. En infectant des souris traitées aux antibiotiques avec ces souches fluorescentes, puis en découpant et en colorant le côlon, ils ont pu localiser précisément les comportements et les positions de milliers de cellules bactériennes individuelles au sein d’un tissu intestinal intact. 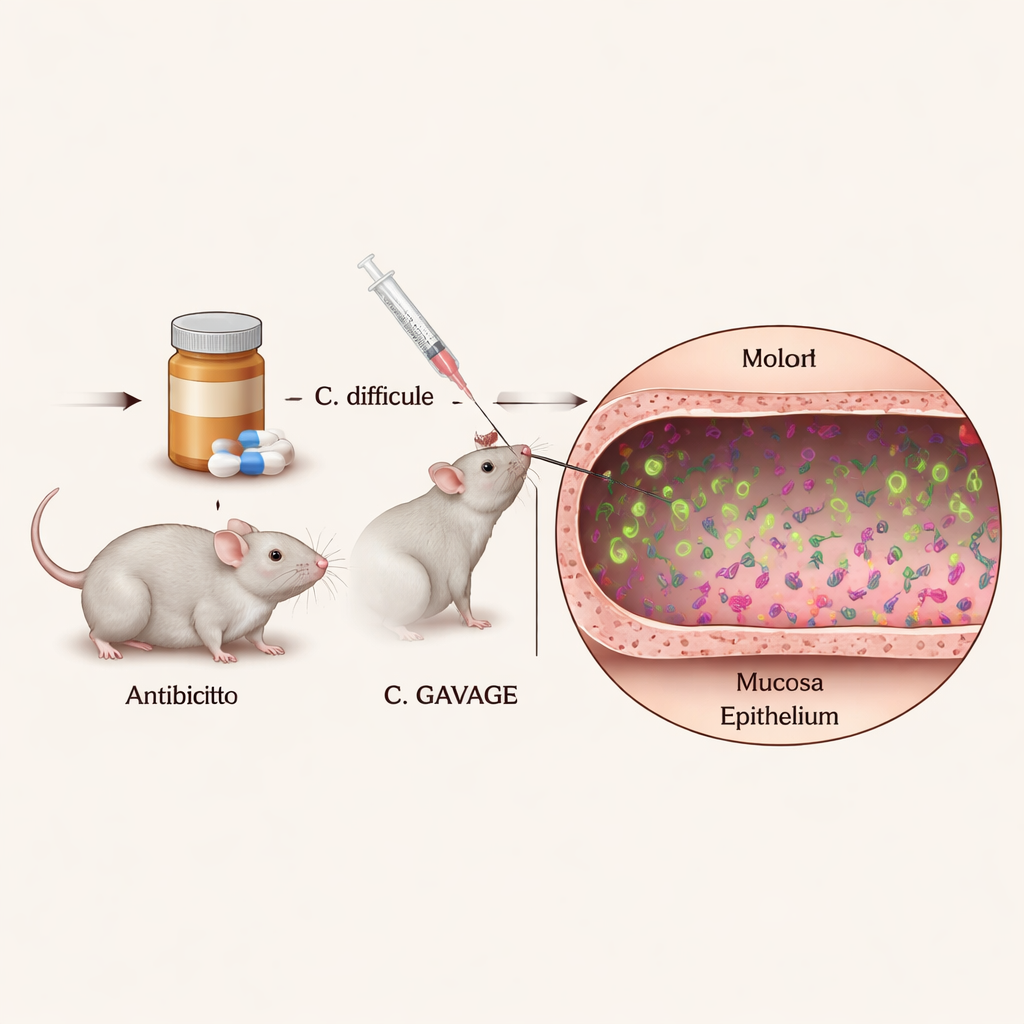
Où vivent les bactéries dans le côlon
Les images ont montré que la majorité des cellules de C. difficile se trouvent au centre du contenu du côlon, appelé lumière, confirmant que l’organisme est principalement un pathogène « luminal » en suspension. Cependant, une minorité notable de cellules apparaissait systématiquement près de la couche de mucus et directement au contact de l’épithélium — la fine couche de cellules qui tapisse le côlon et fait office de barrière. Cette sous‑population en contact étroit n’avait pas été clairement observée auparavant chez des souris conventionnelles avec un système immunitaire normal. Fait important, les balises fluorescentes introduites n’affectaient pas de manière visible la virulence des bactéries chez l’animal, ce qui suggère que les images reflètent probablement le comportement réel de C. difficile lors d’une infection.
Qui produit la toxine, et où ?
L’équipe a ensuite ajouté un second signal fluorescent qui s’allume uniquement lorsque C. difficile active ses gènes de toxine. Les toxines sont les protéines délétères qui endommagent la muqueuse intestinale et provoquent les symptômes de la maladie ; elles sont aussi ce que les médecins recherchent dans les analyses de selles pour poser le diagnostic. De manière surprenante, les bactéries ne produisaient pas toutes les toxines en même temps. À un moment donné, seule une fraction des cellules s’illuminait comme « toxine‑ON », tant au début qu’à la fin de l’infection. Cette fraction était plus élevée dans une souche mutante génétiquement programée pour surfabriquer la toxine, mais même dans ce cas, toutes les cellules n’étaient pas engagées. Autre constat frappant : la position d’une cellule — flottant dans la lumière, logée dans le mucus ou au contact de l’épithélium — n’influençait pas fortement la fréquence de production de toxine ni l’intensité d’activation de ces gènes. 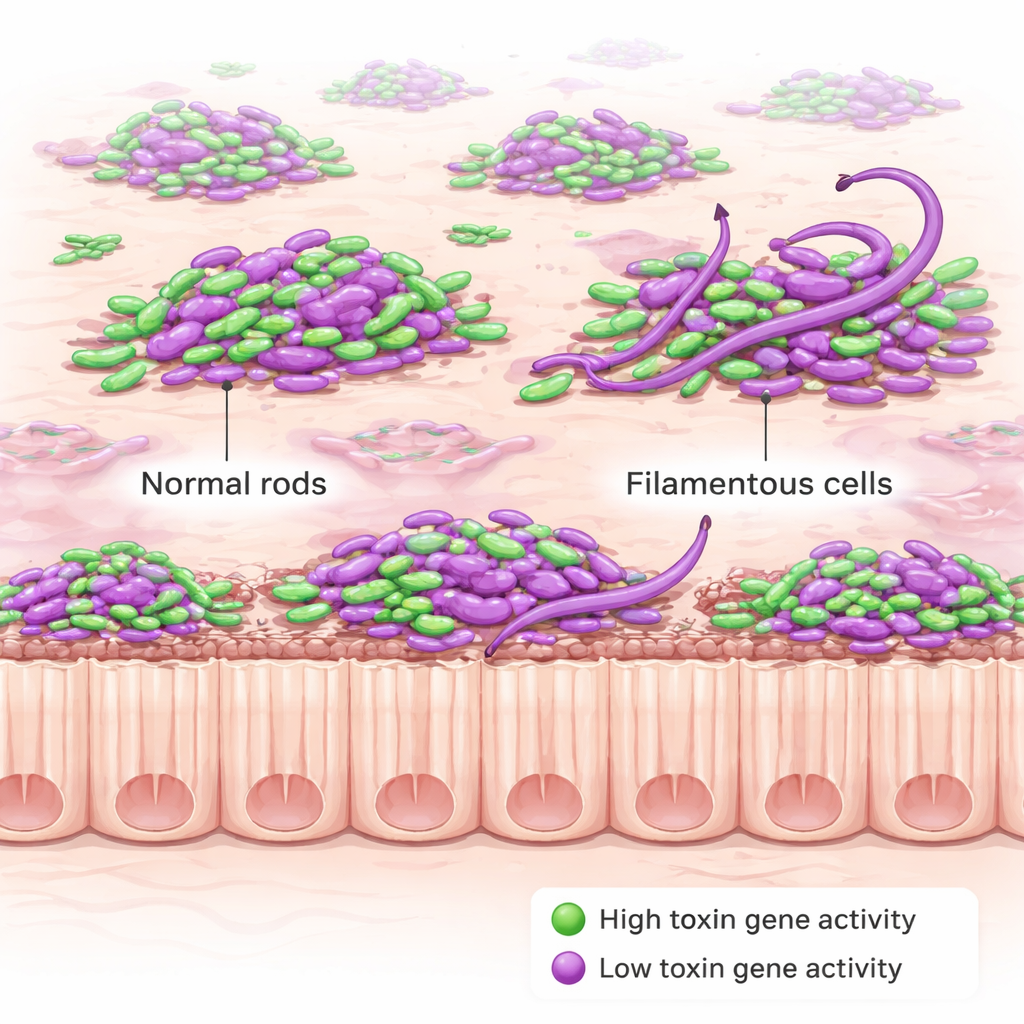
Des cellules qui changent de forme sous stress
En cartographiant la production de toxine, les chercheurs ont découvert un comportement nouveau et surprenant. Chez les souris infectées par la souche mutante surfabricante de toxine, de nombreuses cellules de C. difficile, pendant la phase aiguë de la maladie, sont devenues des filaments exceptionnellement longs et courbés, certains dépassant dix fois la longueur des bacilles courts habituels. Cette morphologie filamenteuse est apparue principalement en début d’infection sévère puis a diminué par la suite, et elle n’était pas observée lorsque la même souche était cultivée en bouillon de laboratoire. Cela suggère que les conditions stressantes de l’intestin enflammé — plutôt que le seul changement génétique — déclenchent cette transformation dramatique. Des expériences complémentaires ont montré que la perte d’une protéine régulatrice appelée RstA, qui contrôle à la fois les gènes de toxine et d’autres réponses au stress, favorise la formation de ces filaments.
Ce que cela signifie pour la maladie à C. difficile
Pour les non‑spécialistes, le message clé est que même une seule souche de C. difficile fonctionne comme une main‑d’œuvre divisée. Certaines cellules assument le coût énergétique de produire des toxines et d’endommager l’intestin, libérant des nutriments que leurs voisines sans toxine peuvent exploiter. Cette « division du travail » partagée peut aider l’infection à persister et à réapparaître, car toutes les cellules ne sont pas également vulnérables aux traitements qui ciblent la toxine ou les bactéries en croissance rapide. Le système rapporteur fluorescent nouvellement développé offre aux scientifiques un outil puissant pour observer, cellule par cellule, comment C. difficile et les microbes intestinaux associés s’adaptent au fil du temps et selon l’espace à l’intérieur de l’hôte. Cette compréhension pourrait ultimement orienter des thérapies visant non seulement à tuer les bactéries, mais aussi à perturber les rôles nocifs de sous‑populations particulières qui conduisent à la maladie et à la récidive.
Citation: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Mots-clés: Clostridioides difficile, microbiome intestinal, toxines bactériennes, hétérogénéité phénotypique, imagerie fluorescente