Clear Sky Science · fr
Un nanosystème ciblant l’inhibiteur tissulaire des métalloprotéinases‑1 pour une thérapie continue spatiotemporelle de la fibrose pulmonaire idiopathique
Pourquoi la cicatrisation pulmonaire tenace importe
La fibrose pulmonaire idiopathique (FPI) est une maladie pulmonaire implacable dans laquelle le tissu pulmonaire normalement spongieux est peu à peu remplacé par du tissu cicatriciel rigide. Les personnes atteintes de FPI deviennent essoufflées lors d’activités quotidiennes, et la plupart ne survivent que quelques années après le diagnostic. Les médicaments actuels peuvent ralentir la maladie pour certains patients, mais ils inversent rarement les cicatrices existantes et provoquent souvent des effets secondaires. Cette étude explore une « nano‑thérapie » inhalée intelligente conçue non seulement pour ralentir la FPI, mais aussi pour éliminer activement le tissu cicatriciel et aider les poumons à se réparer.
Le problème : cicatrices adhérentes et stress chimique
Dans la FPI, les espaces où l’oxygène passe normalement dans le sang se remplissent d’excès de protéines comme le collagène, transformant des alvéoles flexibles en zones rigides. Les auteurs se sont concentrés sur une protéine appelée TIMP‑1, qui agit comme un frein sur les enzymes naturelles qui dégradent normalement l’excès de collagène. En examinant des échantillons pulmonaires de patients et de souris avec cicatrisation induite, ils ont trouvé que les niveaux de TIMP‑1 étaient plusieurs fois supérieurs à ceux des poumons sains et augmentaient en parallèle de l’accumulation de collagène. Parallèlement, les poumons endommagés présentaient des niveaux en hausse d’espèces réactives de l’oxygène (ROS) — des « étincelles » chimiques qui blessent les cellules — et une perte de marqueurs clés des cellules tapissant les alvéoles saines. Ensemble, ces observations indiquent un cercle vicieux : trop de TIMP‑1 freine la dégradation des cicatrices, tandis que le stress oxydatif endommage davantage la structure pulmonaire.
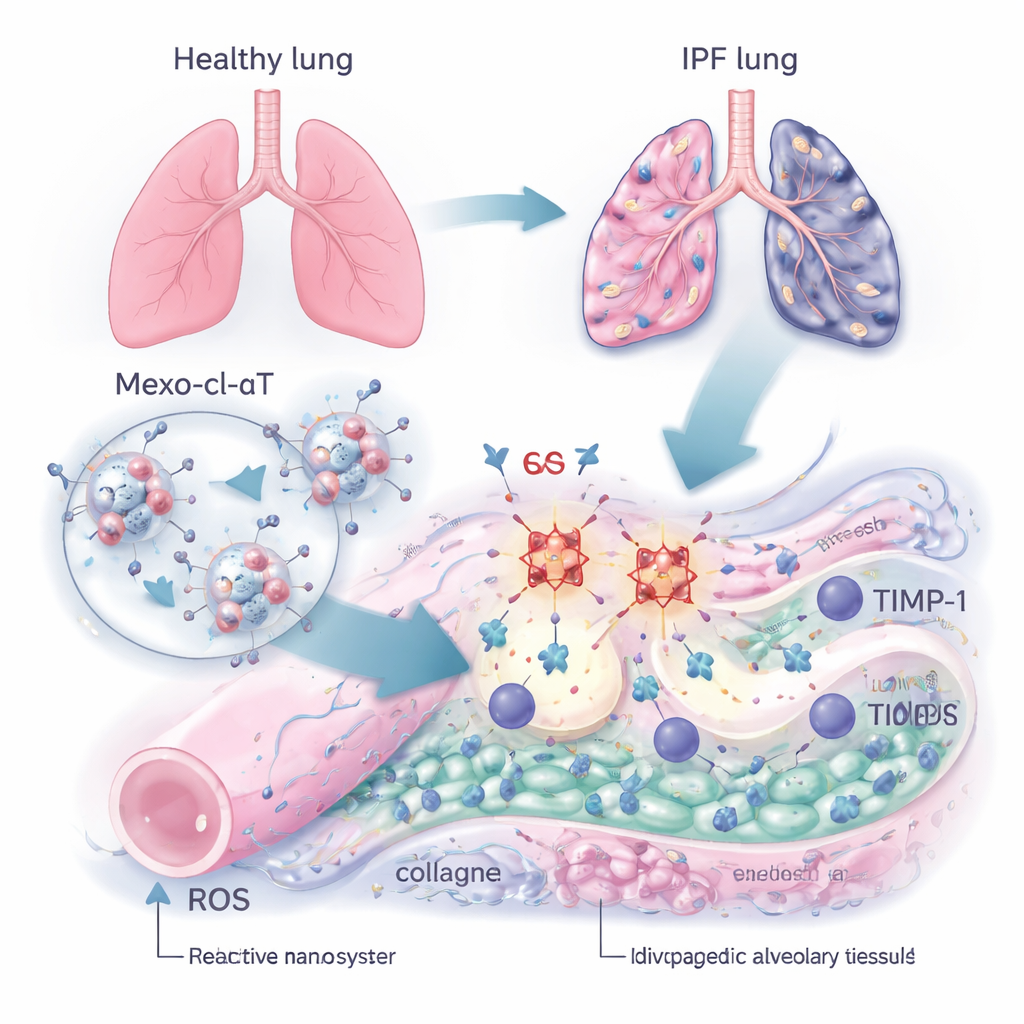
Un vecteur de délivrance intelligent : de petites capsules réparatrices
Pour rompre ce cercle, l’équipe a conçu une thérapie à l’échelle nanométrique appelée Mexo‑cl‑aT. Ils ont commencé avec des exosomes — particules naturelles en forme de bulles libérées par des cellules souches, déjà connues pour se diriger vers les tissus endommagés et favoriser la guérison. À la surface de ces exosomes, ils ont fixé des anticorps qui se lient spécifiquement au TIMP‑1. La connexion entre l’exosome et l’anticorps a été obtenue à l’aide d’un linker chimique spécial qui peut être coupé par les ROS. Autrement dit, l’environnement chimique agressif d’un poumon cicatrisé sert de signal : lorsque l’exosome atteint une région abîmée riche en ROS, le linker se casse, absorbant une partie des ROS et libérant l’anticorps précisément là où TIMP‑1 est concentré, tandis que l’exosome continue de favoriser la réparation tissulaire.
Comportement et mécanisme du nanosystème
Dans des études cellulaires, les chercheurs ont montré que Mexo‑cl‑aT reste stable en milieu fluide mais libère rapidement ses anticorps lorsqu’il est exposé à des niveaux de peroxyde d’hydrogène similaires à ceux observés dans les poumons malades. Parallèlement, il réduit nettement la quantité de peroxyde présente, confirmant son rôle d’éliminateur de ROS. Dans des modèles cellulaires semblables à des tissus cicatriciels, les anticorps libérés ont diminué les niveaux de TIMP‑1 et ont libéré les enzymes responsables de la dégradation du collagène, tandis que la composante exosome a réduit la mort cellulaire, stimulé la prolifération et accéléré la fermeture des plaies tant dans les cellules pulmonaires que vasculaires. Comparée à des versions dont le linker ne pouvait pas être coupé, la conception réactive aux ROS a éliminé plus de collagène et réduit le stress chimique plus efficacement, soulignant l’importance d’une libération contrôlée.
Tests dans un modèle sévère de cicatrisation pulmonaire
L’équipe a ensuite testé la thérapie chez des souris atteintes d’une fibrose pulmonaire avancée déclenchée par la bléomycine, un modèle choisi pour imiter une FPI à un stade tardif. Une dose unique de Mexo‑cl‑aT inhalée a persisté dans les poumons pendant plusieurs jours et a retenu plus d’anticorps que le simple mélange de ses composants. Les poumons traités paraissaient plus sains à l’œil nu et au microscope : les espaces aériens se sont rouvrerts, l’épaisseur des cicatrices a diminué et la teneur totale en collagène est presque revenue à la normale. Les marqueurs des cellules productrices de cicatrices activées ont chuté, tandis que les protéines liées aux cellules tapissant les alvéoles et les vaisseaux sanguins saines ont augmenté. Les mesures chimiques ont montré que le traitement a fortement réduit les niveaux de TIMP‑1, rétabli l’équilibre des enzymes dégradant le collagène et éliminé environ les trois quarts des ROS en excès. Fait important, les marqueurs d’inflammation ont diminué et les analyses sanguines et examens d’organes n’ont pas révélé de toxicité évidente.
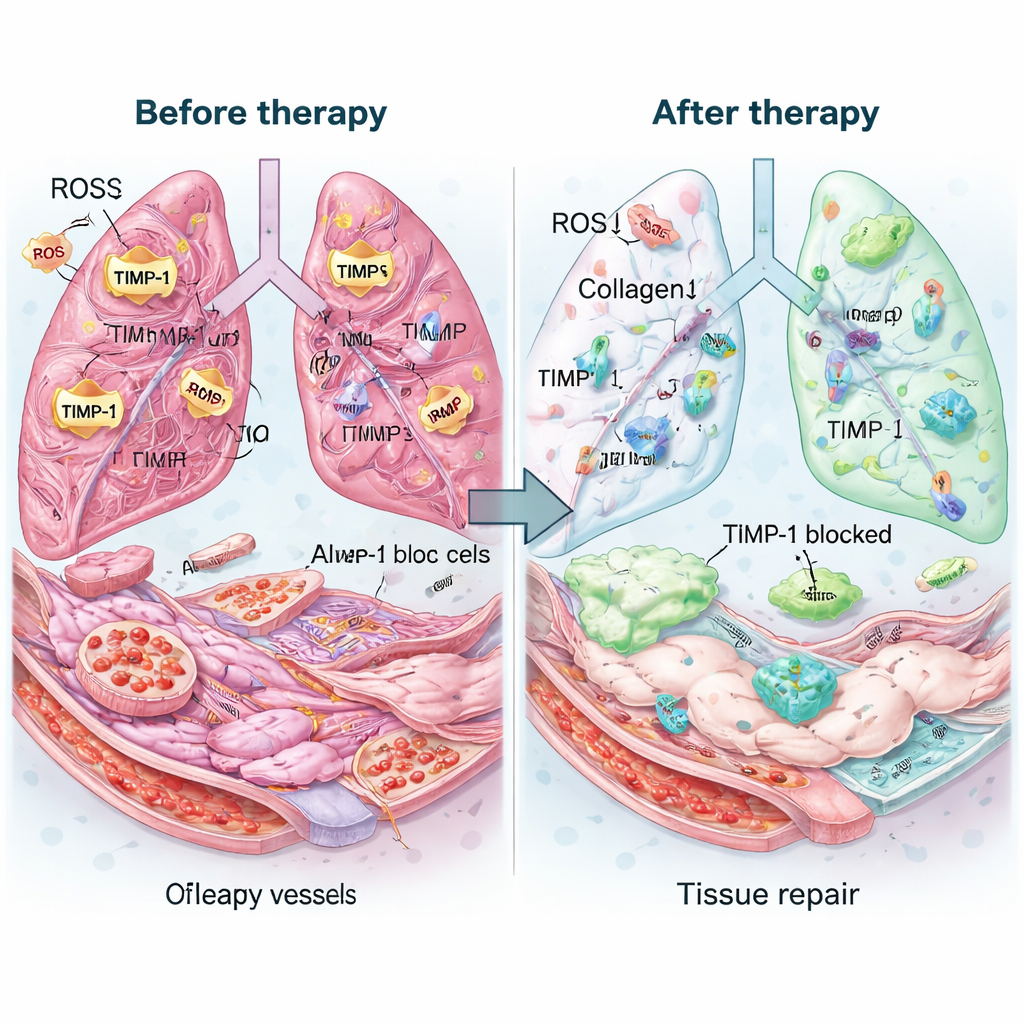
Ce que cela pourrait signifier pour les patients
Pour les personnes vivant avec la FPI, ce travail n’offre pas encore de cure immédiate, mais il introduit une piste prometteuse. Plutôt que de se limiter à ralentir les nouveaux dommages, le nanosystème Mexo‑cl‑aT vise à annuler activement les cicatrices existantes, calmer le stress chimique nocif et soutenir la reconstruction du tissu pulmonaire fragile — le tout sous une forme inhalée ciblée qui concentre le traitement là où il est le plus nécessaire. Bien que des défis subsistent, tels que la production d’exosomes à grande échelle et les essais chez l’humain, l’étude suggère que des nano‑thérapies de précision, accordées à l’environnement pathologique, pourraient un jour transformer la prise en charge des cicatrices pulmonaires tenaces, et peut‑être d’autres maladies fibrotiques.
Citation: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Mots-clés: fibrose pulmonaire idiopathique, cicatrisation pulmonaire, nanomédecine, thérapie par exosomes, TIMP‑1