Clear Sky Science · fr
Des états des cellules épithéliales lésées influencent la survie des greffons rénaux après un rejet médié par les lymphocytes T
Pourquoi cette recherche rénale compte pour les patients
Les transplantations rénales peuvent sauver des vies, mais beaucoup échouent des années après l’intervention, même lorsque les médecins semblent maîtriser l’attaque immunitaire appelée rejet médié par les lymphocytes T. Cette étude pose une question simple mais cruciale : si la réaction immunitaire paraît « traitée » au microscope, pourquoi certains reins transplantés s’épuisent-ils quand même prématurément ? En examinant les cellules individuelles dans des reins transplantés de souris et d’humains, les chercheurs mettent au jour un niveau caché de dommages dans les tubules filtrants du rein qui aide à expliquer quels greffons survivent et lesquels ne survivent pas.
Au‑delà des signes classiques de rejet
Les médecins diagnostiquent généralement le rejet médié par les lymphocytes T en observant des globules blancs envahir le rein et attaquer les petits tubules qui traitent l’urine. Des médicaments anti‑rejet puissants peuvent souvent repousser ces cellules immunitaires et améliorer l’aspect de la biopsie. Pourtant, les patients atteints de ce type de rejet restent exposés à un risque élevé d’échec du greffon. De larges études génétiques antérieures laissaient entendre que des signes de lésion tissulaire au sein des cellules rénales prédisent mieux l’issue que le simple comptage des cellules immunitaires présentes. Les auteurs se sont donc donné pour objectif de définir ces signaux de lésion à la résolution unicellulaire et d’évaluer à quel point ils sont liés à la survie à long terme de la greffe.
Analyser le rejet cellule par cellule
L’équipe a d’abord utilisé un modèle murin contrôlé, en transplantant des reins entre souris génétiquement identiques ou entre souches incompatibles pour déclencher un rejet. Ils ont ensuite appliqué le séquençage ARN de noyau unique, qui lit l’activité de milliers de gènes dans chaque cellule, et la transcriptomique spatiale, qui montre où ces cellules se situent dans la tranche tissulaire. Ces outils ont révélé que, lors du rejet, les changements moléculaires les plus marqués n’apparaissent pas dans les cellules immunitaires mais dans les propres cellules épithéliales du rein, qui tapissent les tubules proximaux et un segment appelé la branche ascendante large. Dans ces zones, les cellules activent des gènes de lésion et de stress, des signaux inflammatoires et des marqueurs d’un état plus primitif et moins spécialisé, tout en réprimant les fonctions de transport nécessaires à une filtration saine.
Poches cachées de cellules tubulaires gravement lésées
En regroupant les cellules selon leur activité génique similaire, les chercheurs ont identifié plusieurs « états de lésion » distincts parmi les cellules tubulaires des reins de souris. Certains reflétaient des réponses de stress précoces, tandis que d’autres représentaient des cellules sévèrement endommagées, hautement altérées, ayant perdu leur identité normale et produisant de nombreuses molécules inflammatoires et pro‑cicatrisantes. La cartographie spatiale a montré que ces états cellulaires ne se répartissaient pas de manière homogène : certains états de lésion sévère formaient des poches irrégulières à travers le cortex rénal et la médulla externe et se trouvaient dans des voisinages complexes avec des lymphocytes T, des macrophages et des fibroblastes. En revanche, certaines cellules lésées dans des régions plus profondes étaient étonnamment isolées des cellules immunitaires, ce qui suggère des modes différents d’apparition et de persistance des dommages.
Relier les états de lésion murins aux greffes humaines
Les auteurs ont ensuite cherché à savoir si des états cellulaires similaires existaient chez l’humain. Ils ont analysé des biopsies de reins transplantés humains présentant un rejet médié par les lymphocytes T actif et des greffons stables. Les données unicellulaires ont à nouveau révélé des cellules des tubules proximaux et de la branche ascendante large dont les profils géniques correspondaient étroitement aux états murins les plus sévèrement lésés. En utilisant ces signatures humaines, l’équipe a « déconvolué » des milliers de profils d’expression génique de biopsies en vrac plus anciens et a constaté que les états tubulaires sévèrement lésés étaient plus fréquents dans le rejet médié par les lymphocytes T et le rejet mixte que dans le rejet uniquement par anticorps ou l’absence de rejet. De manière importante, ils ont construit des jeux de gènes compacts représentant chaque état de lésion et les ont scorés dans une grande cohorte avec un suivi détaillé.
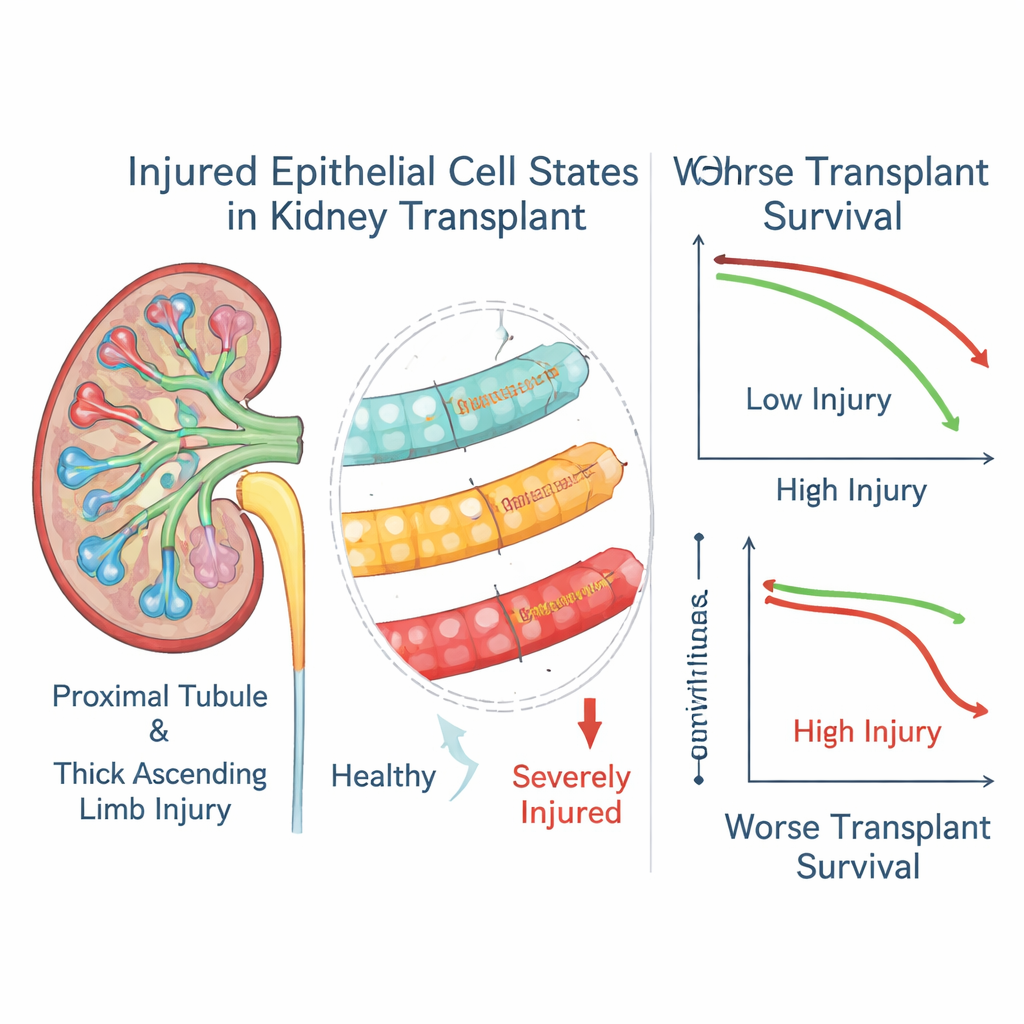
Les cellules tubulaires lésées comme prédicteurs du sort du greffon
Lorsque les auteurs ont relié ces scores géniques aux résultats à trois ans chez plus d’un millier de receveurs de greffe, un schéma net est apparu. Des niveaux élevés de marqueurs des états épithéliaux les plus sévèrement lésés, tant dans les tubules proximaux que dans la branche ascendante large, étaient fortement associés à un risque accru de perte du greffon, même chez des patients dont les biopsies avaient par ailleurs été classées comme rejet traité. Un état de lésion tubulaire plus modéré montrait la tendance inverse et était lié à une meilleure survie, ce qui suggère qu’il peut représenter un programme de réparation plus réussi. Dans un sous‑groupe de patients ayant subi des biopsies répétées, les scores d’« état sévère » restaient souvent élevés longtemps après que l’épisode de rejet semblait résolu, ce qui implique que ces cellules altérées peuvent persister et continuer d’influencer la maladie.
Ce que cela signifie pour la prise en charge des transplantations
Pour les non‑spécialistes, le message clé est que tous les dégâts observés dans un rein en rejet ne proviennent pas directement des cellules immunitaires, et que toutes les lésions ne disparaissent pas lorsque l’attaque immunitaire se calme. Cette étude montre que des poches tenaces de cellules tubulaires gravement lésées agissent comme un système d’alerte précoce pour une future défaillance du greffon. À terme, des tests simples basés sur ces signatures géniques de lésion — éventuellement même en utilisant des cellules éliminées dans l’urine — pourraient aider les médecins à identifier les patients à haut risque, à adapter les traitements et à surveiller si les reins récupèrent réellement. Ces travaux désignent aussi ces cellules épithéliales lésées comme des cibles potentielles pour de nouvelles thérapies visant à protéger les reins transplantés au‑delà de l’immunosuppression standard.
Citation: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Mots-clés: rejet de greffe rénale, lésion des cellules tubulaires, séquençage unicellulaire, survie de la greffe, états des cellules épithéliales