Clear Sky Science · fr
Le polymorphisme de CD39 favorise la thrombose pulmonaire dans la drépanocytose
Pourquoi c’est important pour les personnes atteintes de drépanocytose
La drépanocytose touche des millions de personnes dans le monde et endommage souvent les poumons, conduisant parfois à des caillots soudains et potentiellement mortels. Pourtant, seuls certains patients développent ces caillots pulmonaires dangereux, alors qu’ils partagent tous le même trouble sanguin de base. Cette étude révèle un système de protection intrinsèque présent chez de nombreux patients drépanocytaires — et explique pourquoi une variante génétique peut désactiver cette protection chez un sous-groupe à risque.
Tiraillement dans le sang drépanocyté
Dans la drépanocytose, les globules rouges se rompent plus facilement que la normale. Lorsqu’ils éclatent, ils libèrent une petite molécule appelée ADP dans la circulation. L’ADP agit comme un signal d’alerte pour les plaquettes, les cellules qui forment les caillots. Un excès d’ADP dans les poumons peut déclencher des agrégats de plaquettes qui bouchent de petites artères pulmonaires, provoquant des épisodes douloureux et parfois mortels d’insuffisance respiratoire. Le mystère résidait dans le fait que cela n’arrive pas chez tous les patients, alors que tous subissent une destruction continue des globules rouges.
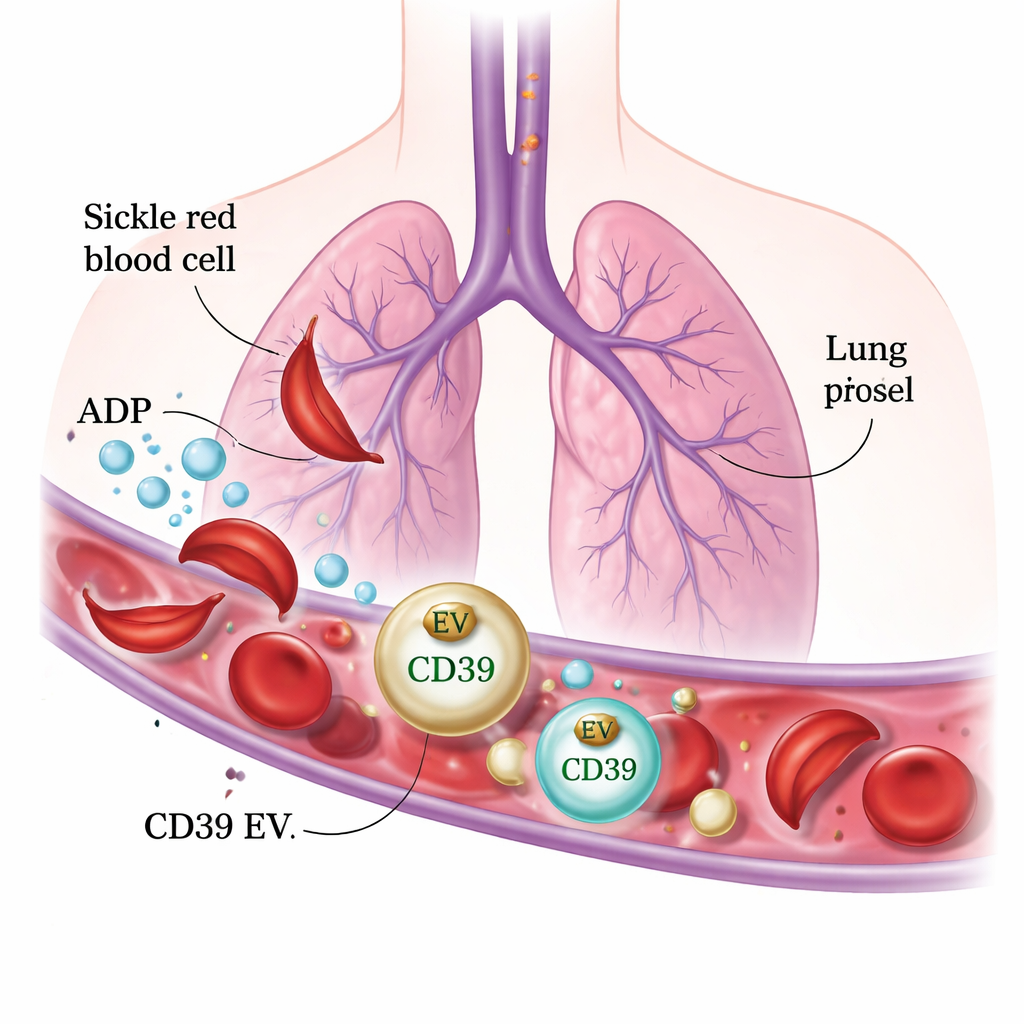
Toutes petites bulles protectrices provenant de la paroi pulmonaire
En travaillant avec des souris génétiquement modifiées portant l’hémoglobine drépanocytaire humaine, les chercheurs ont utilisé une imagerie in vivo à haute résolution pour observer ce qui se passe dans les poumons lorsque l’ADP est injecté dans la circulation. Chez les souris normales, l’ADP provoquait rapidement la formation de caillots riches en plaquettes et l’obstruction temporaire de petits vaisseaux pulmonaires. En revanche, les souris drépanocytaires étaient étonnamment protégées : leurs vaisseaux pulmonaires restaient ouverts et leurs plaquettes ne s’agrégeaient pas en réponse à l’ADP. En analysant le sang, l’équipe a trouvé beaucoup plus de petites « bulles » membranaires, appelées vésicules extracellulaires, chez les souris drépanocytaires que chez les témoins. Ces vésicules portaient de grandes quantités d’une enzyme de surface nommée CD39, qui dégrade l’ADP en une forme moins active. Dans des tests en laboratoire, les vésicules issues des souris drépanocytaires dégradaient puissamment l’ADP et empêchaient l’agrégation plaquettaire.
Désactiver la protection révèle le rôle de CD39
Pour démontrer que CD39 était responsable de cette protection, les scientifiques ont bloqué l’activité de CD39 chez les souris drépanocytaires à l’aide d’un inhibiteur chimique. Une fois CD39 inhibé, l’ADP se comportait comme prévu : il déclenchait une forte agrégation plaquettaire et des obstructions des vaisseaux pulmonaires, accompagnées d’une chute du nombre de plaquettes circulantes, signes de formation active de caillots. De même, lorsque CD39 était inhibé dans des échantillons sanguins de souris drépanocytaires, la réponse des plaquettes à l’ADP retrouvait son intensité normale. Ces expériences ont montré que CD39 porté par les vésicules dans la circulation agit comme un puissant frein aux signaux pro-coagulants dans la drépanocytose, en particulier au niveau pulmonaire.
Une variante génétique qui affaiblit le bouclier
Les chercheurs se sont ensuite intéressés aux personnes vivant avec la drépanocytose. Ils ont constaté que de nombreux patients possédaient aussi des vésicules riches en CD39 dans leur sang, et que leurs plaquettes répondaient mal à l’ADP, ce qui correspond à un effet protecteur naturel. Cependant, l’analyse génétique de plus de 400 patients a révélé que ceux portant une version particulière du gène CD39 — appelée rs3176891 G — avaient plus de chances d’avoir des antécédents de caillots pulmonaires. Dans ce sous-groupe génétique, le sang des patients contenait moins de vésicules positives pour CD39, une activité CD39 plus faible, et des plaquettes qui réagissaient plus fortement à l’ADP. Il est important de noter que cette même variante génétique n’augmentait pas le risque de caillot chez un large groupe de personnes d’ascendance africaine sans drépanocytose, ce qui suggère que le danger intervient principalement en présence d’une destruction continue des globules rouges.
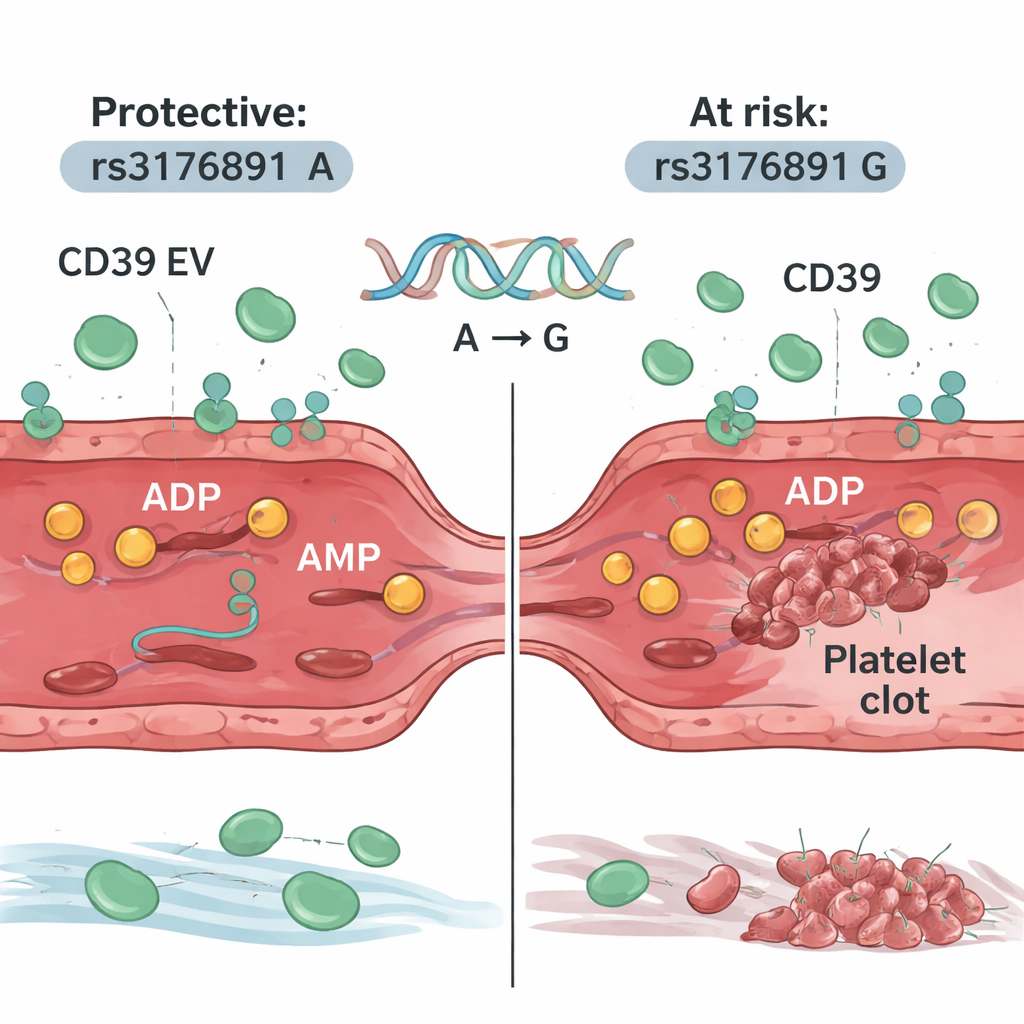
Ce que cela signifie pour les patients et les soins futurs
Pour les personnes atteintes de drépanocytose, ces résultats montrent que l’organisme n’est pas simplement submergé par des signaux pro-coagulants — il déploie aussi des contre-mesures. Chez de nombreux patients, les cellules des vaisseaux pulmonaires libèrent des vésicules riches en CD39 qui absorbent l’excès d’ADP et contribuent à empêcher les plaquettes de boucher les artères pulmonaires fragiles. Mais ceux qui héritent de la version rs3176891 G du gène CD39 peuvent disposer d’un bouclier affaibli, les rendant plus vulnérables à la thrombose pulmonaire. À l’avenir, le dépistage de cette variante génétique et la mesure des vésicules porteuses de CD39 pourraient aider à identifier les patients à risque élevé et à adapter des traitements ciblant plus précisément la signalisation plaquettaire, transformant cette nouvelle compréhension d’un mécanisme de défense naturel en meilleure protection contre l’une des complications les plus graves de la drépanocytose.
Citation: Brzoska, T., Kaminski, T.W., Katoch, O. et al. CD39 polymorphism enables lung thrombosis in sickle cell disease. Nat Commun 17, 1693 (2026). https://doi.org/10.1038/s41467-026-68396-2
Mots-clés: drépanocytose, caillots sanguins pulmonaires, plaquettes, vésicules extracellulaires, polymorphisme CD39