Clear Sky Science · fr
La modélisation du métabolisme tissulaire chez Drosophila identifie une dysrégulation métabolique induite par un régime riche en sucres dans le muscle aux niveaux des réactions et des voies
Pourquoi cette étude sur la mouche des fruits importe pour la santé humaine
Trop de sucre dans notre alimentation peut surmener la capacité de l’organisme à gérer les carburants, contribuant à terme au diabète de type 2. Cette étude utilise la mouche des fruits pour dévoiler, avec un grand niveau de détail, comment différents tissus gèrent le métabolisme et comment un régime riche en sucres perturbe la fonction musculaire. Comme les mouches partagent de nombreux gènes métaboliques et systèmes d’organes avec les humains, ces éléments aident à comprendre ce qui peut mal tourner dans nos propres muscles en cas de surcharge chronique en sucre.
Cartographier le métabolisme tissu par tissu
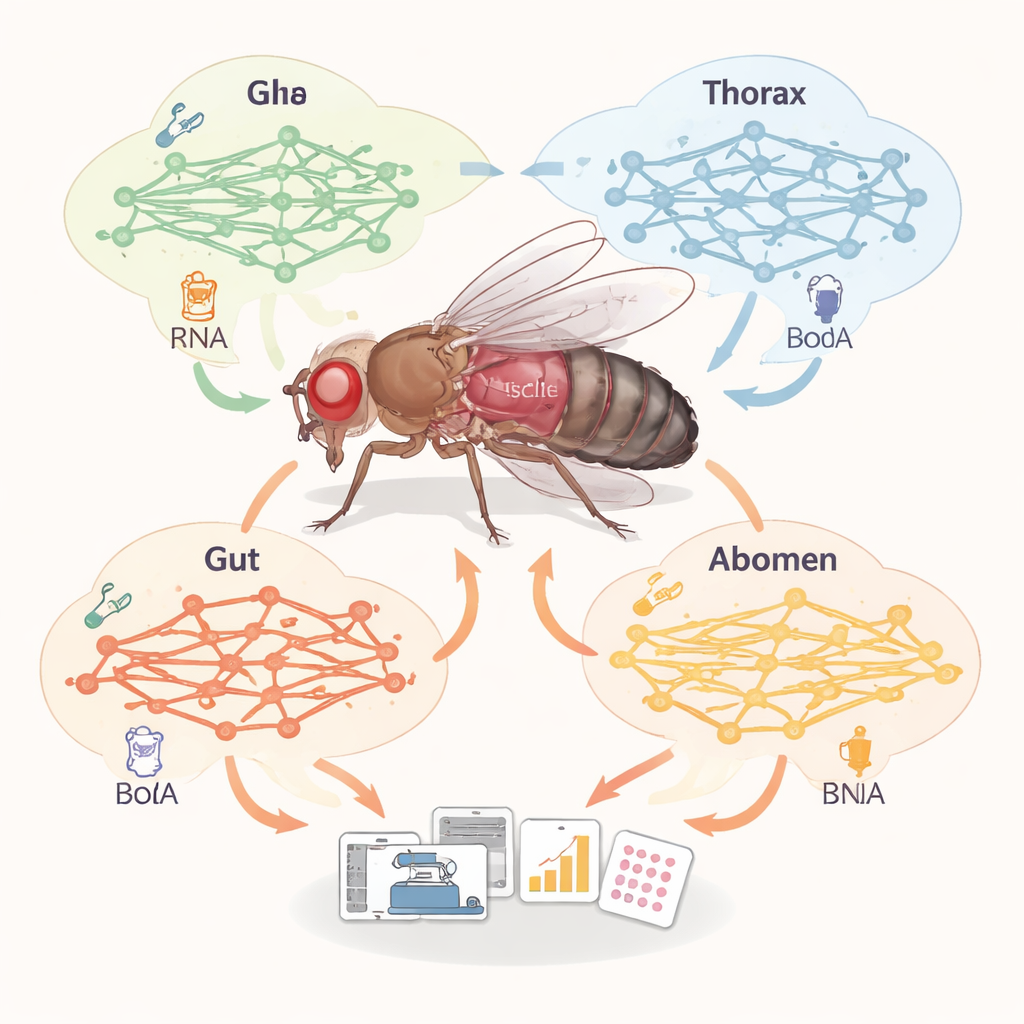
Nos corps, comme ceux des mouches, sont composés de tissus qui remplissent des rôles métaboliques très différents : le muscle brûle du carburant, le tissu adipeux le stocke, l’intestin traite les aliments, etc. Plutôt que de mesurer chaque enzyme directement, les chercheurs ont construit de vastes « cartes » du métabolisme — appelées modèles métaboliques à l’échelle du génome — pour 32 tissus distincts de la mouche. Ils ont combiné un réseau de réactions chimiques existant et validé avec des données d’expression génique en cellule unique, qui indiquent quels gènes métaboliques sont activés dans chaque tissu. Cela leur a permis de comparer combien de réactions, de métabolites et de gènes sont actifs dans chaque réseau tissulaire et de voir quelles voies sont mises en avant dans le muscle, le tissu adipeux, l’intestin et divers types de cellules nerveuses.
Des fonctions énergétiques distinctes selon les organes
La comparaison a révélé des « personnalités » métaboliques nettes selon les tissus. Le tissu adipeux et les oenocytes — homologues de la graisse et du foie humains chez la mouche — contenaient l’ensemble de réactions le plus riche, en particulier celles qui oxydent les graisses via la bêta-oxydation. Le muscle, en revanche, n’avait pas le plus grand réseau, mais possédait la plus forte proportion de réactions impliquées dans le transport de substances vers l’intérieur et l’extérieur des cellules, ce qui suggère que le muscle est un hub majeur d’échange de carburants et de blocs de construction avec le reste de l’organisme. Les scientifiques ont aussi vérifié si les voies prévues concordaient avec les profils de métabolites réels mesurés dans différentes régions du corps. Grâce à une métabolomique ciblée, ils ont analysé des centaines de petites molécules provenant des têtes, thorax, intestins et abdomens de mouches, puis ont testé si les voies enrichies dans les données se superposaient à celles prédites par les modèles. Dans le muscle et le tissu adipeux, la concordance était forte, ce qui renforce la confiance que les modèles tissulaires capturent une biologie réelle mieux que l’expression génique seule.
Ce que fait un régime riche en sucres au flux énergétique du muscle
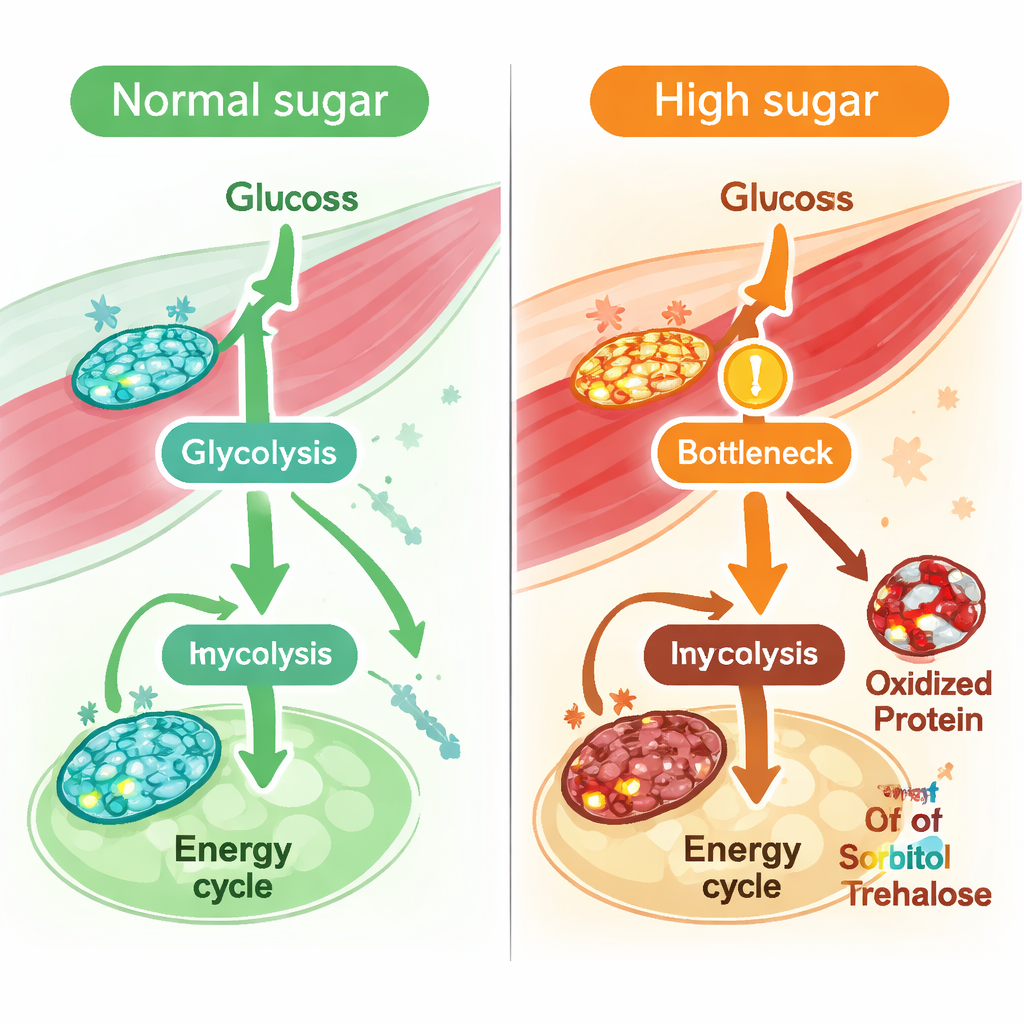
Avec un modèle musculaire validé, l’équipe a simulé ce qui se passe lorsque les mouches reçoivent un régime riche en sucres à long terme, un modèle bien établi du diabète de type 2. Ils ont contraint le modèle en utilisant des caractéristiques connues du muscle diabétique, comme une captation réduite du glucose et une activité ralentie du cycle énergétique central dans les mitochondries. Des analyses computationnelles de « flux » — calculs de la vitesse potentielle des réactions — ont montré de larges réductions des réactions dépendant du couple redox NAD/NADH, des molécules qui transportent des électrons et sont essentielles à la production d’énergie. En particulier, les réactions de la voie centrale d’oxydation du sucre, la glycolyse, ont ralenti, y compris celles catalysées par l’enzyme GAPDH. Le modèle a aussi prédit une diminution d’environ un quart de la capacité musculaire globale à produire du NADH, suggérant un déséquilibre redox sous tension. Des mesures directes dans le muscle thoracique des mouches ont confirmé que le ratio NAD/NADH diminuait bien sous régime riche en sucres.
Suivre le sucre marqué et les protéines oxydées
Pour vérifier si ces goulots d’étranglement prédits se produisaient réellement chez l’animal vivant, les chercheurs ont nourri les mouches avec un régime riche en sucres contenant du glucose uniformément marqué au carbone‑13, puis ont suivi où le carbone marqué se dirigeait. Ils ont constaté que les intermédiaires glycolytiques précoces en amont de la GAPDH s’accumulaient, tandis que les produits en aval et leurs fractions marquées diminuaient, signalant un vrai ralentissement à ce niveau et en aval. De même, les contributions du carbone du glucose au cycle énergétique central étaient réduites. Parallèlement, la protéomique redox — une méthode qui détecte les modifications oxydatives sur des acides aminés spécifiques des protéines — a montré une augmentation de l’oxydation de nombreuses enzymes glycolytiques, y compris à plusieurs sites sur la GAPDH. Dans l’ensemble de la glycolyse, les enzymes présentant davantage de modifications oxydatives montraient tendance à des chutes plus marquées des flux prédits, bien que leurs niveaux protéiques globaux soient restés majoritairement inchangés. Cela suggère que les dommages chimiques dus au stress oxydatif, plutôt que la perte d’abondance enzymatique, sont un moteur clé de l’altération du métabolisme des sucres dans le muscle.
Un problème caché dans la gestion du fructose et du saccharose
Au‑delà des réactions isolées, l’équipe a moyenné les flux sur des voies entières pour voir lesquelles étaient le plus perturbées par l’excès de sucre. La glycolyse, le cycle énergétique et la phosphorylation oxydative ont tous montré des déclins, mais l’une des diminutions les plus prononcées prévues concernait le métabolisme du fructose. Le profil métabolique du muscle soutenait cette idée : les niveaux de sorbitol et de tréhalose/saccharose augmentaient, et une enzyme clé qui convertit la tréhalose en glucose, la tréhalase, montrait à la fois une activité prédite réduite et une augmentation de l’oxydation sur un résidu de méthionine sensible. Ensemble, ces observations indiquent une perturbation plus large de la façon dont le muscle traite les sucres alimentaires — en particulier les carburants dérivés du fructose et du saccharose — lors d’une surcharge chronique en sucre.
Ce que cela signifie pour la compréhension du diabète
En termes simples, ce travail montre que trop de sucre n’entraîne pas seulement une surcharge du sang ; il reconfigure aussi silencieusement la façon dont les cellules musculaires dirigent et brûlent les carburants. En construisant des cartes métaboliques détaillées et tissulaires pour la mouche des fruits et en les recoupant avec la métabolomique, le traçage isotopique et la protéomique redox, les chercheurs montrent que l’excès de sucre induit un stress redox, oxyde des enzymes glycolytiques clés comme la GAPDH, ralentit la dégradation du sucre et perturbe les voies liées au fructose. Ces connaissances, obtenues dans un organisme modèle très manipulable, offrent un cadre puissant pour identifier quelles réactions et voies pourraient être prioritaires à protéger ou à restaurer dans le muscle humain afin de prévenir ou traiter le diabète de type 2.
Citation: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Mots-clés: Métabolisme de Drosophila, modèles métaboliques tissulaires, régime riche en sucres, glycolyse musculaire, régulation redox