Clear Sky Science · fr
OCT4 améliore l’efficacité d’initiation des origines de réplication tardive dans les cellules souches embryonnaires de souris
Pourquoi cela compte pour nos cellules
Chaque fois qu’une cellule se divise, elle doit copier l’intégralité de son ADN avec précision et dans les délais. Si ce processus de copie échoue, il peut entraîner des problèmes de développement ou des maladies, y compris le cancer. Cette étude examine comment une protéine clé des cellules souches, OCT4, aide à organiser le moment et le lieu où la copie de l’ADN commence dans les cellules souches embryonnaires de souris — offrant un aperçu de la manière dont les premiers embryons préservent la stabilité de leur génome tout en se divisant à grande vitesse.
Cartographier quand l’ADN est copié
Les auteurs se concentrent sur le « timing de réplication » — l’ordre selon lequel différentes parties du génome sont dupliquées pendant la phase S du cycle cellulaire. Le génome est divisé en larges voisinages, ou domaines temporels, qui sont copiés tôt, au milieu ou tard pendant la phase S. En utilisant des méthodes de séquençage à haut débit qui marquent l’ADN nouvellement synthétisé, l’équipe a dressé la carte du paysage de timing de réplication des cellules souches embryonnaires de souris et l’a comparée à celui de types cellulaires plus matures, comme les fibroblastes et les cellules souches mésenchymateuses. Ils ont identifié des milliers de « zones d’initiation », des segments d’ADN où la réplication débute réellement, et les ont classées comme précoces, moyennes ou tardives en fonction du domaine temporel auquel elles appartiennent.
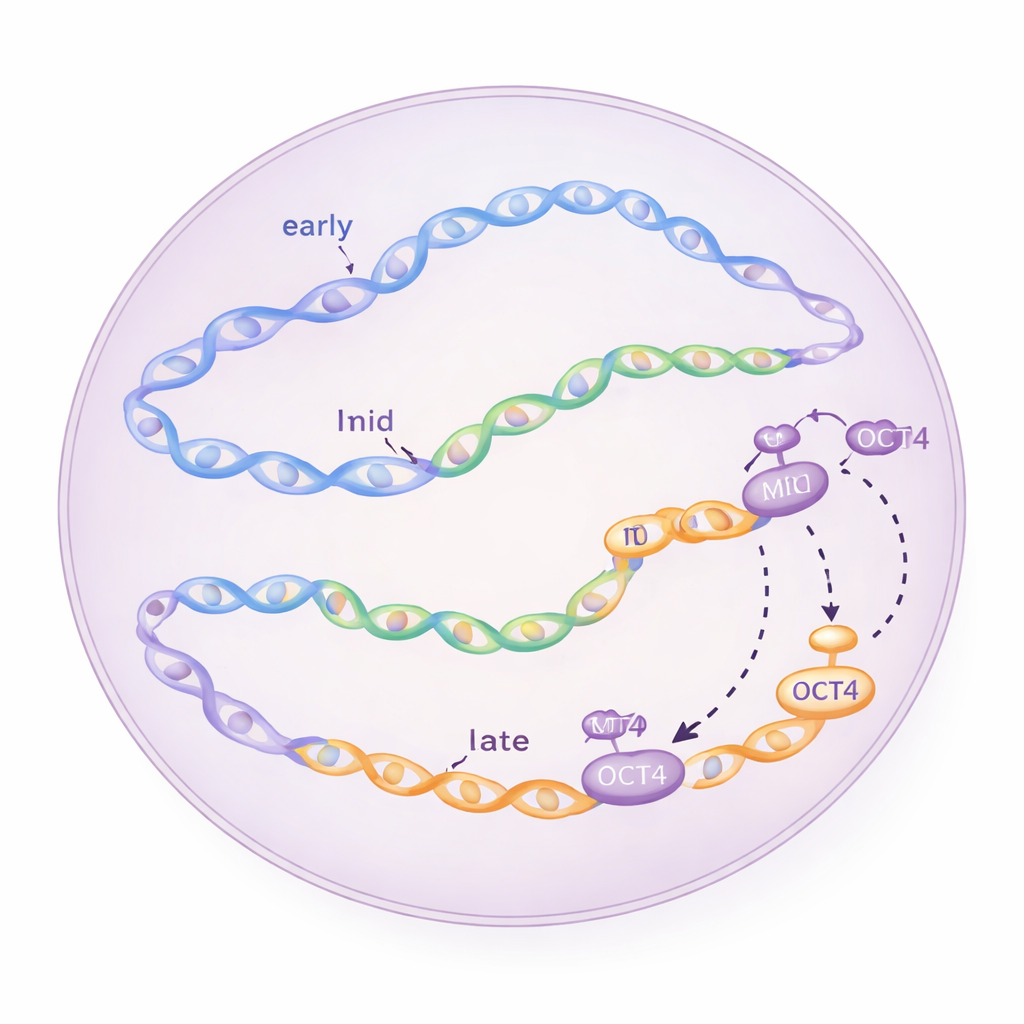
Des zones tardives qui « passent devant »
La sagesse conventionnelle veut que les régions programmées pour une réplication tardive attendent majoritairement la fin de la phase S pour commencer à être copiées. De manière surprenante, dans les cellules souches embryonnaires, les chercheurs ont observé que certaines zones d’initiation situées dans des domaines tardifs commençaient à s’activer très peu après le début de la phase S — en l’espace d’une à deux heures. En synchronisant les cellules à différents stades du cycle cellulaire et en prenant à plusieurs reprises des instantanés de l’ADN nouvellement synthétisé, ils ont confirmé que ces zones « tardives » s’allument réellement tôt et que leur activité dépend des régulateurs du cycle cellulaire habituels comme les kinases CDC7 et CDK1, ainsi que de la voie de contrôle ATR, qui aide normalement à éviter la surcharge du dispositif de réplication.
Voisinages d’ADN ouverts et rôle d’OCT4
Pour comprendre ce qui rend ces régions tardives à activation précoce particulières, l’équipe a examiné leur environnement local. Ils ont superposé les cartes de réplication avec des données sur la production d’ARN et les marques de chromatine — des étiquettes chimiques et des caractéristiques structurales indiquant si l’ADN est dans un état ouvert et accessible ou compacté. Les zones d’initiation précoces avaient tendance à se situer près de gènes actifs et de chromatine ouverte, tandis que les zones tardives se trouvaient plus souvent dans des régions réprimées et fortement compactées. Pourtant, les zones tardives qui s’activaient tôt dans les cellules souches embryonnaires présentaient des signatures d’ouverture : elles coïncidaient avec de la chromatine accessible, des éléments ressemblant à des enhancers et des sites de liaison pour des facteurs de pluripotence tels qu’OCT4, SOX2, NANOG et KLF4. Cela suggère que les mêmes protéines qui maintiennent la plasticité des cellules souches pourraient aussi préparer certaines régions tardives du génome à une réplication plus précoce.
Éteindre OCT4 modifie le calendrier
Les auteurs ont ensuite mis cette idée à l’épreuve en utilisant une lignée de cellules souches spéciale dans laquelle les niveaux d’OCT4 peuvent être rapidement réduits par l’ajout de la doxycycline. Lorsque OCT4 a été épuisé pendant une partie d’un seul cycle cellulaire, la progression globale vers la phase S est restée en grande partie inchangée, mais l’initiation de nombreuses zones d’initiation moyennes et tardives a été affaiblie ou retardée. Des analyses à l’échelle du génome ont montré que, dans les régions où OCT4 se lie normalement, à la fois l’accessibilité de la chromatine et les signaux d’initiation de la réplication diminuaient en parallèle lorsque OCT4 était éteint. Des modèles statistiques ont confirmé que cet effet était le plus marqué dans les zones à réplication tardive : plus une zone d’initiation dépendait d’OCT4 pour maintenir une chromatine ouverte, plus son efficacité de réplication pâtissait en l’absence d’OCT4.
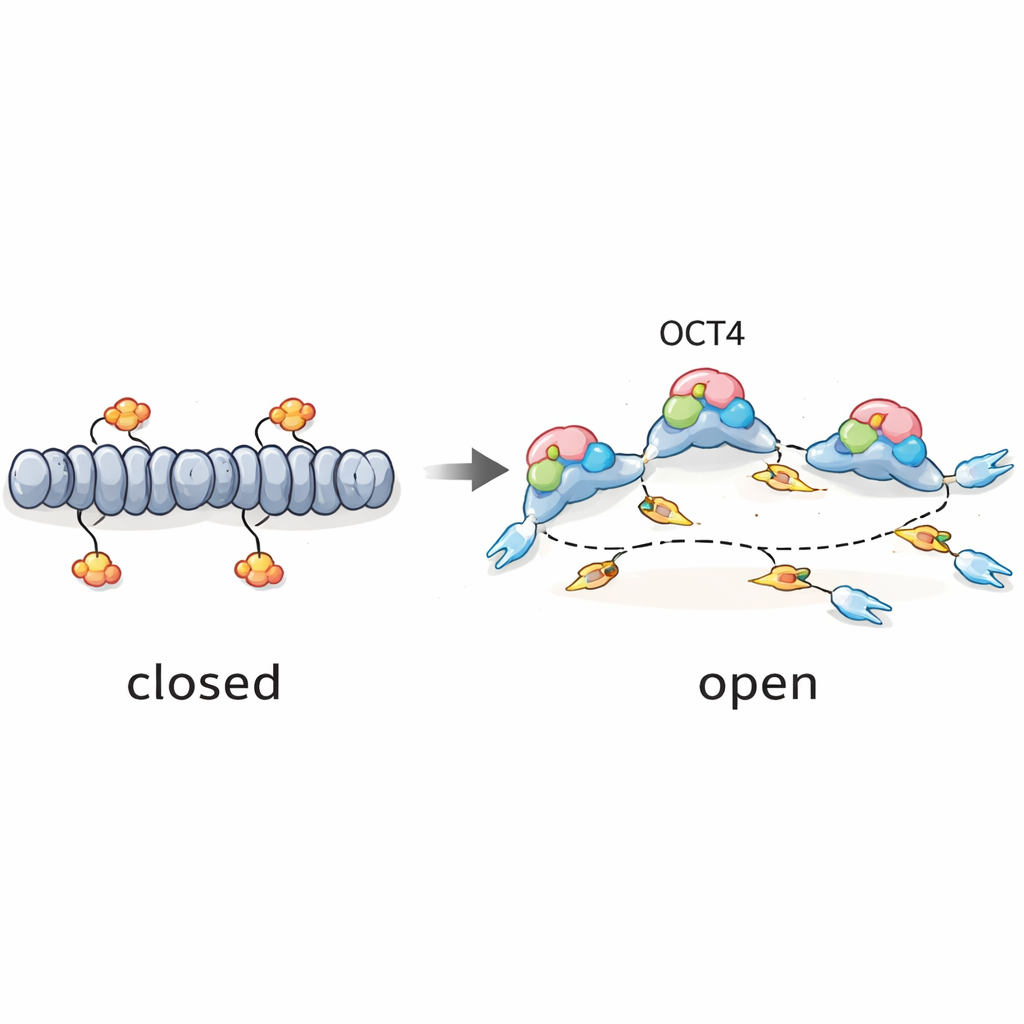
Un facteur « pionnier » qui règle aussi la temporalité de la copie de l’ADN
Pris ensemble, les résultats soutiennent une idée simple : OCT4 agit comme un facteur « pionnier » non seulement pour l’activité génique, mais aussi pour la réplication de l’ADN. En ouvrant des régions tardives spécifiques du génome dans les cellules souches embryonnaires, OCT4 crée des points de départ efficaces pour la copie de l’ADN qui peuvent s’activer plus tôt et de manière plus fiable qu’ils ne le feraient dans des cellules différenciées. Parallèlement, des régulateurs globaux tels qu’ATR, CDC7 et CDK1 ajustent le nombre de ces sites autorisés à s’activer, empêchant le système de réplication d’être submergé. Pour un lectorat non spécialiste, le message clé est que les mêmes protéines qui préservent la polyvalence des cellules souches contribuent aussi à orchestrer le moment où différentes parties de leur ADN sont copiées, ajoutant une couche supplémentaire à notre compréhension de la façon dont les cellules embryonnaires à division rapide maintiennent l’ordre dans leurs génomes.
Citation: Rodriguez-Carballo, E., Dionellis, V.S., Ntallis, S.G. et al. OCT4 enhances the firing efficiency of late DNA replication origins in mouse embryonic stem cells. Nat Commun 17, 1686 (2026). https://doi.org/10.1038/s41467-026-68389-1
Mots-clés: timing de la réplication de l’ADN, cellules souches embryonnaires, OCT4, accessibilité de la chromatine, déclenchement des origines