Clear Sky Science · fr
Rajeunissement mécanique des cellules souches sénescentes et de l’os âgé via le remodelage de la chromatine
Pourquoi il est important de garder les os jeunes
En vieillissant, nos os perdent progressivement en solidité : ils s’amincissent et deviennent plus fragiles. Cela augmente le risque de fractures, la perte d’autonomie et les douleurs chroniques. La plupart des traitements actuels visent à ralentir la dégradation osseuse ou à renforcer la minéralisation, mais ils ne réparent pas directement le vieillissement des cellules souches qui construisent l’os. Cette étude explore une approche différente : utiliser des forces physiques contrôlées — plutôt que des médicaments — pour « rajeunir » les cellules souches formatrices d’os et améliorer la santé osseuse et la condition physique chez des souris âgées.
Quand les bâtisseurs de l’os vieillissent
Au cœur de nos os résident les cellules souches mésenchymateuses de la moelle osseuse, des constructeurs maîtres capables de devenir des cellules formatrices d’os. Avec l’âge, ces cellules se divisent moins, fabriquent moins d’os et présentent des signes classiques du vieillissement cellulaire, tels que des dommages à l’ADN et des signaux inflammatoires. Les auteurs ont comparé des cellules provenant de donneurs humains jeunes et âgés et ont constaté que les cellules âgées n’étaient pas seulement différentes biochimiquement : elles étaient mécaniquement affaiblies. Elles exerçaient moins de forces internes, avaient un échafaudage interne plus lâche et transmettaient moins efficacement les signaux mécaniques vers le noyau. Dans le tissu osseux de souris âgées, un déclin similaire apparaissait : le réseau d’os spongieux s’était aminci, des protéines clés de la signalisation mécanique étaient réduites et des marqueurs du vieillissement étaient élevés.
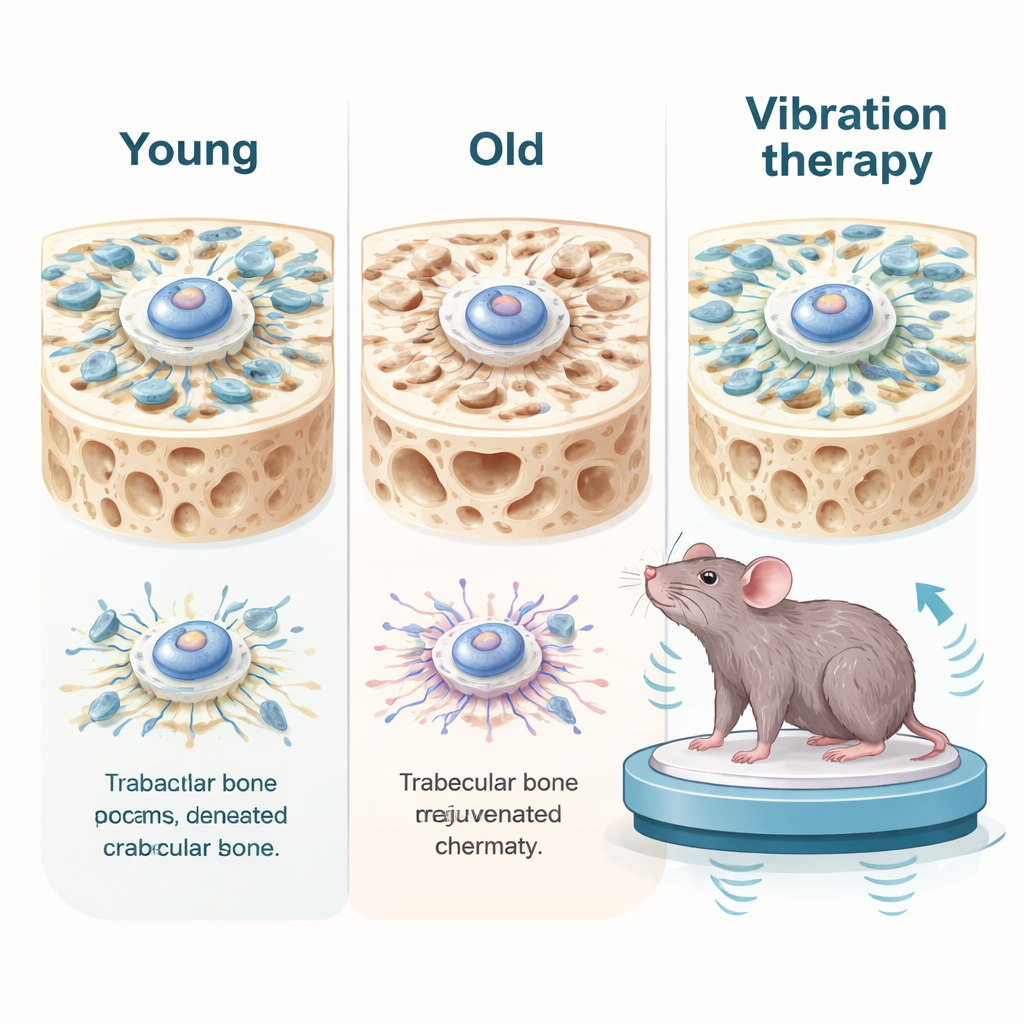
Tirer doucement les cellules vers la jeunesse
L’équipe a ensuite cherché à savoir si la restauration des forces mécaniques pouvait inverser ces traits de vieillissement. En culture, ils ont appliqué un léger étirement aux cellules souches sénescentes ou utilisé un médicament qui augmente l’activité des moteurs moléculaires. Ces traitements ont renforcé les forces de traction cellulaires et amélioré l’organisation du cytosquelette. Remarquablement, les cellules âgées ont commencé à paraître et à se comporter comme plus jeunes : les marqueurs de sénescence ont diminué, les dommages à l’ADN se sont atténués et la prolifération cellulaire s’est accrue. L’inverse était également vrai : lorsqu’ils ont assoupli l’environnement sous des cellules jeunes ou affaibli chimiquement leur machinerie contractile, les cellules sont entrées dans un état apparent de vieillissement, ralentissant et activant des marqueurs de sénescence, même dans un gel 3D mimant l’os.
Comment la force dialogue avec les gènes
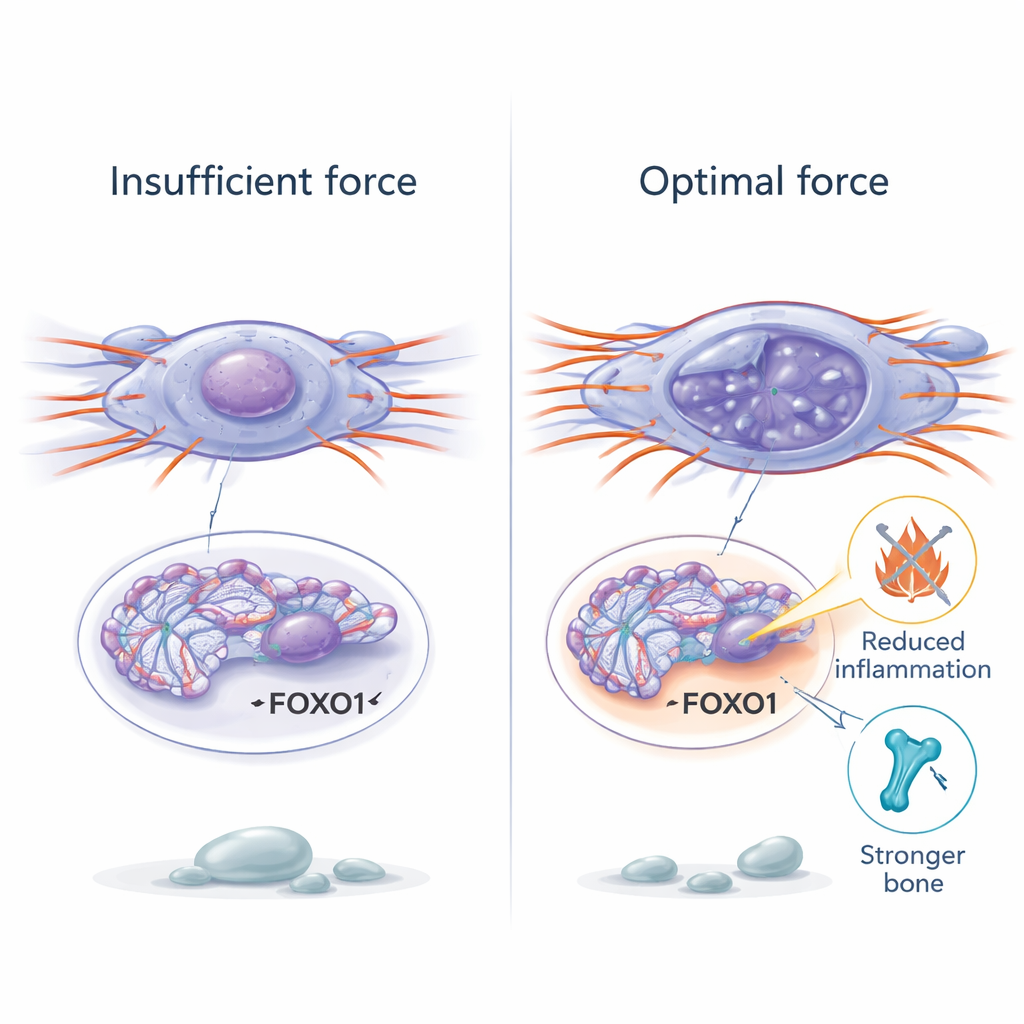
Pour comprendre comment des forces physiques pouvaient modifier aussi profondément le comportement cellulaire, les chercheurs se sont intéressés à la chromatine — la forme compactée de l’ADN à l’intérieur du noyau. Dans les cellules souches âgées, la chromatine était plus condensée et moins accessible, rendant plus difficile l’activation de gènes bénéfiques. La restauration de la force mécanique a provoqué une relaxation locale de la chromatine, augmentant des marques chimiques associées à un ADN ouvert et actif. À l’aide d’un test génomique d’accessibilité de la chromatine, l’équipe a montré qu’une stimulation mécanique douce ouvrait des régions situées près de gènes impliqués dans le contrôle du vieillissement. Un gène, appelé FOXO1, s’est distingué par sa sensibilité particulière à la force : lorsque la force augmentait, la région d’ADN de FOXO1 devenait plus accessible, son activité augmentait et les cellules perdaient des signes de sénescence. Bloquer FOXO1 annulait les bénéfices de la stimulation mécanique, révélant son rôle de relais clé qui relie la contrainte physique aux programmes génétiques de résilience et de réparation.
Trouver le juste équilibre de la thérapie mécanique
Les chercheurs ont ensuite testé la stimulation mécanique chez des souris vivantes. Des animaux âgés ont été placés sur une plateforme à vibration de faible intensité pour de courtes séances quotidiennes pendant un mois, tandis que d’autres ont vu leurs pattes arrière déschargées par suspension par la queue, mimant une inactivité extrême. Chez les souris âgées, une vibration douce a renforcé la signalisation mécanique dans l’os, réduit les marqueurs de vieillissement et d’inflammation et partiellement reconstruit le réseau d’os spongieux. Elle a aussi amélioré la force de préhension, l’endurance à l’exercice, des tâches liées à la mémoire et a abaissé l’inflammation dans le sang, le foie et les reins. Cependant, lorsque la vibration était appliquée en continu sans jours de repos, les bénéfices disparaissaient et s’inversaient : la structure osseuse se dégradait, les dommages à l’ADN augmentaient et l’inflammation s’élevait. En culture cellulaire, un étirement excessif ou trop fréquent provoquait des cassures d’ADN et repoussait les cellules vers la sénescence, montrant que la force mécanique peut guérir ou nuire selon la dose.
Des simulateurs d’exercice aux traitements futurs
Pour un lecteur non spécialiste, le message central est que nos cellules ne répondent pas seulement aux hormones et aux substances chimiques : elles « écoutent » aussi attentivement les forces physiques. Dans ce travail, les auteurs montrent qu’une stimulation mécanique modérée et bien réglée peut réveiller des cellules souches osseuses âgées, ouvrir des programmes géniques protecteurs tels que FOXO1, reconstruire un os affaibli et calmer l’inflammation chronique chez des souris âgées. En même temps, trop peu ou trop de contrainte accélère l’usure cellulaire. Ces résultats laissent entrevoir que des thérapies mécaniques soigneusement conçues — peut-être des régimes d’exercice spécifiques ou des dispositifs vibratoires sûrs — pourraient un jour compléter les médicaments pour maintenir les os, et possiblement d’autres tissus, en meilleure santé plus longtemps.
Citation: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Mots-clés: vieillissement osseux, stimulation mécanique, rajeunissement des cellules souches, remodelage de la chromatine, FOXO1