Clear Sky Science · fr
Hydrolyse catalytique efficace et stable des perfluorocarbures rendue possible par un apport de protons médié par SO2
Pourquoi ce gaz à effet de serre tenace compte
Certaines gaz industriels sont si stables qu’une fois libérés, ils persistent dans l’atmosphère pendant des dizaines de milliers d’années. Le tétrafluorométhane (CF4), un type de perfluorocarbone utilisé et émis lors de la production d’aluminium et de la fabrication de puces, est l’un des pires coupables : il piège la chaleur environ 7 400 fois plus efficacement que le dioxyde de carbone. Cette étude explore une nouvelle manière de décomposer le CF4 de façon efficace et fiable, transformant un polluant presque indestructible en produits plus sûrs dans des conditions réalistes pour les usines.
Une molécule coriace qui refuse de se casser
Le CF4 appartient à la grande famille des PFAS, des substances reconnues pour leur persistance dans l’environnement. Ce qui rend le CF4 particulièrement difficile, ce sont ses liaisons carbone–fluor extrêmement fortes et sa très longue durée de vie atmosphérique, estimée à plus de 50 000 ans. Les méthodes traditionnelles pour détruire le CF4 requièrent des températures très élevées et entraînent souvent une usure rapide et une perte d’activité des catalyseurs qui pilotent la réaction. Pourtant, de nouvelles politiques climatiques, comme le mécanisme d’ajustement carbone aux frontières de l’Union européenne, exercent une pression croissante sur les industries lourdes pour réduire ces émissions sans augmenter fortement leur consommation d’énergie.
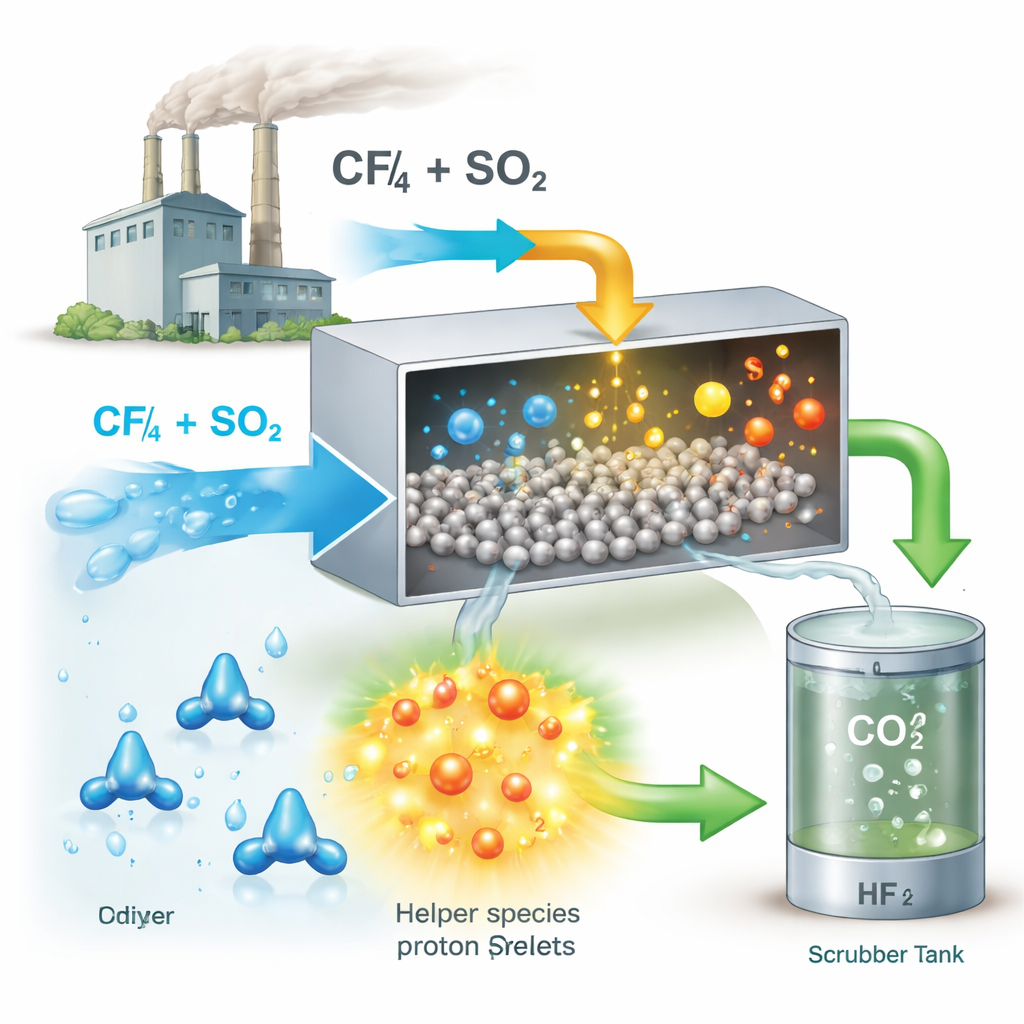
Transformer un polluant courant en aide
De manière surprenante, les chercheurs ont découvert qu’un autre polluant bien connu, le dioxyde de soufre (SO2), peut être utilisé pour résoudre le problème du CF4. Le SO2 est fréquemment émis en même temps que le CF4 lors de la production d’aluminium. Alors que le SO2 nuit habituellement aux catalyseurs en s’adsorbant sur leurs surfaces, l’équipe a montré que, dans des conditions appropriées, il peut produire l’effet inverse : il reconfigure la surface du catalyseur de sorte que l’eau se dissocie plus facilement et fournisse davantage d’ions hydrogène réactifs (protons). Ces protons sont essentiels pour affaiblir les liaisons tenaces du CF4 et pour débarrasser le catalyseur du fluor afin qu’il conserve son activité.
Construire des « stations d’alimentation » en protons à la surface
L’avancée clé est la création de sites riches en protons directement sur le catalyseur, qui est à base d’oxyde d’aluminium dopé au gallium. Lorsque du SO2, de la vapeur d’eau et du CF4 circulent sur ce matériau à haute température, le SO2 se transforme en groupes acides fortement liés à la surface. Deux familles de ces groupes apparaissent : l’une principalement attachée à l’aluminium (Al–HSO4) et l’autre au gallium (Ga–HS). À l’aide d’outils spectroscopiques sensibles et de simulations informatiques, les auteurs montrent que les groupes liés à l’aluminium attirent le CF4 et favorisent la scission de l’eau pour libérer des protons, tandis que les groupes liés au gallium utilisent ces protons pour enlever le fluor des sites empoisonnés et le libérer sous forme d’acide fluhydrique, restaurant ainsi l’activité du catalyseur.
Performance record en conditions réelles
Parce que ces « stations d’alimentation » en protons sont fortement ancrées et restent stables à haute température, elles fournissent des hydrogènes réactifs bien plus efficacement que les additifs traditionnels. L’étude montre que l’activation de l’eau est augmentée d’environ six fois et que la disponibilité en protons est multipliée par près de dix par rapport à un fonctionnement sans SO2. En conséquence, la décomposition complète du CF4 est obtenue à 550 °C au lieu des 700 °C habituels, réduisant ainsi la demande énergétique du procédé. Autre point important : le catalyseur fonctionne pendant plus de 2 500 heures — plus de trois mois de fonctionnement continu — sans perte de performance notable, et il opère sur une large plage de niveaux de SO2 correspondant à ceux des flux d’échappement industriels.
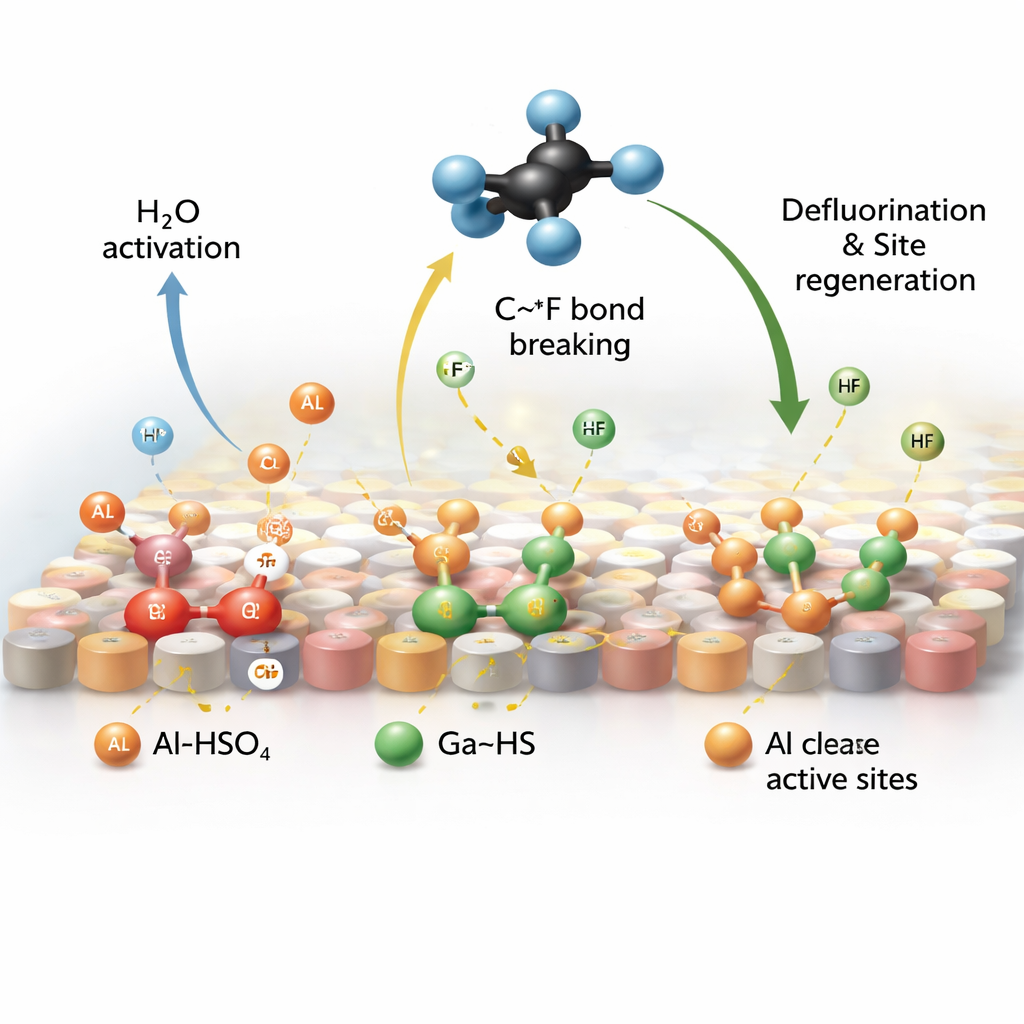
Une nouvelle voie pour nettoyer les polluants atmosphériques persistants
Pour un non-spécialiste, le résultat peut se résumer ainsi : enseigner un nouveau tour à un catalyseur — utiliser un gaz indésirable (SO2) pour construire de minuscules sites acides robustes qui lui fournissent les protons nécessaires pour attaquer l’un des gaz à effet de serre les plus résistants connus. En facilitant à la fois la destruction du CF4 et la longévité du catalyseur, cette stratégie ouvre la voie à des épurateurs pratiques qui pourraient être ajoutés aux cheminées des usines d’aluminium et des sites de semi-conducteurs. Plus généralement, le même concept de régulation locale des protons pourrait être adapté pour démanteler d’autres PFAS en phase gazeuse, offrant un outil prometteur pour réduire l’impact climatique et environnemental à long terme des industries de pointe.
Citation: Zhang, H., Luo, T., Chen, Y. et al. Efficient and stable catalytic hydrolysis of perfluorocarbon enabled by SO2-mediated proton supply. Nat Commun 17, 597 (2026). https://doi.org/10.1038/s41467-026-68386-4
Mots-clés: tétrafluorométhane, destruction des PFAS, hydrolyse catalytique, promotion par dioxyde de soufre, contrôle des émissions industrielles