Clear Sky Science · fr
Excision précise des répétitions GGC étendues dans NOTCH2NLC par CRISPR/Cas9 pour traiter la maladie à inclusions intranucléaires neuronales
Éditer l’ADN pour combattre un trouble cérébral mystérieux
La maladie à inclusions intranucléaires neuronales (MIIN) est un trouble cérébral rare mais dévastateur pouvant provoquer démence, troubles moteurs et, parfois, un décès précoce. Il n’existe aujourd’hui aucun remède. Cette étude examine si un outil puissant d’édition génétique, CRISPR, peut être utilisé pour exciser un court mais toxique fragment d’ADN responsable de la MIIN, offrant un aperçu de la façon dont de futurs traitements pourraient réécrire nos gènes pour lutter contre les maladies cérébrales. 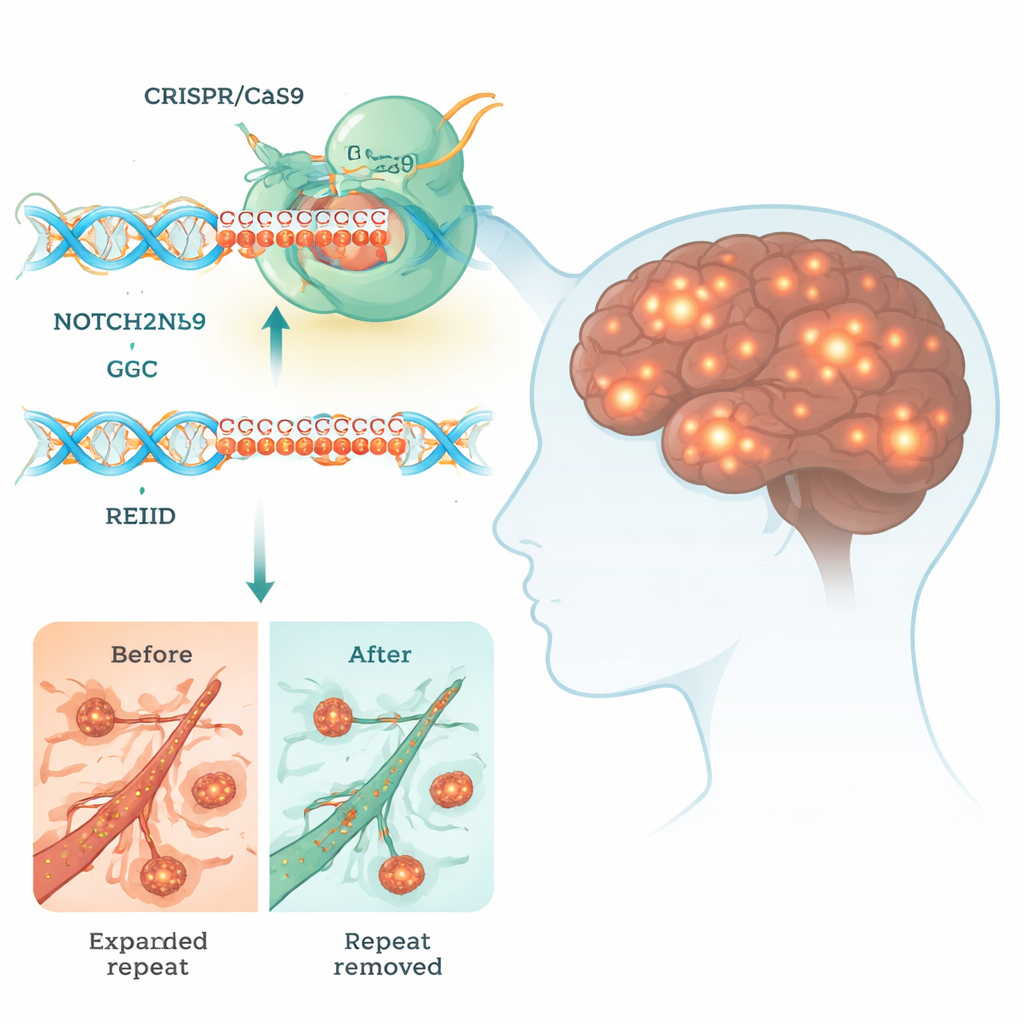
Un coupable génétique caché
De nombreuses maladies cérébrales héréditaires sont causées par de courtes séquences d’ADN qui se sont étendues bien au-delà de leur longueur normale. Dans la MIIN, le problème est une course excessive d’unités d’ADN de trois lettres, « GGC », dans un gène appelé NOTCH2NLC. Bien que cette séquence se situe dans une région qui ne code pas directement pour une protéine classique, elle peut néanmoins être lue par la machinerie cellulaire pour produire des chaînes anormales de polyglycine (polyG). Ces chaînes adhésives s’agglomèrent en amas à l’intérieur du noyau des cellules nerveuses et d’autres tissus, perturbant des processus vitaux tels que la production d’énergie, le traitement de l’ARN et le trafic de molécules entre le noyau et le cytoplasme.
Le défi d’une chirurgie génétique précise
Concevoir un traitement d’édition génique pour la MIIN est particulièrement difficile parce que NOTCH2NLC possède plusieurs gènes sœurs presque identiques qui sont importants pour le développement cérébral humain. Si CRISPR coupe le mauvais gène, cela pourrait faire plus de mal que de bien. Les chercheurs ont soigneusement analysé l’ADN autour de la répétition GGC et trouvé de petites différences de séquence qui distinguent NOTCH2NLC de ses proches. Ils ont ensuite conçu des paires d’ARN guides CRISPR qui dirigent les « ciseaux moléculaires » Cas9 pour couper juste avant et juste après la répétition étendue. Cette stratégie à double coupe permet au système de réparation de la cellule d’éliminer le segment toxique tout en laissant le reste de la famille de gènes intact.
Des cellules en culture aux neurones dérivés de patients
L’équipe a d’abord testé leur conception CRISPR dans des cellules humaines standard et dans des cellules modifiées pour porter une longue répétition de NOTCH2NLC. Dans ces modèles, l’outil a efficacement éliminé la répétition, et les niveaux d’amas de polyG ont diminué d’environ la moitié ou plus. Ils sont ensuite passés à des cellules souches pluripotentes induites (iPSC) dérivées d’un patient atteint de MIIN et ont converti ces cellules en progéniteurs neuronaux, un stade précoce des cellules cérébrales. En utilisant CRISPR, ils ont soit supprimé la répétition étendue, soit remplacé celle-ci par une version de longueur normale. Le séquençage détaillé de l’ADN et du génome entier a montré que l’édition était très précise, avec peu de preuves de coupures indésirables, et les cellules éditées se divisaient et mûrissaient normalement. 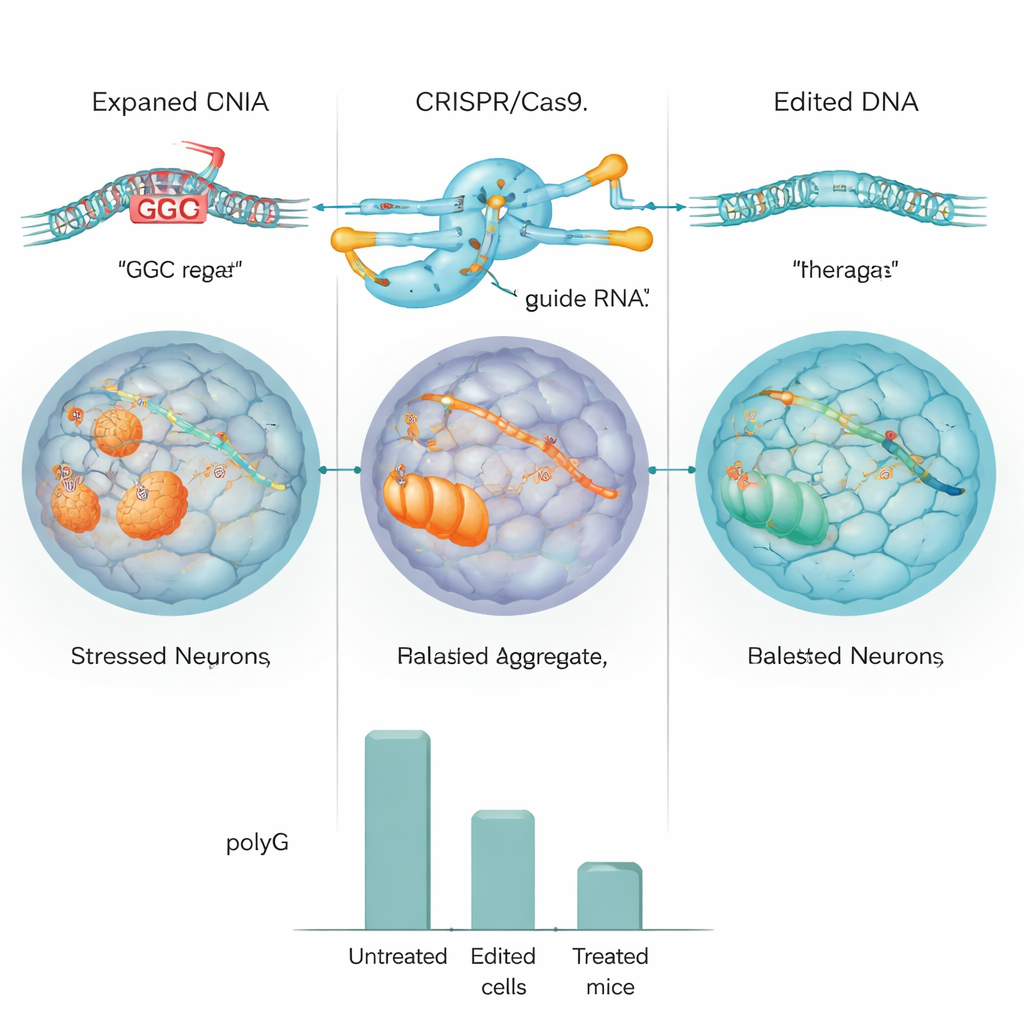
Rétablir fonction cérébrale et organique chez une souris modèle
Pour savoir si cette approche pouvait réellement améliorer la maladie, les chercheurs ont utilisé des souris conçues pour porter la répétition humaine de NOTCH2NLC et développer des caractéristiques semblables à la MIIN, y compris des inclusions nucléaires, des troubles moteurs et une durée de vie réduite. Ils ont emballé le système CRISPR dans un virus modifié capable de se répandre dans tout le cerveau après une simple injection dans le sang chez des souriceaux nouveau-nés. Chez les animaux traités, la répétition étendue a été retirée avec succès dans les tissus cérébraux. En conséquence, les niveaux toxiques de polyG ont fortement chuté, les marqueurs de santé des neurones se sont améliorés et l’activation anormale des cellules de soutien du cerveau s’est atténuée. Les tests comportementaux ont montré que les souris traitées bougeaient davantage, gardaient mieux l’équilibre et vivaient plus longtemps que leurs congénères non traitées. Des bénéfices similaires ont été observés au niveau cardiaque, qui accumule également du polyG dans ce modèle.
Ce que cela pourrait signifier pour de futurs traitements
Pour un non-spécialiste, le message principal est que la MIIN semble être largement provoquée par une seule répétition d’ADN spécifiquement élargie, et que l’excision précise de cette répétition peut inverser de nombreux signes de la maladie dans des cellules et chez la souris. Ce travail ne se traduit pas encore par une thérapie prête à l’emploi pour l’humain : les chercheurs doivent encore affiner la sécurité à long terme, améliorer les méthodes de délivrance et tester dans des animaux plus grands et plus proches de l’humain. Mais l’étude offre une preuve de concept solide que l’édition génique ciblée avec précaution peut neutraliser une répétition toxique tout en épargnant des gènes étroitement apparentés. Cette stratégie pourrait un jour être adaptée non seulement à la MIIN, mais aussi à d’autres maladies cérébrales et musculaires causées par des expansions de répétitions similaires.
Citation: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Mots-clés: édition génétique CRISPR, maladie à inclusions intranucléaires neuronales, affections liées à l'expansion de répétitions, NOTCH2NLC, neurodégénérescence