Clear Sky Science · fr
Conception par IA générative basée sur les séquences de synthases de tryptophane polyvalentes
Apprendre de nouveaux tours aux enzymes grâce à l’IA
La société moderne fonctionne grâce à des molécules — médicaments, matériaux et produits chimiques spécialisés — souvent fabriquées par des procédés gourmands en énergie et polluants. Les catalyseurs de la nature, les enzymes, peuvent accomplir des tâches similaires de façon propre et efficace, mais trouver ou construire l’enzyme adaptée à une nouvelle application industrielle est lent et incertain. Cette étude montre que l’intelligence artificielle générative, la même famille de technologies derrière les chatbots qui rédigent du texte, peut être utilisée pour concevoir des enzymes entièrement nouvelles qui non seulement fonctionnent bien au laboratoire, mais surpassent parfois les meilleurs résultats obtenus par l’évolution naturelle et des années d’ingénierie.
Pourquoi les enzymes comptent au quotidien
Les enzymes sont de petites machines protéiques qui accélèrent les réactions chimiques dans les cellules vivantes. Les chimistes ont appris à les réutiliser pour fabriquer des médicaments, des ingrédients alimentaires et d’autres produits de valeur en utilisant moins d’énergie et moins de réactifs toxiques que la chimie conventionnelle. Le problème est que chaque nouvelle application demande généralement une enzyme aux performances bien précises — capable d’accepter des matières premières particulières, de résister aux conditions de transformation et de produire de hauts rendements. L’« évolution dirigée » conventionnelle améliore les enzymes en créant et testant de nombreuses versions mutées, génération après génération. Cela fonctionne bien mais dépend d’une enzyme de départ convenable et peut prendre des mois voire des années d’essais et d’erreurs, laissant de nombreuses réactions intéressantes inexplorées.
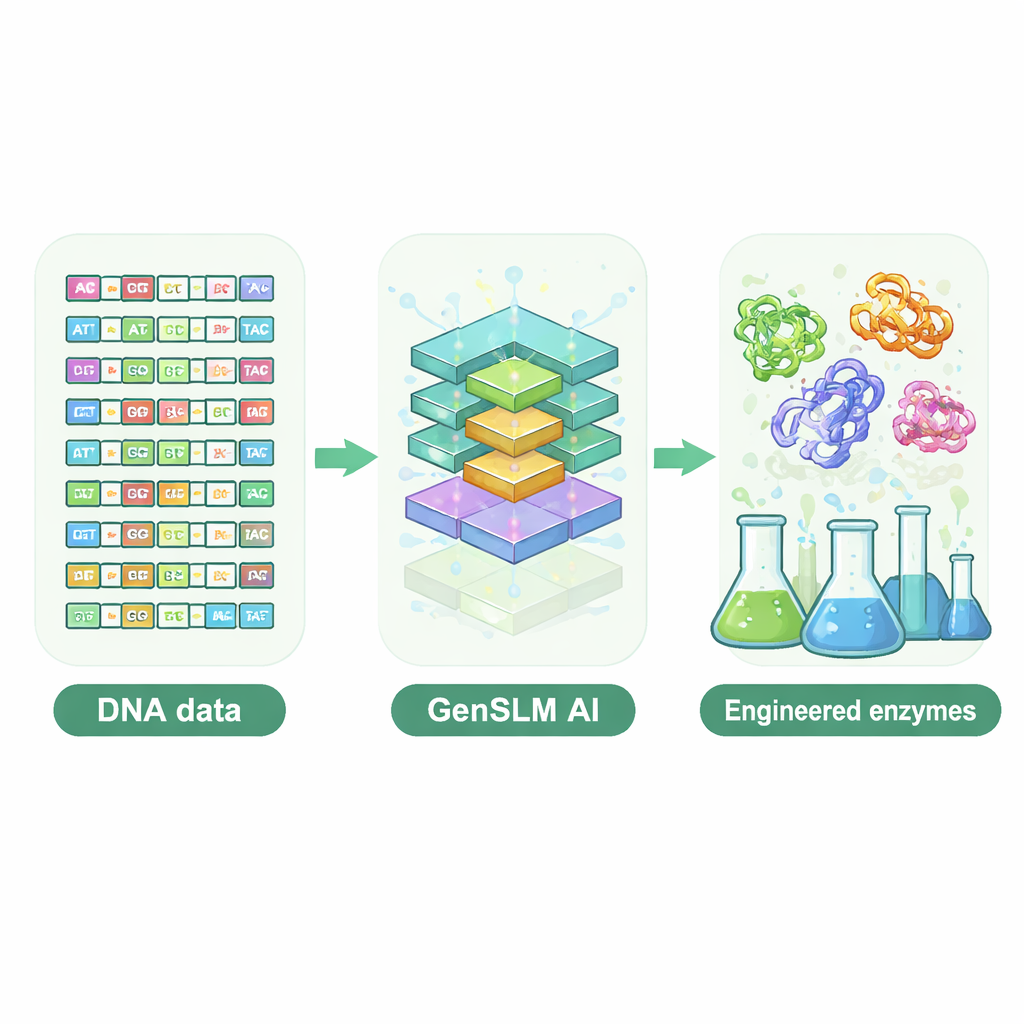
Laisser un modèle de langage écrire de l’ADN
Les chercheurs se sont tournés vers un modèle de langage à l’échelle génomique appelé GenSLM, qui apprend les motifs de l’ADN de la même manière qu’un modèle de langage apprend la grammaire et le style d’un texte. Plutôt que de travailler avec des séquences protéiques finales, GenSLM lit et écrit l’ADN en codons de trois lettres, reflétant la façon dont les cellules traduisent les gènes en protéines. L’équipe a d’abord affiné GenSLM sur des dizaines de milliers de gènes naturels pour une sous‑unité enzymatique particulièrement complexe, appelée TrpB, qui aide à construire l’acide aminé tryptophane. Ils ont ensuite demandé au modèle de générer des milliers de gènes trpB entièrement nouveaux. Des filtres computationnels simples ont écarté les séquences trop courtes ou trop longues, peu susceptibles de se replier correctement, ou presque identiques à des enzymes naturelles connues, laissant 105 candidats divers pour des tests expérimentaux en bactéries.
Des conceptions informatiques à des catalyseurs fonctionnels
Lorsque ces 105 enzymes TrpB conçues par l’IA ont été produites dans E. coli, beaucoup se sont repliées correctement et ont été exprimées en grande quantité. Des dizaines ont pu accomplir leur tâche principale : convertir l’indole et l’acide aminé partenaire naturel, la sérine, en tryptophane. Certaines ont bien fonctionné même à des températures élevées, malgré l’absence de conception explicite pour la résistance thermique. Lors de tests comparatifs, un sous‑ensemble de GenSLM‑TrpB a égalé ou surpassé une enzyme de référence qui avait été patiemment évoluée en laboratoire pendant des années pour fonctionner seule à 75 °C. Une conception remarquable, baptisée 230, a produit plus de tryptophane que cette référence industrielle à la fois à température ambiante et à haute température, montrant qu’un modèle entraîné uniquement sur des données de séquence peut atteindre directement des performances de haut niveau.
Une nouvelle flexibilité au‑delà de ce que la nature a produit
L’équipe a ensuite mis les enzymes au défi avec un panel de substrats non naturels — dérivés de l’indole, un partenaire de type alcool différent et un composé fluoré utilisé dans la fabrication pharmaceutique. Les versions naturelles de TrpB sont généralement exigeantes : elles favorisent fortement leurs substrats natifs et montrent peu d’activité sur de telles alternatives. De manière remarquable, les enzymes générées par l’IA ont souvent été plus aventureuses. Pour chaque substrat non naturel testé, au moins une conception GenSLM a montré une activité mesurable, et beaucoup ont fait mieux que les enzymes naturelles. Là encore, le variant 230 s’est démarqué, convertissant les sept substrats alternatifs avec des rendements allant de modestes à quasi complets, une étendue de « promiscuité » jamais observée auparavant dans cette famille d’enzymes. Pour autant, lorsque les chercheurs ont comparé 230 à son parent naturel le plus proche — ne différant que par 78 positions d’acides aminés sur 400 — ils ont constaté que l’enzyme naturelle manquait de cette polyvalence bien que sa structure globale et les résidus clés du site actif soient presque identiques.
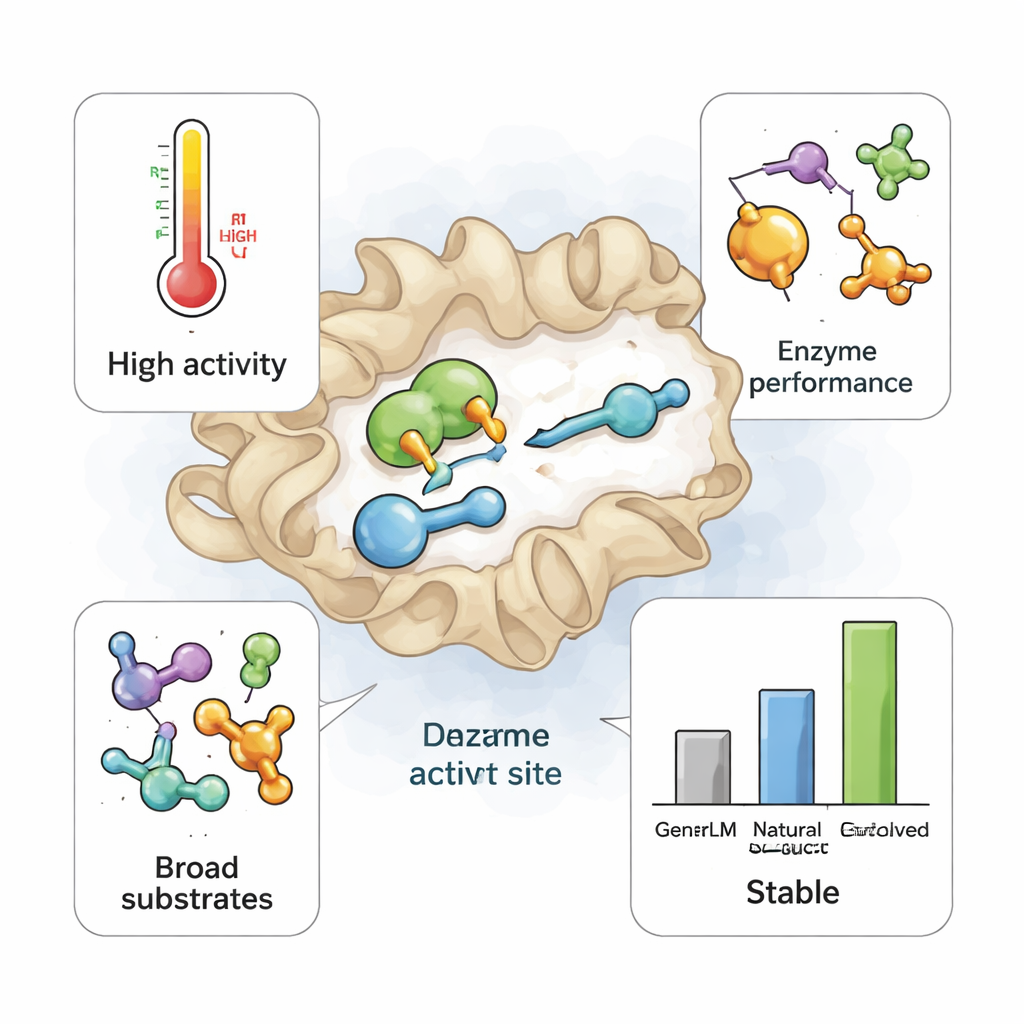
Ce que cela signifie pour la chimie verte à venir
Pour un non‑spécialiste, le message essentiel est qu’un modèle d’IA entraîné uniquement sur des séquences d’ADN existantes peut imaginer de nouvelles enzymes réalistes que la nature n’a jamais testées, dont certaines sont de meilleurs outils pour la chimie que celles que nous utilisons aujourd’hui. Ces variants de TrpB conçus par l’IA conservent la forme et la fonction essentielles de leurs homologues naturels tout en acquérant une capacité inhabituelle à traiter de nombreux matériaux de départ différents. Cette flexibilité pourrait réduire considérablement le travail de laboratoire nécessaire pour découvrir des voies enzymatiques vers de nouveaux médicaments et autres produits. À mesure que la conception, la synthèse d’ADN et les tests deviennent plus rapides et moins coûteux, des modèles génératifs similaires pourraient transformer la découverte d’enzymes d’une chasse au trésor lente en une tâche de conception rapide et routinière, aidant à orienter davantage la chimie industrielle vers des procédés propres, alimentés par des enzymes.
Citation: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Mots-clés: ingénierie des enzymes, IA générative, conception de protéines, synthase de tryptophane, biocatalyse