Clear Sky Science · fr
Tmem110 régule la conformation de TRPML1 pour maintenir l’homéostasie endolysosomale et prévenir la fuite d’ADN mitochondrial et le traitement pathologique de l’ADN propre
Pourquoi la fuite d’ADN après une blessure importe
Lorsqu’on subit un traumatisme sévère, comme un coup violent à la tête, les dégâts ne se limitent pas au site de la blessure. De nombreux patients développent ensuite une réaction systémique dangereuse dans laquelle les poumons, le foie, les reins et d’autres organes commencent à défaillir. Cette étude révèle comment de petites structures intracellulaires — lysosomes, mitochondries et capteurs immunitaires — communiquent pour décider si le corps nettoie discrètement les débris ou bascule dans une attaque immunitaire dirigée contre lui‑même. Comprendre ce système de nettoyage caché pourrait ouvrir de nouvelles voies pour prévenir l’insuffisance d’organes après un traumatisme et pour traiter les maladies auto‑immunes et inflammatoires.
Du traumatisme crânien à la crise généralisée
Le traumatisme crânien (TBI) peut déclencher une tempête inflammatoire puissante appelée syndrome de dysfonctionnement multiviscéral (MODS), mais le mécanisme par lequel des lésions cérébrales se propagent vers des organes distants restait flou. Les auteurs se concentrent sur les monocytes et les macrophages, des cellules immunitaires qui patrouillent le sang et les tissus et jouent le rôle de ramasseurs de déchets professionnels. Après un TBI, des cellules meurent de manière incontrôlée et libèrent des mitochondries entières — petites centrales énergétiques qui possèdent leur propre ADN — dans la circulation. Cet ADN mitochondrial (ADNmt) ressemble à s’y méprendre à de l’ADN bactérien pour le système immunitaire et peut déclencher des défenses antivirales puissantes s’il n’est pas éliminé rapidement. Normalement, les cellules internalisent ces mitochondries errantes dans des compartiments acides appelés lysosomes, où des enzymes digèrent l’ADN avant qu’il ne fuit dans le cytosol. 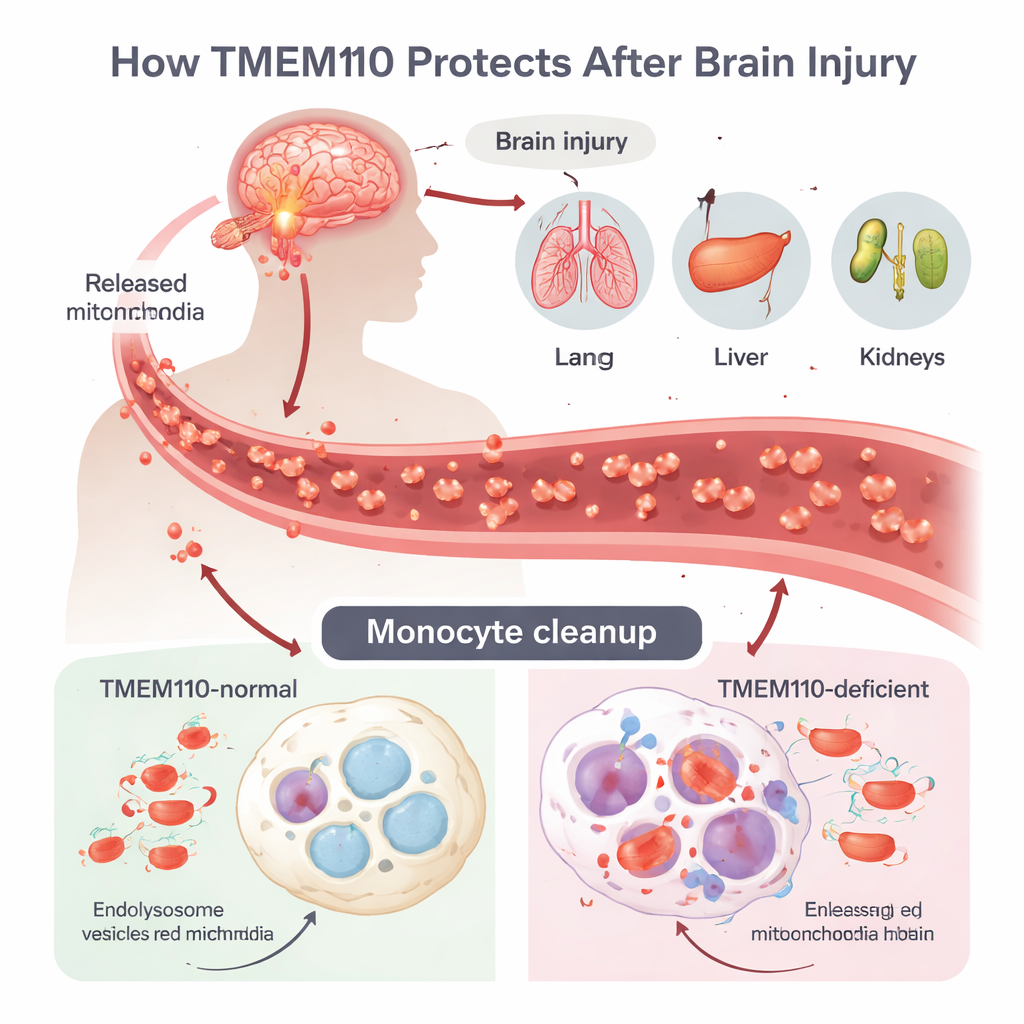
Une protéine gardienne qui stabilise les lysosomes
L’équipe a identifié TMEM110, une protéine traversant la membrane du réticulum endoplasmique (un important réseau membranaire intracellulaire), comme un gardien crucial de ce processus. En utilisant des souris génétiquement modifiées dépourvues de TMEM110 uniquement dans les monocytes et les macrophages, ils ont mis en place un modèle contrôlé de lésion cérébrale. Par rapport aux souris normales, les animaux déficients en TMEM110 présentaient des niveaux nettement plus élevés d’interférons de type I — de puissantes molécules de signalisation antivirale — dans leur sang et leur liquide céphalorachidien. Leurs poumons, foie, reins et ganglions lymphatiques montraient des lésions plus sévères, et leur survie à long terme après TBI était considérablement réduite. Lorsque les chercheurs bloquèrent le récepteur des interférons de type I, ou remplacèrent la moelle osseuse mutante par des cellules normales, les taux de lésions d’organes et de mortalité diminuèrent, indiquant que la signalisation interféron excessive par les monocytes périphériques est un moteur clé du MODS dans ce contexte.
Comment une mauvaise gestion des ions laisse l’ADN s’échapper
En explorant ces cellules immunitaires, les auteurs constatèrent que les lysosomes dépourvus de TMEM110 étaient déséquilibrés sur le plan chimique : moins acides et surchargés en calcium. Dans ces conditions, l’enzyme DNase II — qui dégrade normalement l’ADN dans les lysosomes — perdait de son activité, les membranes lysosomales devenaient fragiles et l’ADNmt s’échappait dans le cytosol environnant. Des expériences en laboratoire avec des monocytes humains phagocytant des mitochondries donneuses marquées confirmèrent que, sans TMEM110, davantage d’ADNmt fuyait dans le cytosol et déclenchait une montée des gènes stimulés par les interférons. L’étude montre que TMEM110 agit en contrôlant une autre protéine, le canal ionique lysosomal TRPML1. Lorsque TMEM110 est présent, il contacte physiquement TRPML1 et le déplace vers une conformation « ouverte » qui crée de petits points de libération de calcium à la surface du lysosome. Ces sorties contrôlées de calcium aident à maintenir l’acidité adéquate, soutiennent la réparation membranaire et empêchent l’ADNmt de s’échapper, en favorisant sa dégradation à l’intérieur. 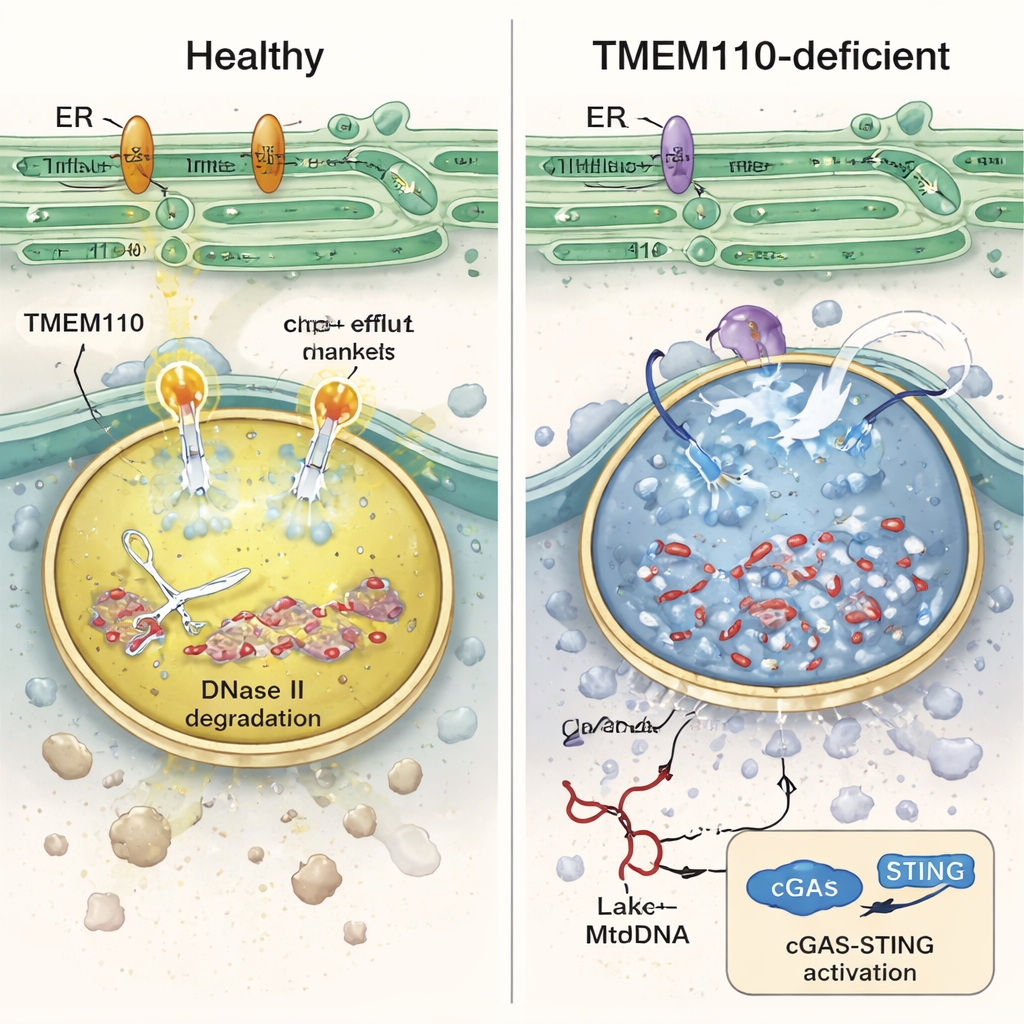
Une boucle de rétroaction avec le système d’alarme de l’ADN
Une fois que l’ADNmt se répand dans le cytosol, il est reconnu par la voie cGAS–STING, la principale alarme cellulaire contre l’ADN errant. Fait intéressant, TMEM110 se lie aussi à STING au repos et le maintient séquestré dans le réticulum endoplasmique, empêchant une alarme inutile. Lorsque l’ADN cytosolique s’accumule, STING s’active et relâche son emprise sur TMEM110. Cela expose alors une autre région de TMEM110 qui interagit avec TRPML1 et renforce l’efflux de calcium lysosomal, créant une boucle de rétroaction : la détection d’ADN propre active un mécanisme qui améliore son élimination. Des mutations de STING associées à des maladies humaines inflammatoires perturbent ce transfert, piégeant TMEM110 dans un état inhibé et contribuant à une activation chronique des interférons. Chez des souris porteuses d’une telle mutation de STING, le TBI entraîna des lésions d’organes plus graves et une mortalité plus élevée, mais l’administration d’un petit fragment de TMEM110 ciblé aux lysosomes via une thérapie par nanoparticules lipidiques d’ARNm restaura partiellement le contrôle de l’ADNmt et améliora la survie.
Indices tirés des patients et voies vers de nouveaux traitements
Les auteurs se sont ensuite tournés vers une cohorte clinique de 143 personnes présentant un traumatisme crânien lié à un traumatisme et un MODS. Les patients dont les monocytes montraient des niveaux plus élevés de TMEM110 peu après la blessure étaient plus susceptibles de récupérer la fonction organique et de survivre. Ceux ayant moins de TMEM110 présentaient davantage d’ADNmt circulant et de mitochondries décellularisées, des réponses interferoniques plus fortes, des scores de défaillance d’organes plus élevés et des profils d’auto‑anticorps plus larges, y compris des anticorps dirigés contre l’ADN et des protéines nucléaires. Ces schémas reflétaient étroitement les observations chez la souris, soutenant l’idée que le contrôle de la stabilité lysosomale et de l’élimination de l’ADNmt piloté par TMEM110 est un mécanisme partagé dans la maladie humaine.
Ce que cela signifie pour les patients victimes de traumatismes sévères
En termes simples, ce travail suggère qu’après une blessure majeure notre système immunitaire fait face à un choix délicat : digérer silencieusement le flot d’ADN provenant des cellules mourantes, ou l’interpréter comme une invasion virale et déclencher une attaque massive qui peut endommager nos propres organes. TMEM110, en modulant un canal ionique lysosomal et en coordonnant avec le capteur d’ADN STING, aide les cellules à choisir la voie la plus sûre. Lorsque ce système échoue — parce que TMEM110 manque, que STING est muté ou que les lysosomes sont submergés — l’ADNmt s’échappe, l’alarme ne cesse de retentir et une atteinte multiviscérale s’ensuit. Cibler cet axe TMEM110–TRPML1–STING, par exemple avec des thérapies d’ARNm dirigées vers les lysosomes, pourrait offrir une nouvelle façon de prévenir ou de traiter l’insuffisance d’organes et les complications de type auto‑immun après un traumatisme sévère.
Citation: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Mots-clés: traumatisme crânien, ADN mitochondrial, lysosomes, interféron de type I, voie cGAS‑STING