Clear Sky Science · fr
L’expression de la versican par les fibroblastes pulmonaires supprime la fibrose pulmonaire
Pourquoi la cicatrisation pulmonaire a besoin d’un meilleur frein
La fibrose pulmonaire idiopathique est une maladie pulmonaire implacable où la réparation normale se transforme en cicatrisation incontrôlée, privant progressivement les patients de leur souffle. Cette étude révèle un surprenant « système de freinage » naturel dans les poumons : une grande molécule chargée de sucres appelée versican, produite par les cellules du tissu conjonctif connues sous le nom de fibroblastes. Plutôt que d’aggraver les lésions, la versican d’origine fibroblastique aide à limiter la formation de cicatrices, remettant en cause notre vision de la cicatrisation et ouvrant des pistes pour de nouvelles stratégies thérapeutiques contre cette maladie jusque‑là difficile à traiter.
Une réparation mortelle qui déraille
Dans des poumons sains, un maillage délicat de protéines et de sucres — la matrice extracellulaire — soutient les petits sacs aériens où s’effectue l’échange d’oxygène. Après une lésion, les fibroblastes affluent, déposent une nouvelle matrice, puis se calmeraient. Dans la fibrose pulmonaire idiopathique, ce programme de réparation ne s’éteint jamais correctement. Les fibroblastes s’accumulent, tissent des échafaudages de collagène denses et rigidifient le tissu pulmonaire, si bien que respirer ressemble à gonfler une balle en caoutchouc remplie de ciment. Les auteurs ont cherché à comprendre le rôle d’un composant matriciel particulier, la versican, car elle est abondante dans les poumons malades mais sa fonction restait énigmatique.
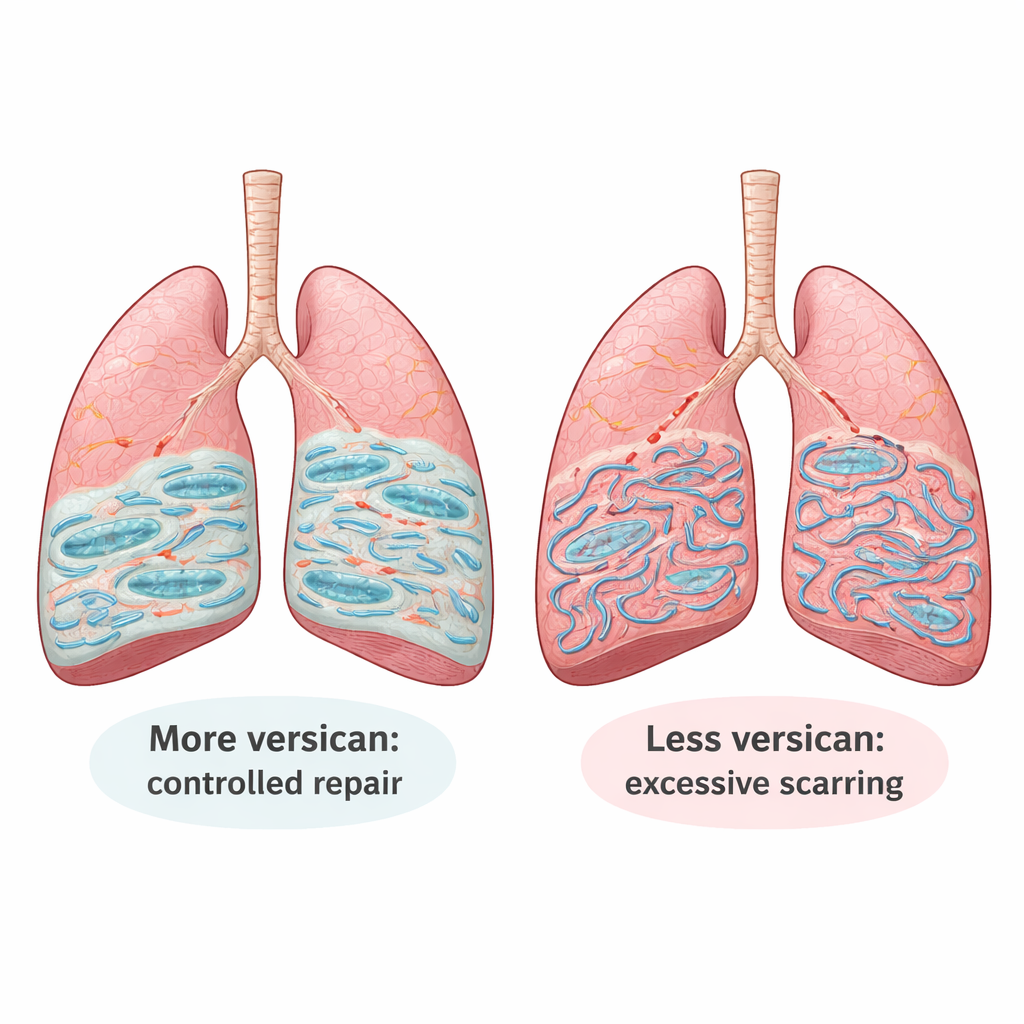
Un manteau protecteur autour des cellules pulmonaires
En explorant de larges bases de données génétiques de patients et en examinant des biopsies pulmonaires, les chercheurs ont constaté que les niveaux de versican sont constamment plus élevés dans les poumons fibrosés et en particulier augmentés dans les fibroblastes et certaines cellules immunitaires. Dans un modèle murin couramment utilisé de fibrose pulmonaire, ils ont observé le même schéma : après la lésion, la production de versican a fortement augmenté au pic de la cicatrisation puis a diminué à l’amorce de la récupération. In vitro, des fibroblastes pulmonaires normaux exposés à un signal pro‑cicatrisation puissant (le facteur de croissance TGF‑β) ou cultivés sur une matrice déjà cicatrisée ont réagi en augmentant la production de versican, ce qui suggère que la versican fait partie de la réponse intrinsèque du poumon à un environnement rigide et riche en collagène.
Quand le frein s’affaiblit, la cicatrisation s’aggrave
Pour savoir si la versican est amie ou ennemie, l’équipe a utilisé des souris qui ne produisent qu’environ la moitié de la quantité normale de versican. Contrairement à ce que pourrait laisser penser sa forte présence dans la maladie, ces souris « pauvres en versican » ont été plus gravement touchées après une lésion pulmonaire. Elles ont perdu plus de poids, accumulé davantage de liquide et de collagène soluble dans les espaces aériens, et développé des poumons plus épais et plus rigides qui mettaient plus de temps à récupérer. L’imagerie détaillée montrait des dépôts de collagène plus massifs et une structure tissulaire plus déformée. Des mesures sur coupes pulmonaires avec microscopie à force atomique ont confirmé que le tissu cicatriciel de ces souris était mécaniquement plus rigide, un facteur clé de l’activation continue des fibroblastes.
Comment une matrice relâchée devient une autoroute pour l’invasion
En analysant plus finement, les scientifiques ont étudié comment la versican façonne l’ossature physique du poumon. Dans des tests sans cellules, l’ajout de versican ralentissait le rapprochement des fibres de collagène, tandis que la réduction de versican permettait au collagène de s’assembler en faisceaux plus épais et plus entremêlés. Dans les tissus vivants et dans la matrice produite par des fibroblastes en culture, une versican réduite signifiait non seulement plus de collagène et de faisceaux plus épais, mais aussi davantage d’autres composants matriciels comme la tenascine‑C et l’acide hyaluronique, ainsi que plus de liaisons croisées qui verrouillent les fibres en réseaux rigides. Les fibroblastes posés sur cette matrice altérée passaient à un mode hautement invasif, formant de nombreux « podosomes » petits et riches en enzymes qui grignotent le matériau environnant et permettent aux cellules de s’enfoncer plus profondément. Bloquer des récepteurs clés du collagène et de la tenascine‑C réduisait ce comportement invasif, reliant directement les modifications structurelles aux actions cellulaires.
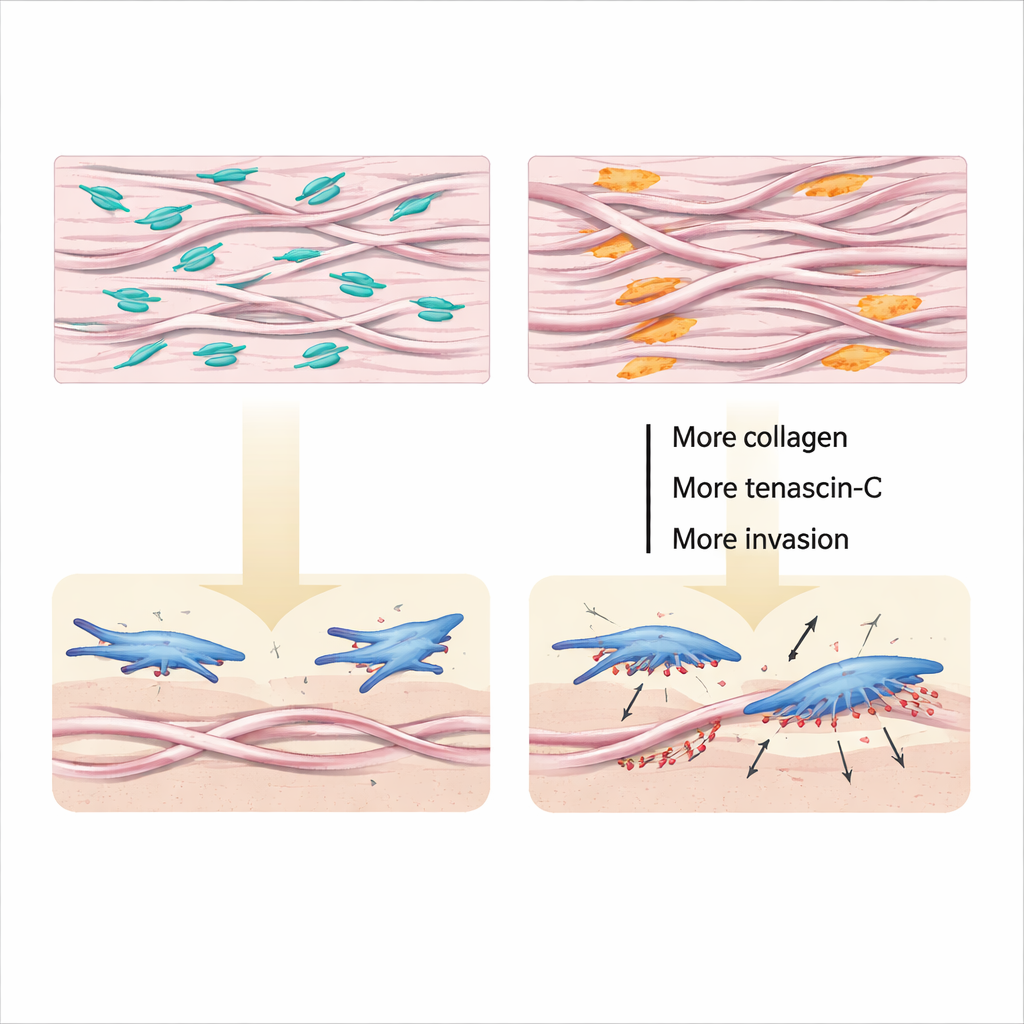
Une molécule à double tranchant porteuse d’espoir
Ces expériences dessinent un tableau clair : la versican produite par les fibroblastes pulmonaires agit comme un limiteur interne de la cicatrisation. Quand la lésion et les facteurs de croissance augmentent la production de collagène, les fibroblastes répondent en élevant la versican, qui empêche les fibres de collagène de devenir trop épaisses et emmêlées, atténue le durcissement excessif et freine la formation de podosomes invasifs. Si les niveaux de versican chutent, le collagène et la tenascine‑C explosent, la matrice se raidit et se noue, les fibroblastes envahissent plus agressivement et la fibrose s’aggrave et persiste. Comme d’autres cellules, notamment immunitaires, peuvent utiliser la versican différemment, elle reste une « arme à double tranchant », mais ce travail montre qu’augmenter ou imiter de façon ciblée l’action de la versican produite par les fibroblastes pourrait constituer une nouvelle voie puissante pour ralentir, voire inverser, la cicatrisation pulmonaire.
Citation: Kanellopoulou, P., Barbayianni, I., Fanidis, D. et al. Versican expression from lung fibroblasts suppresses pulmonary fibrosis. Nat Commun 17, 1676 (2026). https://doi.org/10.1038/s41467-026-68377-5
Mots-clés: fibrose pulmonaire idiopathique, matrice extracellulaire, versican, fibroblastes pulmonaires, cicatrisation tissulaire