Clear Sky Science · fr
Micropatch d’aiguilles à nanomoteurs activés par lumière proche infrarouge pour le traitement actif de l’acné infectée par des bactéries
Pourquoi cette recherche sur l’acné est importante
L’acné est souvent réduite à un simple problème esthétique, mais pour les adolescents et les adultes elle peut être douloureuse, laisser des cicatrices et peser sur le plan émotionnel. Les traitements classiques, en particulier les antibiotiques, peuvent provoquer des effets indésirables et favoriser l’émergence de bactéries résistantes. Cette étude décrit un patch d’aiguilles alimenté par une lumière proche infrarouge inoffensive qui délivre de minuscules « nanomoteurs » directement dans les lésions d’acné. Ces particules intelligentes génèrent leur propre oxygène, se déplacent activement à travers les couches visqueuses des bactéries et chauffent juste assez pour tuer les germes et calmer l’inflammation — offrant un aperçu d’un futur soin de l’acné plus ciblé et moins dépendant des antibiotiques.
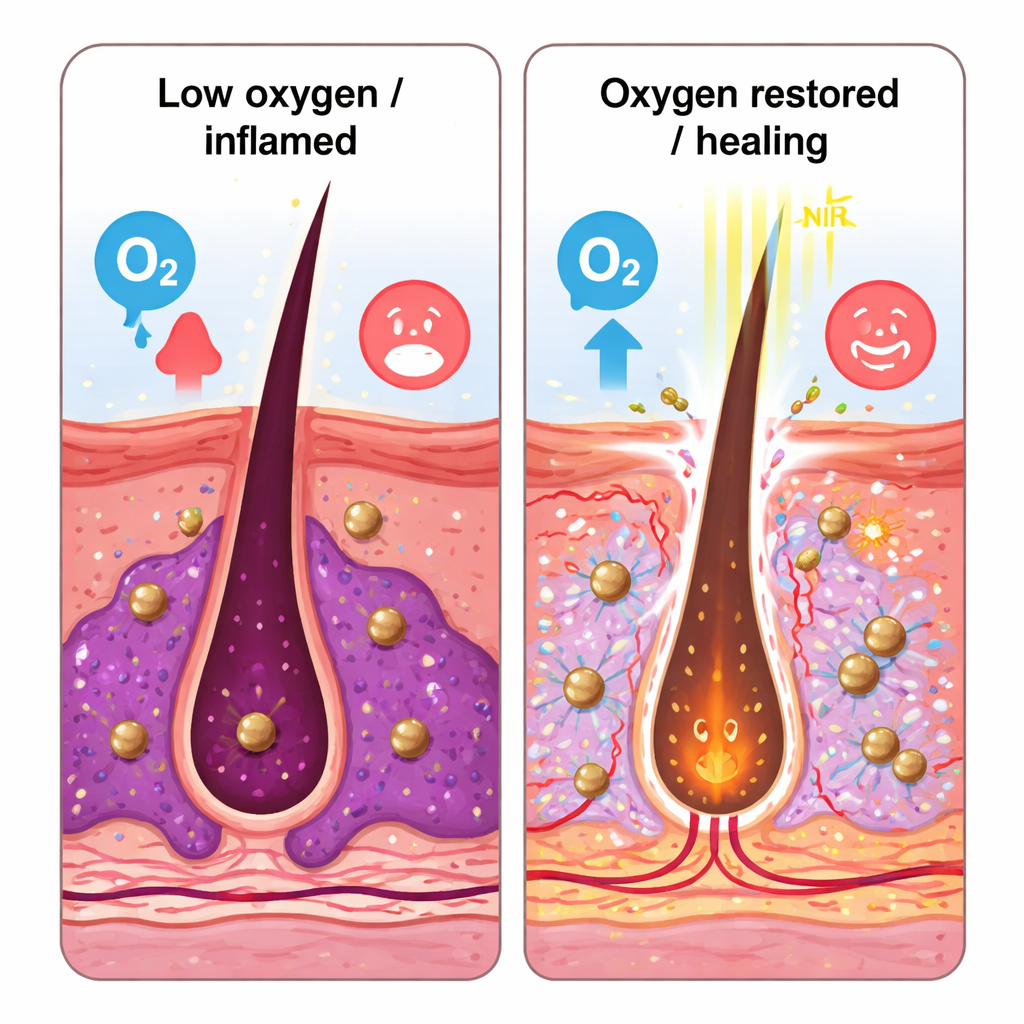
Comment l’acné évolue en une papule enflammée
La plupart des acnés commencent lorsque les pores et les follicules pileux se bouchent avec du sébum et des cellules mortes. À l’intérieur de ces follicules obstrués, une bactérie appelée Cutibacterium acnes (anciennement Propionibacterium acnes) se multiplie dans cet environnement pauvre en oxygène. Les microbes forment des biofilms protecteurs — des communautés collantes enveloppées dans une matrice dense — qui les protègent des médicaments. En se nourrissant des huiles cutanées, ils libèrent des acides gras qui réduisent encore l’oxygène et irritent les cellules voisines. La peau réagit en produisant des signaux inflammatoires tels que le TNF‑α et des interleukines, et les cellules immunitaires locales qui maintiennent normalement l’équilibre microbien s’épuisent. Ensemble, ces modifications provoquent les rougeurs, le gonflement et parfois les cicatrices observés dans l’acné tenace.
Pourquoi les crèmes et comprimés classiques échouent souvent
Les crèmes et gels topiques peinent à traverser la barrière externe de la peau, et les antibiotiques oraux exposent tout l’organisme au médicament pour atteindre une petite zone, augmentant le risque d’effets indésirables et d’apparition de souches résistantes. À l’intérieur d’une lésion d’acné mature, le biofilm épais autour de C. acnes bloque en outre la pénétration. Même la photothermie — l’utilisation de particules absorbantes de lumière pour produire de la chaleur qui tue les bactéries — rencontre des limites, car les particules ne peuvent pas se déplacer profondément dans le biofilm, et l’environnement acide et pauvre en oxygène autour de la lésion entretient une inflammation chronique plutôt que la guérison.
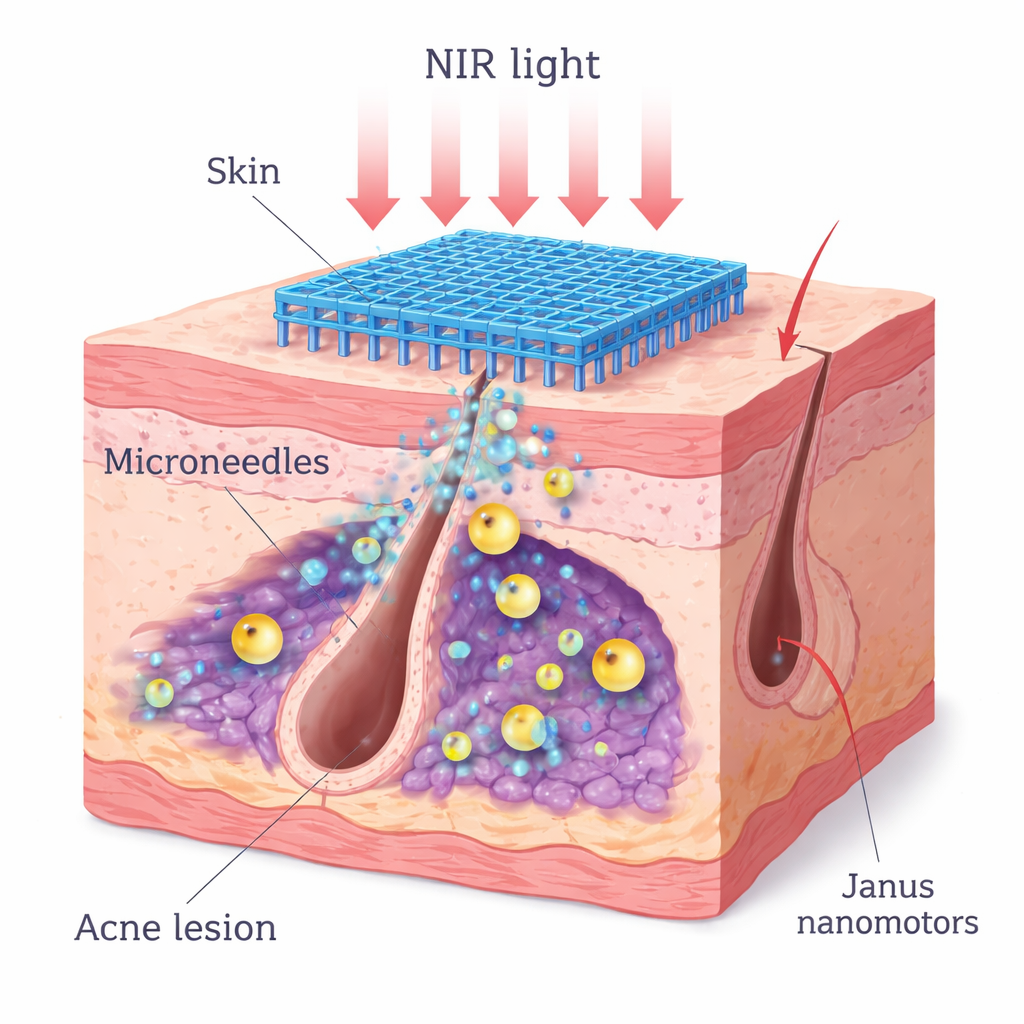
Un patch microneedle activé par la lumière avec de minuscules moteurs
Les chercheurs ont conçu un patch à microneedles dissolvable qui pénètre sans douleur juste sous la surface de la peau et libère des nanomoteurs conçus. Chaque nanomoteur possède un cœur en peroxyde de zinc qui se décompose lentement en conditions acides, libérant du peroxyde d’hydrogène, lui‑même converti en oxygène par une enveloppe de dioxyde de manganèse. Un côté de la particule est revêtu d’une couche absorbante de lumière composée de polydopamine et de dioxyde de manganèse, créant une structure « Janus » (à deux faces). Quand un laser proche infrarouge de 808 nm éclaire la peau, ce revêtement asymétrique chauffe un côté plus que l’autre, créant un gradient de température qui propulse la particule en avant. Cette autopropulsion aide les nanomoteurs à se répandre à travers les biofilms denses et les espaces folliculaires tout en délivrant simultanément de la chaleur pour affaiblir les défenses bactériennes.
Du banc de laboratoire à la peau de souris
Dans des essais en laboratoire, les nanomoteurs chauffaient efficacement sous lumière proche infrarouge, restaient stables sur des cycles répétés et libéraient davantage de peroxyde d’hydrogène et d’oxygène en conditions acides simulant un biofilm. Les patchs microneedles fabriqués en acide hyaluronique, bien toléré par la peau, étaient suffisamment robustes pour percer la peau mais se dissolvaient en environ une demi‑heure, libérant les nanomoteurs dans le derme. Sous le faisceau lumineux, les particules montraient un mouvement nettement amélioré et pénétraient plus profondément dans des biofilms artificiels et la peau de porc. Dans des cultures bactériennes de C. acnes et de Staphylococcus aureus résistant aux médicaments, la combinaison microneedles + nanomoteurs + cinq minutes d’exposition proche infrarouge a réduit la masse du biofilm et la survie bactérienne de plus de 90 %, et provoqué des dégâts visibles aux membranes microbiennes et à l’ADN.
Apaiser l’inflammation et rétablir l’équilibre
Dans un modèle murin d’acné, obtenu en injectant C. acnes dans la peau, le patch activé par la lumière a réduit la taille des lésions et le nombre de bactéries aussi efficacement que l’érythromycine, mais sans dommages tissulaires évidents. Les coupes cutanées des souris traitées montraient moins de cellules inflammatoires, des niveaux plus faibles de molécules inflammatoires (IL‑6, TNF‑α) et une activité réduite de HIF‑1α, un marqueur d’hypoxie. Parallèlement, des marqueurs de néovascularisation et de réparation tissulaire augmentaient, et des cellules immunitaires clés appelées ILC3, qui avaient été supprimées par l’infection, rebondissaient et produisaient davantage du facteur de réparation IL‑22. Les auteurs suggèrent qu’en fournissant de l’oxygène et en fragmentant physiquement les biofilms, les nanomoteurs contribuent à normaliser à la fois le microbiome local et l’environnement immunitaire cutané.
Ce que cela pourrait signifier pour les soins anti‑acné futurs
Pour un lecteur non spécialiste, la conclusion est que ce système microneedle‑nanomoteur agit comme un traitement intelligent et localisé : il ouvre doucement un passage à travers la peau, guide de minuscules moteurs au cœur d’une lésion d’acné et, sous une brève impulsion de lumière invisible, délivre chaleur et oxygène exactement là où ils sont nécessaires. Chez la souris, cette approche a éliminé l’infection, atténué l’inflammation et favorisé la réparation tissulaire, égalant la performance d’un antibiotique sans exposer tout l’organisme au médicament. Si des essais chez l’humain et des études de sécurité à long terme restent nécessaires, ce travail ouvre la voie à une nouvelle classe de thérapies de l’acné qui combinent pénétration mécanique, activation à la demande et oxygène auto‑généré pour traiter de façon plus précise les infections à base de biofilm avec moins d’effets secondaires.
Citation: Hu, Z., Gan, Y., Song, Y. et al. Near-infrared light-driven nanomotors-based microneedles for the active therapy of bacterial infected acne. Nat Commun 17, 1675 (2026). https://doi.org/10.1038/s41467-026-68376-6
Mots-clés: traitement de l’acné, patch à microneedles, nanomoteurs, thérapie proche infrarouge, biofilms bactériens