Clear Sky Science · fr
Structure cryo‑EM du complexe ubiquitine ligase humain COP1‑DET1
Comment les cellules décident quelles protéines détruire
À l’intérieur de chaque cellule, des milliers de protéines doivent être continuellement fabriquées, remodelées ou détruites au bon moment. Cet article examine l’une des machines de « contrôle qualité » clés de la cellule, un broyeur moléculaire qui décide quand éliminer des régulateurs puissants de l’expression génique impliqués dans le développement et le cancer. En révélant sa structure tridimensionnelle à une résolution quasi atomique, les auteurs montrent comment cette machine peut basculer entre un état empilé inactif et une forme active capable de traiter les substrats — un éclairage qui pourrait, à terme, aider à concevoir des médicaments pour l’activer ou la bloquer.
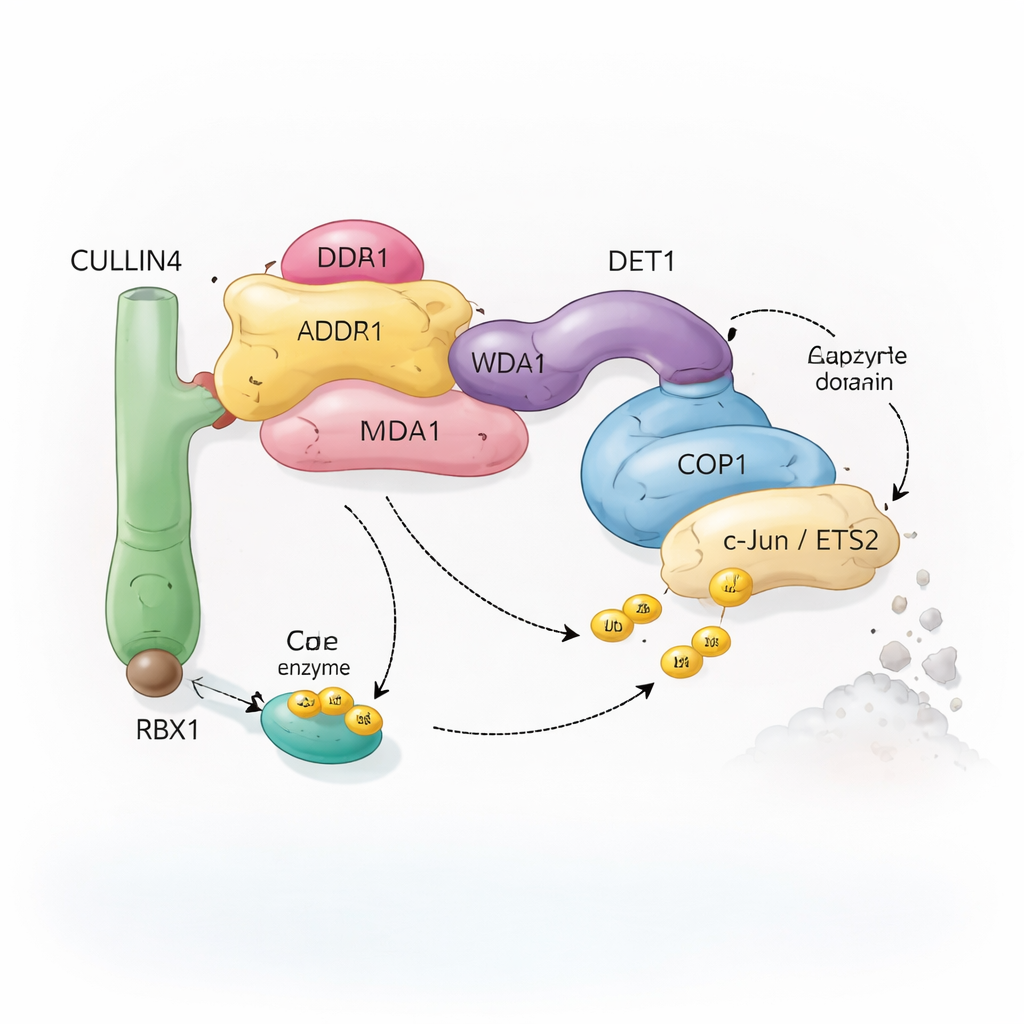
Une équipe moléculaire de recyclage composée de nombreuses pièces
Les cellules s’appuient sur un système appelé ubiquitination pour marquer les protéines destinées au recyclage. De petits peptides d’ubiquitine jouent le rôle de drapeaux amovibles qui indiquent à la cellule si une protéine doit être modifiée, relocalisée ou détruite. Des complexes enzymatiques spécialisés, appelés ligases d’ubiquitine, fixent ces drapeaux sur des cibles sélectionnées. Le complexe étudié ici est centré sur COP1, une protéine présente des plantes aux humains, qui aide à marquer des facteurs de transcription importants — des protéines qui contrôlent l’activation ou la répression des gènes. COP1 ne travaille pas seul : il s’intègre dans un assemblage plus vaste construit autour d’une protéine échafaudage nommée CULLIN4, ainsi que plusieurs adaptateurs appelés DDB1, DDA1 et DET1. Ensemble, ces éléments forment une « équipe de recyclage » flexible qui reconnaît des facteurs de transcription spécifiques tels que c‑Jun et ETS2, bon nombre étant impliqués dans la croissance cellulaire et le cancer.
Capturer le complexe en 3D
Pour comprendre comment cette équipe fonctionne, les chercheurs ont utilisé la cryo‑microscopie électronique en particules uniques, une technique qui image des protéines vitrifiées et reconstruit leurs formes à haute résolution. Ils ont reconstitué le système humain COP1–DET1 dans des cellules en culture, purifié les complexes et visualisé plusieurs états structurels distincts. Ils ont d’abord résolu la structure du module DDB1–DDA1–DET1, qui agit comme un noyau central. DET1 adopte une forme inhabituelle, partiellement flexible plutôt qu’un disque rigide, avec une « griffe » saillante capable d’agripper des enzymes partenaires. Puis, en ajoutant COP1 et une classe d’enzymes auxiliaires connues sous le nom d’E2, ils ont capturé des assemblages plus grands montrant comment toutes les pièces s’emboîtent, révélant à la fois des empilements compacts et des arrangements dimériques plus ouverts (deux COP1).
Un empilement inactif et un dimère actif
Une des découvertes les plus frappantes est une structure empilée, en filament, constituée de couches répétées du complexe. Dans chaque couche, huit molécules de COP1 s’entrelacent via leurs segments en coiled‑coil, formant un anneau en forme de losange. Leurs régions de reconnaissance des substrats, appelées domaines WD40, sont orientées dans une même direction et partiellement protégées par les couches voisines. Ce compactage serré représente probablement un état « off » dans lequel l’accès aux protéines cibles est limité. En revanche, lorsque l’équipe a examiné des complexes co‑exprimés avec des substrats de COP1 tels que c‑Jun ou ETS2, ils ont observé une forme dimérique différente : deux molécules de COP1 disposées côte à côte, avec leurs domaines WD40 orientés vers l’extérieur et disponibles pour se lier aux courts motifs « VP » présents dans de nombreux facteurs de transcription. Des tests biochimiques ont confirmé que seul cet état dimérique soutient efficacement l’élongation de longues chaînes d’ubiquitine sur c‑Jun.
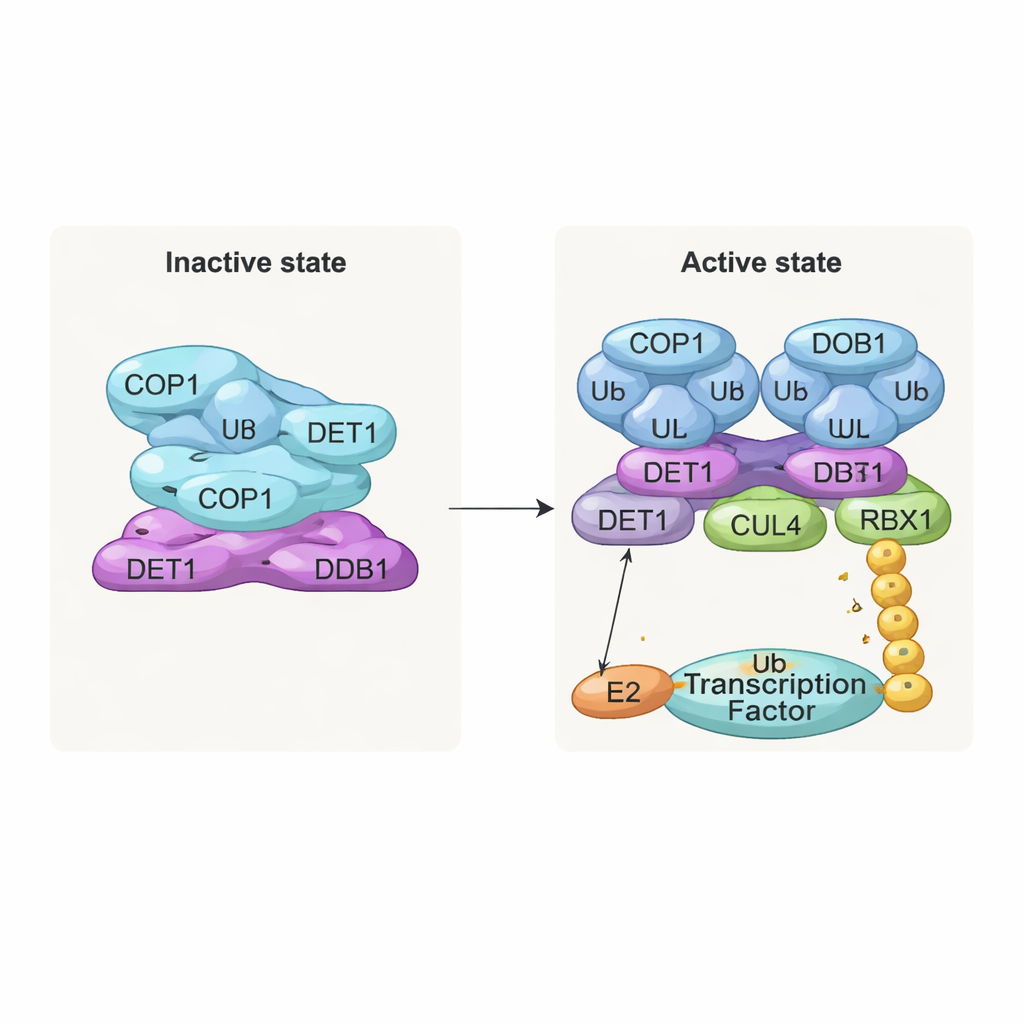
DET1, pont flexible et chef de la circulation
DET1 apparaît comme l’organisateur clé qui relie toutes les parties de la machine. Sa région N‑terminale s’insère dans DDB1, ancrant le complexe sur l’échafaudage CULLIN4, tandis que sa région en forme de griffe s’enroule autour d’une famille d’enzymes E2 appelées Ube2e. Des expériences mutationnelles détaillées montrent que c’est DET1, et non COP1, qui saisit directement ces E2, les positionnant à proximité de la région catalytique RING de COP1. Dans cet agencement, Ube2e semble aider à placer les toutes premières étiquettes d’ubiquitine sur le substrat. Une seconde enzyme E2, Ube2d3, est ensuite recrutée via le bras CULLIN4–RBX1 pour prolonger ces étiquettes en chaînes plus longues signalant la dégradation complète. Autrement dit, DET1 fonctionne comme un pont flexible présentant un E2 à COP1, tandis que l’échafaudage plus large amène un second E2 pour terminer le travail.
Pourquoi c’est important pour la santé et la maladie
En cartographiant ces états structuraux et leurs activités, l’étude explique comment un même jeu de protéines peut alterner entre une forme empilée inerte et un dimère actif qui cible des facteurs de transcription pour destruction. Cet interrupteur est particulièrement important pour des facteurs comme c‑Jun, qui stimulent la division cellulaire et sont fortement liés au cancer lorsqu’ils sont mal régulés. Comprendre comment COP1 et DET1 coopèrent — comment la griffe de DET1 sélectionne des E2 spécifiques, comment la surface WD40 de COP1 reconnaît des substrats contenant le motif VP, et comment le dimère actif se forme — fournit une feuille de route pour des travaux futurs. À long terme, des médicaments qui stabilisent l’empilement inactif ou favorisent le dimère actif pourraient offrir de nouveaux moyens de moduler les voies de contrôle génique dans le cancer et d’autres maladies où la dégradation des protéines est perturbée.
Citation: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Mots-clés: ligase ubiquitine, COP1, dégradation des protéines, structure cryo‑EM, c‑Jun