Clear Sky Science · fr
Les protéases dépendantes de l’ubiquitine K48 découpent les protéines post-RER
Comment les cellules décident quelles protéines détruire
Nos cellules éliminent en permanence les protéines usées ou endommagées, en particulier celles intégrées aux membranes qui jouent le rôle de portes et de capteurs. Cet article révèle que les cellules utilisent une petite étiquette appelée ubiquitine non seulement comme un simple label « poubelle », mais comme un code qui indique précisément comment les protéines membranaires seront dégradées. Comprendre ce code aide à expliquer comment les cellules préservent leur santé et peut orienter des thérapies futures visant à détruire délibérément des protéines pathogènes.
Un code-barres cellulaire pour l’élimination des protéines
Les cellules décorent les protéines indésirables de chaînes d’une petite protéine appelée ubiquitine. Ces chaînes peuvent être reliées de différentes manières, un peu comme des perles passées par différents trous, et chaque motif peut signaler une issue différente. Les auteurs se sont concentrés sur les protéines membranaires qui ont déjà quitté le réticulum endoplasmique (RER) et circulent dans des compartiments tels que l’appareil de Golgi et les endosomes. Ils ont cherché à savoir si deux types de chaînes courants, appelés ubiquitine liée en K48 et en K63, sont véritablement interchangeables ou s’ils dirigent la cargaison vers des voies de destruction distinctes.
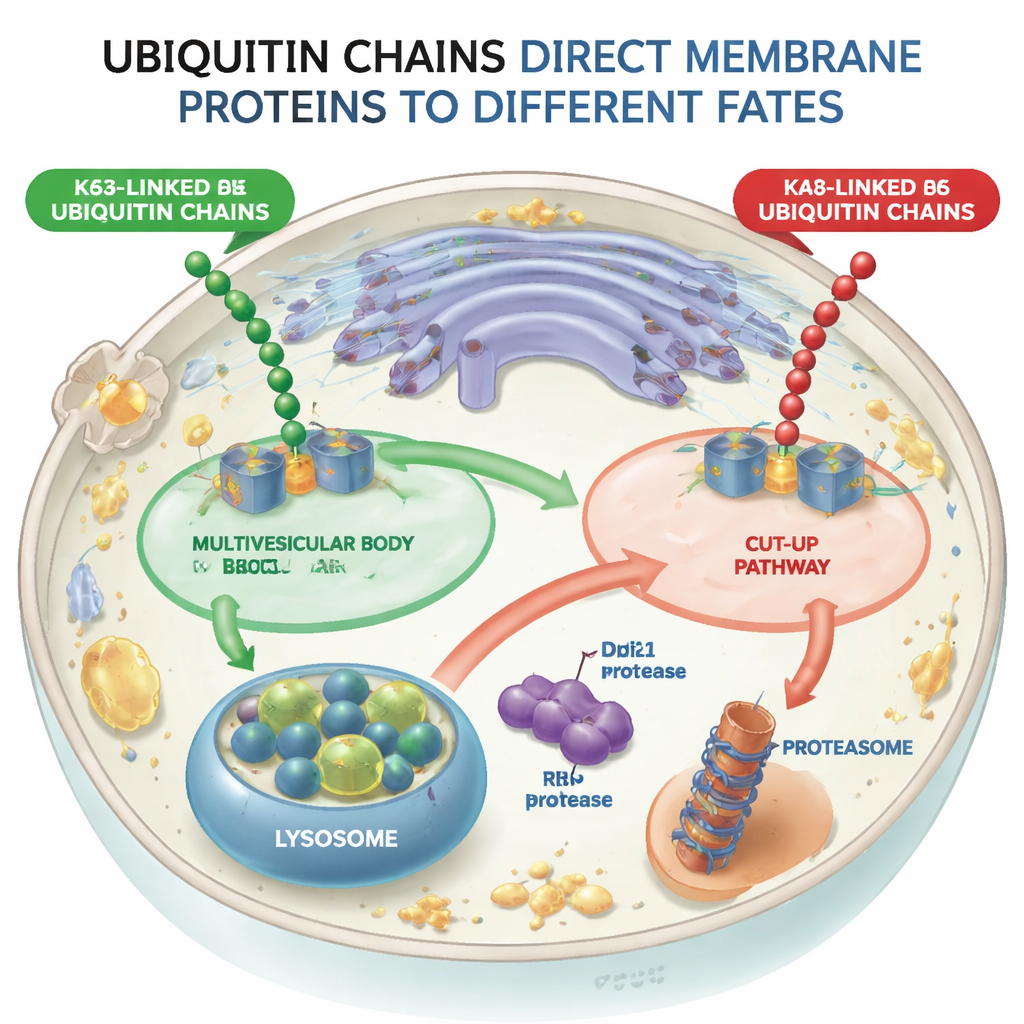
Deux voies divergentes pour les protéines étiquetées
En utilisant des levures comme modèle, les chercheurs ont conçu des machines moléculaires (ligases d’ubiquitine) capables d’attacher soit des chaînes K48, soit des chaînes K63 à la même protéine membranaire test, un récepteur de triage nommé Vps10. Quand Vps10 recevait des chaînes liées en K63, il était envoyé dans des vésicules internes à l’intérieur des endosomes — des structures appelées corps multivésiculaires — qui finissent par fusionner avec les lysosomes, les compartiments digestifs de la cellule. En revanche, quand Vps10 portait des chaînes liées en K48, il ne suivait pas cette voie multivésiculaire. Il était au contraire détruit d’une manière totalement différente, montrant que la cellule distingue ces deux types de chaînes et que la voie multivésiculaire rejette effectivement la cargaison marquée K48.
Une voie « CUT-UP » qui tranche les protéines en deux
L’équipe a découvert que les chaînes liées en K48 déclenchent une voie d’ébranchage des protéines qu’ils appellent CUT-UP, pour Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases (Clivage des cibles ubiquitinées par des protéases dépendantes de l’ubiquitine). Plutôt que d’extraire la protéine entière de la membrane d’un seul coup, CUT-UP la découpe en morceaux qui sont ensuite achevés par les systèmes d’élimination cellulaires existants. Une enzyme clé, Ddi1, circule dans le cytosol et coupe la portion de la protéine membranaire faisant face au cytoplasme. Ce fragment est ensuite digéré par le protéasome, le broyeur principal de protéines de la cellule. Parallèlement, une autre enzyme, Rbd2, est intégrée à la membrane elle-même et coupe la partie de la protéine tournée vers l’intérieur du compartiment, la libérant dans l’espace qui finit par se connecter au lysosome. Il a fallu bloquer simultanément Ddi1, Rbd2, le protéasome et les enzymes lysosomales pour protéger complètement Vps10 marqué K48 de la destruction, confirmant que tous ces composants coopèrent dans la voie CUT-UP.
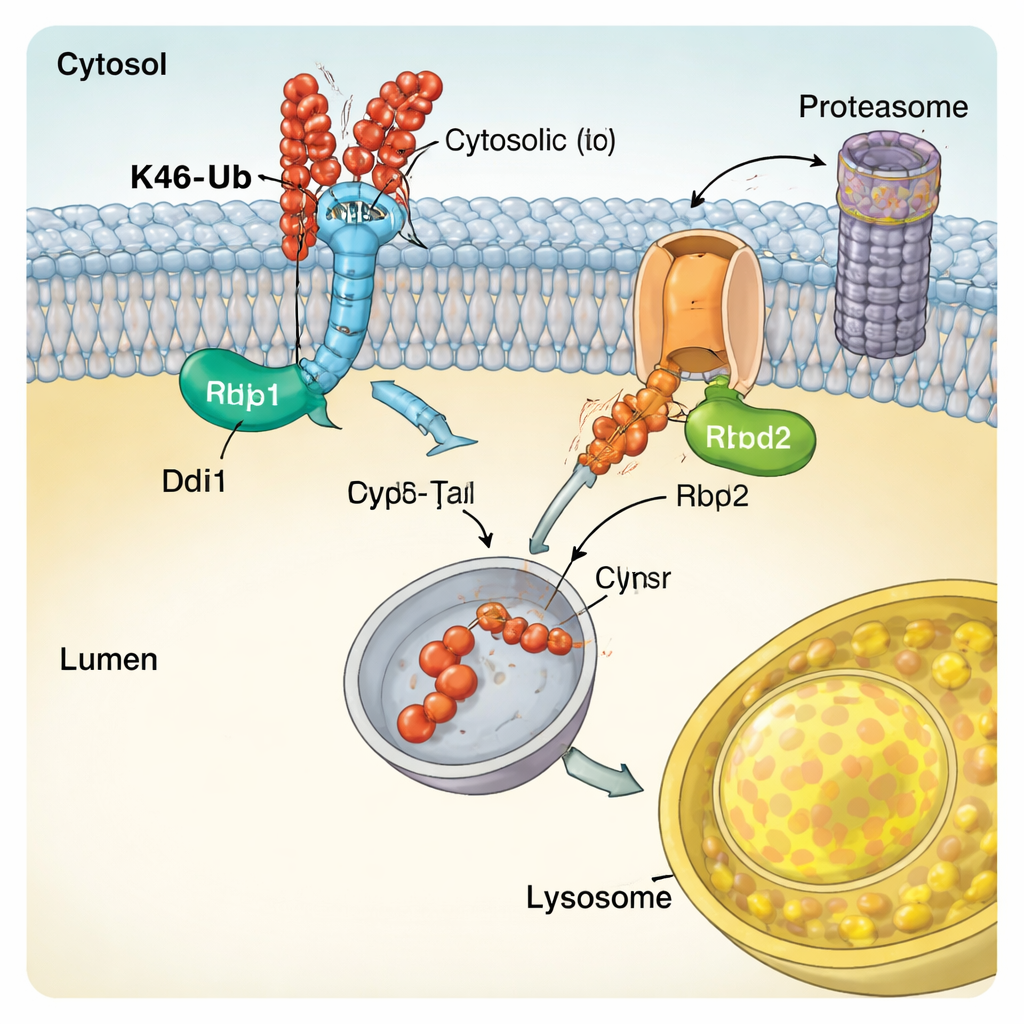
Des enzymes spécialisées qui lisent le code ubiquitine
Pour comprendre comment CUT-UP reconnaît ses cibles, les auteurs ont examiné les caractéristiques moléculaires de Ddi1. Ils ont montré que le noyau catalytique central de Ddi1 non seulement clive les protéines mais peut aussi se lier directement à l’ubiquitine, et que son activité est modulée par des régions supplémentaires qui se fixent aux chaînes d’ubiquitine. Ddi1 montrait une dépendance particulière aux chaînes liées en K48, en accord avec son rôle dans CUT-UP. Rbd2, quant à lui, est une protéase rhomboïde qui traverse la membrane. L’étude a établi que le site actif de Rbd2 est essentiel pour couper les portions de Vps10 faisant face à la lumière du compartiment et que l’enzyme circule à travers plusieurs compartiments sécrétoires, ce qui lui permet d’agir à plusieurs endroits cellulaires. Des enzymes similaires existent dans les cellules humaines et ont été impliquées dans des affections allant de la neurodégénérescence au cancer, suggérant que des mécanismes analogues à CUT-UP pourraient avoir une large importance.
Pourquoi cela compte pour la santé et la thérapie
En montrant que différents types de chaînes d’ubiquitine envoient la même protéine membranaire vers des destins nettement distincts — soit le tri vers les corps multivésiculaires, soit le découpage médié par CUT-UP — ce travail fournit une preuve solide que les cellules utilisent un véritable « code ubiquitine » pour ajuster finement l’élimination des protéines. La découverte de CUT-UP clarifie comment des protéines membranaires récalcitrantes peuvent être démantelées morceau par morceau et met en lumière Ddi1 et Rbd2 comme des acteurs clés qui lisent et appliquent ce code. Pour le grand public, la conclusion est que les cellules ne se contentent pas de marquer les protéines comme déchets : elles spécifient la manière dont ces déchets seront évacués. Alors que les développeurs de médicaments conçoivent des outils qui marquent les protéines nocives avec de l’ubiquitine pour les éliminer, comprendre des voies comme CUT-UP sera essentiel pour prévoir quels fragments seront produits et comment cela pourrait affecter le comportement cellulaire.
Citation: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Mots-clés: code de l’ubiquitine, dégradation des protéines, protéines membranaires, protéasome, lysosome