Clear Sky Science · fr
La perte de la communication Fsr favorise la formation de biofilms et aggrave les issues dans l’endocardite infectieuse à entérocoques
Saboteurs silencieux sur les valves cardiaques
L’endocardite infectieuse est une infection potentiellement mortelle des valves cardiaques, et son incidence augmente dans le monde. Cette étude se concentre sur un coupable majeur, la bactérie intestinale Enterococcus faecalis, et s’interroge sur les raisons pour lesquelles certaines infections sont particulièrement difficiles à traiter. En révélant comment ces bactéries communiquent entre elles et construisent des biofilms protecteurs sur les valves, les chercheurs montrent pourquoi certaines souches entraînent des maladies plus sévères et résistent aux antibiotiques, et pourquoi un système de communication bactérienne, appelé Fsr, s’avère être étonnamment un frein plutôt qu’un accélérateur des dégâts.
Comment les bactéries érigent des forteresses dans le cœur
Les valves cardiaques subissent normalement des flux sanguins parmi les plus rapides de l’organisme, mais si la surface valvulaire est endommagée, des plaquettes et des protéines de la coagulation peuvent former un petit caillot, ou végétation. Ce caillot devient une plate‑forme d’atterrissage pour les bactéries circulant dans le sang. Une fois attachées, les bactéries se multiplient et tissent un biofilm — une communauté visqueuse et structurée qui les protège des cellules immunitaires et des médicaments. L’équipe a utilisé des dispositifs microfluidiques pour imiter le flux sanguin en laboratoire, et un modèle de rat pour recréer l’endocardite chez l’animal, ce qui leur a permis d’observer comment E. faecalis s’adapte à mesure que l’infection passe de quelques cellules isolées à des biofilms épais et matures. 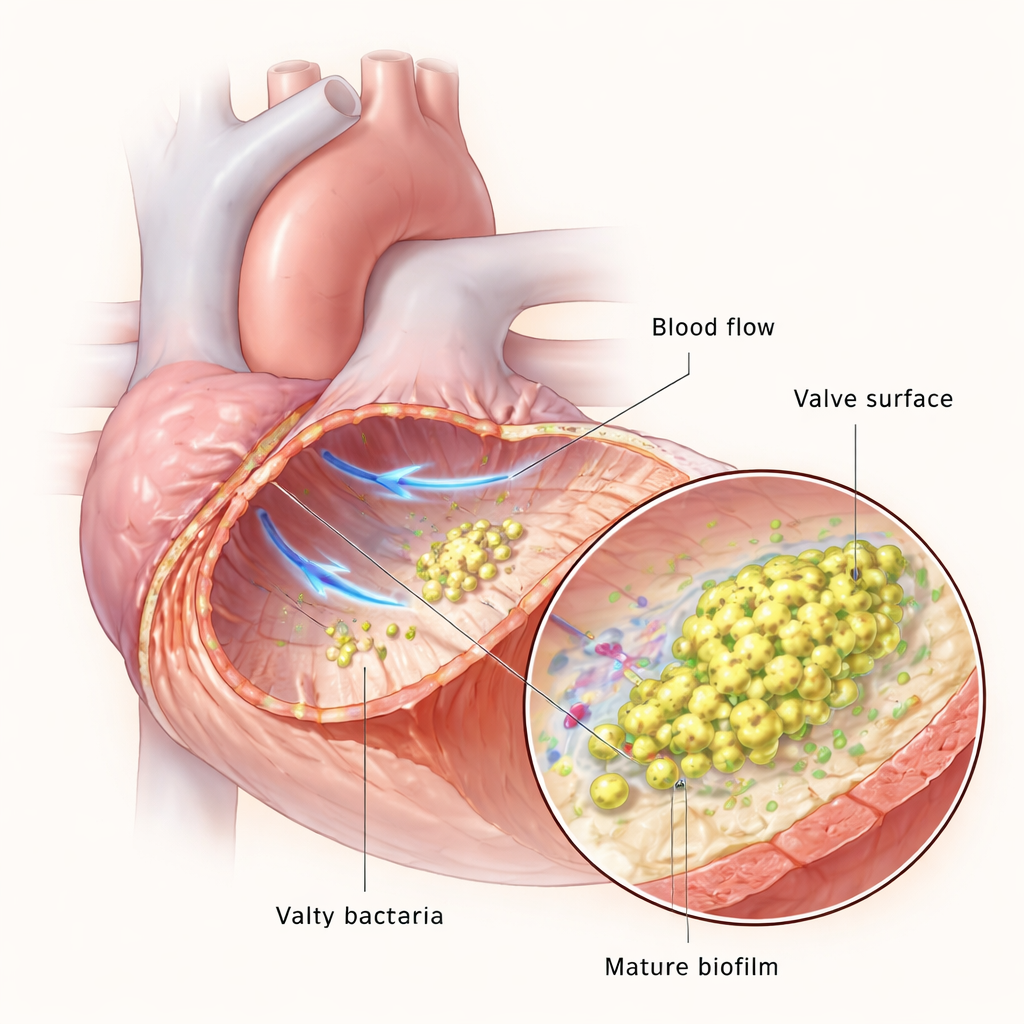
Quand un flot sanguin rapide coupe la « conversation » bactérienne
Les bactéries coordonnent souvent leur comportement via le quorum sensing, un système chimique de « vote » qui active ou désactive des gènes une fois qu’un nombre suffisant de cellules est atteint. Fsr est le système de quorum sensing utilisé par E. faecalis. De manière surprenante, les chercheurs ont constaté qu’un fluide fort et en mouvement lessive en fait les molécules de signal nécessaires à l’activation de Fsr. Au début de l’infection, quand les bactéries adhèrent à la surface exposée de la végétation et subissent la pleine force du flux sanguin, Fsr est largement silencieux. Ce n’est que plus tard, lorsque des microcolonies grossissent et s’enfouissent plus profondément dans la végétation — à l’abri du flux — que Fsr s’active. Cela signifie que dans le cœur réel, le quorum sensing dépend non seulement du nombre de bactéries présentes, mais aussi de leur position au sein de la structure tridimensionnelle.
La désactivation de Fsr laisse les biofilms s’emballer
Pour tester le rôle réel de Fsr dans l’infection, l’équipe a comparé des bactéries normales à des mutants dépourvus de l’ensemble du système Fsr. Au départ, les deux versions colonisaient les valves de façon équivalente. Mais au bout de trois jours, les animaux infectés par des souches déficientes en Fsr présentaient des végétations plus volumineuses et beaucoup plus de bactéries y étaient entassées. L’imagerie détaillée a montré que leurs biofilms recouvraient une plus grande surface du caillot et que leurs microcolonies étaient plus grosses. La perte de Fsr a également arrêté la production de deux enzymes sécrétées clés, GelE et SprE, qui contribuent normalement à façonner le biofilm et peuvent limiter la surcroissance. Les animaux infectés par des mutants manquant uniquement ces enzymes ont aussi développé des biofilms plus volumineux, bien que pas aussi extrêmes que dans les souches Fsr‑nulles, ce qui suggère que d’autres facteurs contrôlés par Fsr jouent également un rôle. 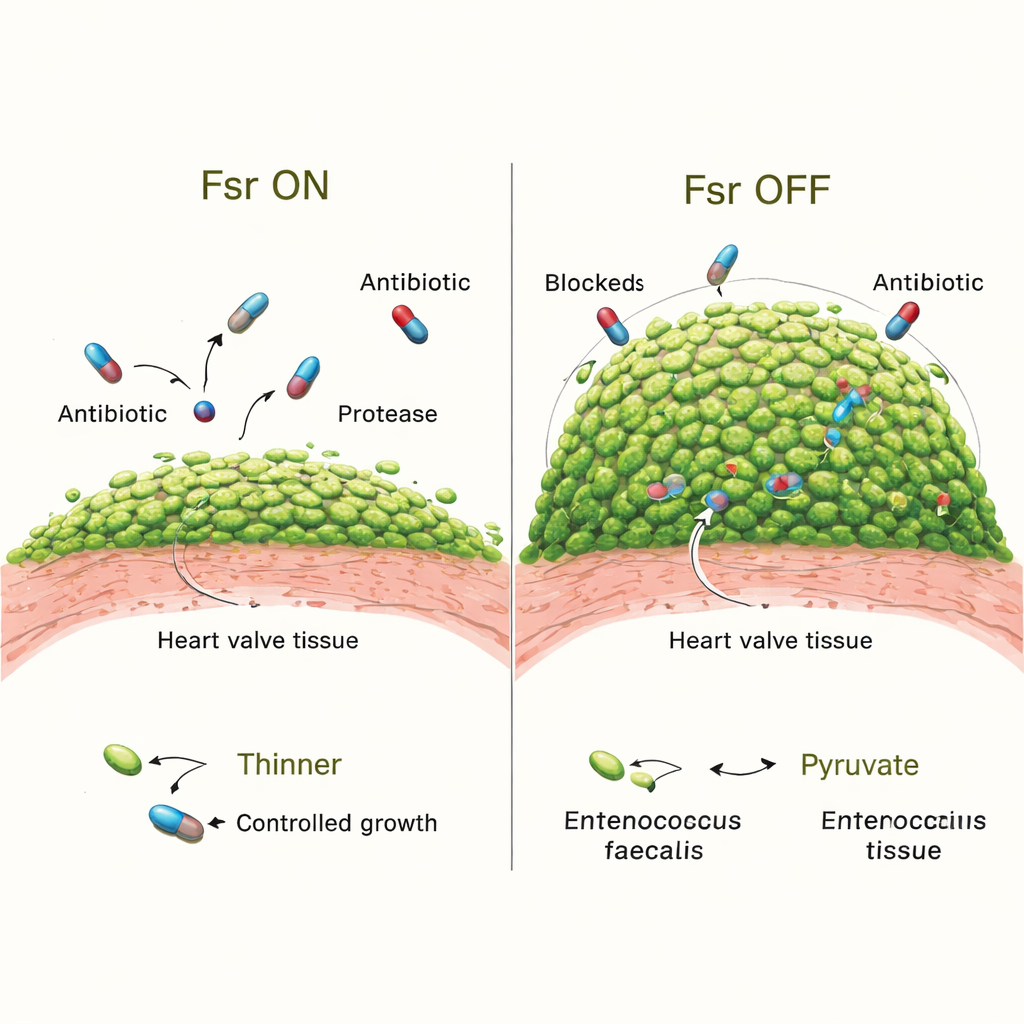
Réorientation métabolique et meilleure tolérance aux antibiotiques
Le profilage de l’expression génique des bactéries à l’intérieur des valves infectées a révélé que Fsr fait plus que contrôler quelques enzymes. En l’absence de Fsr, des centaines de gènes modifiaient leur activité, en particulier ceux impliqués dans l’absorption des sucres et la production d’énergie. Une paire de gènes, lrgA et lrgB, s’est distinguée : fortement activés chez les bactéries déficientes en Fsr, ils aident les cellules à mieux exploiter le pyruvate, une petite molécule énergétique présente dans le sang. Lorsque les chercheurs ont supprimé lrgAB en plus de Fsr, la surcroissance du biofilm a disparu, ce qui indique un rôle clé de cette voie métabolique dans l’alimentation de l’infection envahissante. Il est notable que les biofilms déficients en Fsr étaient aussi plus difficiles à traiter. Chez des rats traités par la gentamicine, les infections à bactéries normales ont régressé et le nombre de plaquettes — un marqueur de la sévérité — s’est amélioré. En revanche, les infections déficientes en Fsr ont à peine répondu, bien que les bactéries n’affichaient pas de résistance accrue aux antimicrobiens dans les tests standards de laboratoire.
Une torsion spécifique à l’humain dans l’inflammation
L’étude a aussi mis au jour un mécanisme potentiel par lequel ces bactéries peuvent déclencher l’inflammation chez l’homme. L’enzyme GelE peut cliver le précurseur humain du signal immunitaire IL‑1β en une forme active qui déclenche des réponses inflammatoires. De façon intrigante, GelE clivait différemment l’IL‑1β du rat, la dégradant plutôt que l’activant, et la coupure précise d’activation était absente des protéines de rat et de souris. Cet effet spécifique à l’espèce suggère que chez l’humain, GelE pourrait concentrer l’inflammation au bord du biofilm, aggravant possiblement les lésions tissulaires lors de l’endocardite.
Du laboratoire au chevet : pourquoi la perte de Fsr importe pour les patients
Pour déterminer si ces résultats expérimentaux avaient une portée clinique, les chercheurs ont analysé des isolats d’E. faecalis provenant de 81 patients atteints d’endocardite infectieuse en Suisse et aux États‑Unis. Près de la moitié des souches étaient dépourvues naturellement du système Fsr. Les patients infectés par ces souches Fsr‑négatives présentaient une bactériémie plus prolongée — plus de jours avec des bactéries détectables dans le sang — et avaient plus de chances d’appartenir à une catégorie de haute gravité incluant soins intensifs, hospitalisations prolongées, interventions cardiaques majeures ou décès. D’autres gènes de virulence n’expliquaient pas ce schéma, pointant directement la perte de Fsr comme marqueur clé d’une maladie plus agressive.
Pourquoi cela compte pour les traitements futurs
Pris ensemble, ces résultats renversent l’idée simpliste selon laquelle bloquer la communication bactérienne affaiblira systématiquement les infections. Dans l’endocardite à E. faecalis, le système Fsr freine en réalité l’expansion du biofilm et rend les bactéries plus vulnérables aux antibiotiques. En l’absence de Fsr, les bactéries forment des biofilms plus denses, exploitent plus efficacement les nutriments sanguins et favorisent des infections tenaces et prolongées. Pour les patients, cela signifie que les souches dépourvues de Fsr peuvent prédire une maladie plus difficile à traiter, et que des thérapies qui ferment aveuglément le quorum sensing pourraient se retourner contre nous dans ce contexte. À la place, cibler finement des voies métaboliques comme l’utilisation du pyruvate, ou surveiller le statut de Fsr et GelE comme marqueurs pronostiques, pourrait offrir de meilleures stratégies pour gérer ces infections cardiaques dangereuses.
Citation: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Mots-clés: endocardite infectieuse, biofilms bactériens, quorum sensing, Enterococcus faecalis, tolérance aux antibiotiques