Clear Sky Science · fr
Principes biochimiques du ciblage des miARN chez la mouche
Petits messages ARN qui orientent les cellules de la mouche
À l’intérieur de chaque cellule de la drosophile, de minuscules molécules appelées microARN agissent comme des inspecteurs de qualité, décidant quels messages génétiques seront traduits en protéines et lesquels seront silencés. Cette étude pose une question apparemment simple : comment ces microARN reconnaissent-ils exactement leurs cibles chez la mouche ? En y répondant, les auteurs nous rapprochent de la capacité à prédire, à partir de la seule séquence, quels gènes seront activés ou réprimés pendant le développement, le comportement et la maladie.
Comment de petits ARN réduisent l’expression des gènes
Les microARN sont de courts fragments d’ARN, d’environ 22 unités, qui s’associent à une protéine appelée Argonaute 1 (Ago1) chez la mouche. Ensemble, ils scrutent des ARN messagers (ARNm) beaucoup plus longs, qui portent les instructions de fabrication des protéines. Lorsqu’un microARN trouve une région partiellement complémentaire sur un ARNm, le complexe Ago1 peut soit cliver l’ARNm, soit bloquer sa traduction en protéine, réduisant ainsi la production génique. Chez les mammifères, les règles de reconnaissance ont été cartographiées en détail, révélant une surprenante variété de modalités d’accrochage des microARN à leurs cibles. En revanche, ces règles chez la mouche sont restées moins claires, alors même que les microARN y contrôlent des processus clés tels que la croissance, la chronologie du développement et les cycles veille-sommeil.
Un test de liaison à haut débit
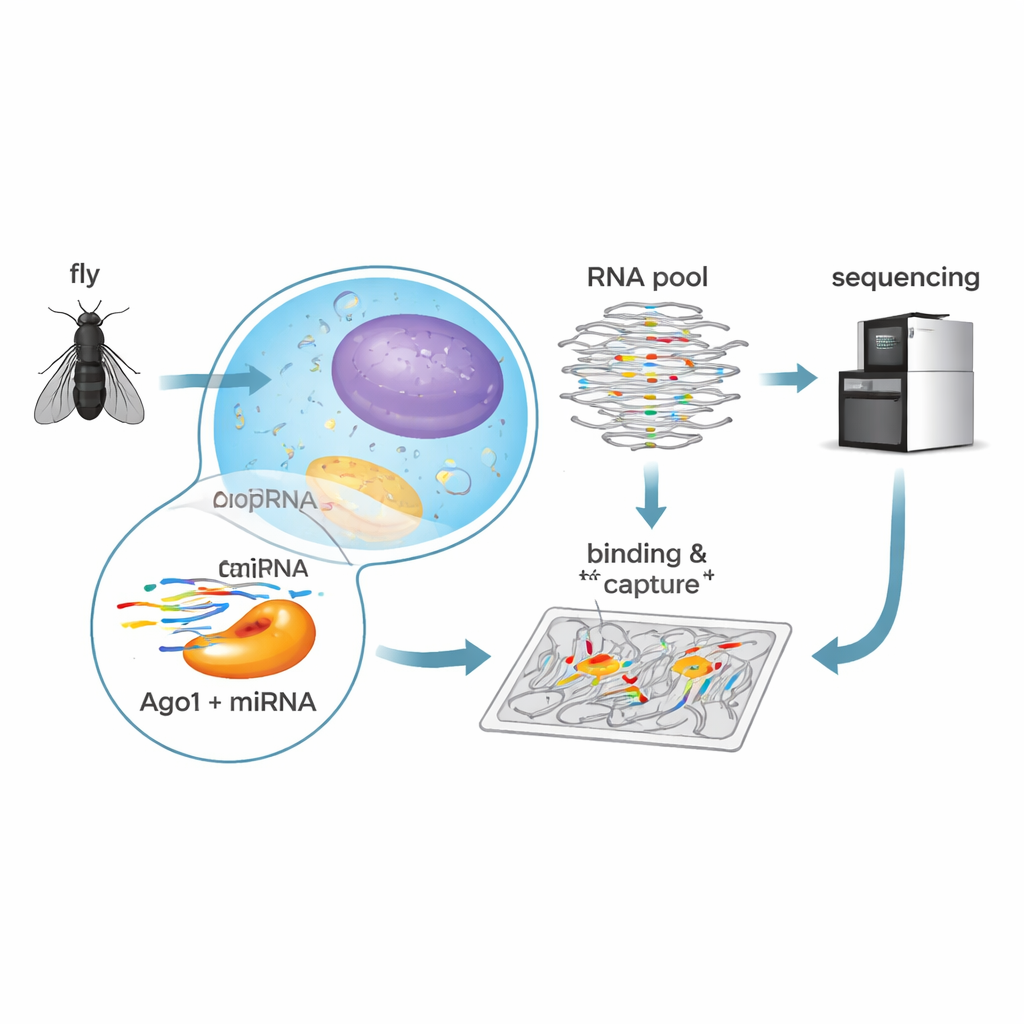
Pour décoder ces règles chez la drosophile, les chercheurs ont utilisé une méthode biochimique appelée RNA Bind-n-Seq. Ils ont chargé l’Ago1 purifié de la mouche avec l’un des cinq microARN abondants — let-7, bantam, miR-184, miR-11 ou miR-124 — chacun ayant des rôles connus dans le développement et la fonction cérébrale. Ils ont ensuite mélangé chaque complexe Ago1–microARN avec une vaste bibliothèque d’ARN synthétiques contenant des séquences aléatoires. Après incubation pour permettre la liaison, ils ont séparé les ARN liés des non liés, séquencé les molécules liées et utilisé des modèles statistiques pour calculer la force d’affinité de chaque type de séquence. Cette approche a fourni des mesures quantitatives d’affinité pour des centaines de motifs cibles distincts en une seule série d’expériences.
Des règles simples avec quelques exceptions astucieuses
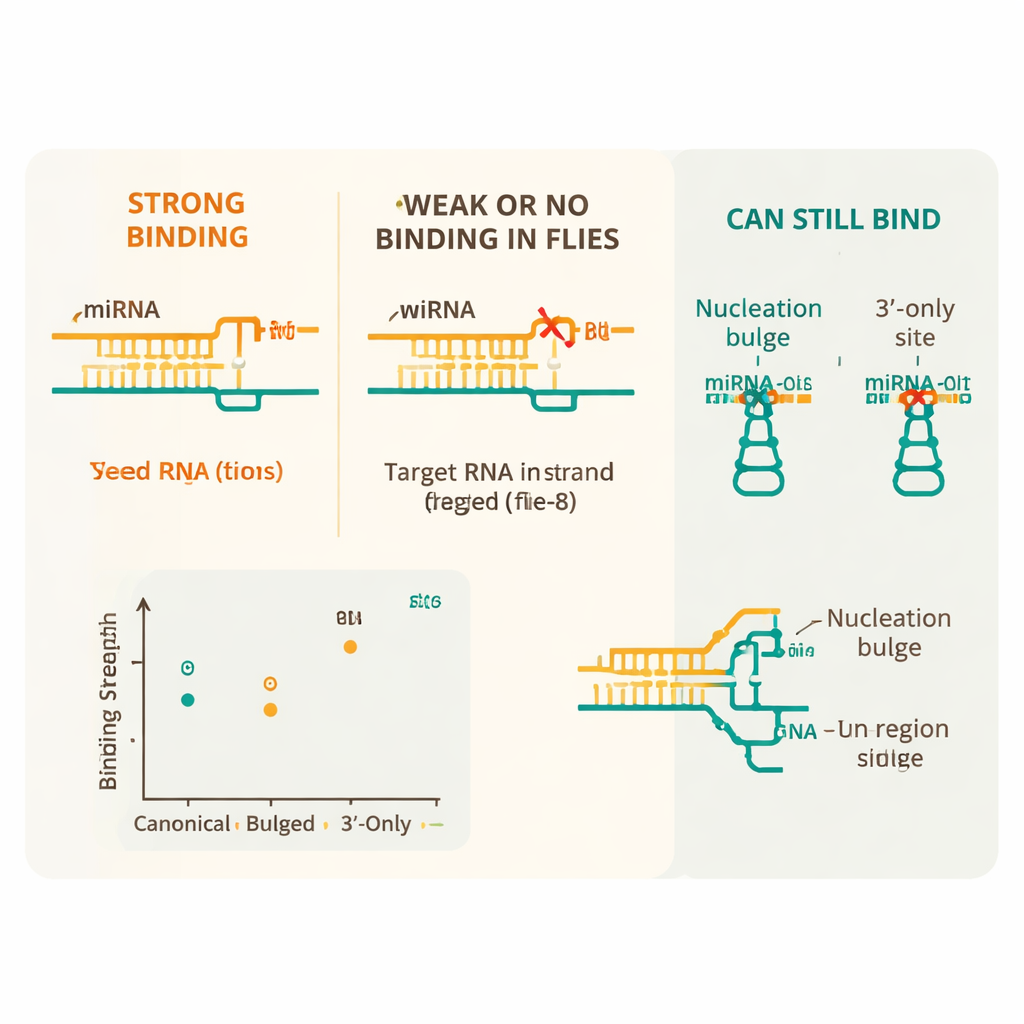
Les résultats montrent que les microARN de la mouche suivent un cahier des charges plus strict que leurs homologues mammaliens. La caractéristique la plus importante est une région « seed » — positions 2 à 8 du microARN — qui doit s’apparier presque parfaitement avec l’ARNm pour une liaison forte. Les sites canoniques appariés au seed, en particulier ceux avec huit bases correspondantes et un nucléotide adjacent spécifique, présentent la plus grande affinité. En revanche, même une seule paire bancale du mauvais type (une paire dite G:U) au sein de ce seed réduit fortement la liaison, et deux imperfections ou plus rendent l’interaction indiscernable du bruit de fond. Les mésappariements au milieu du seed sont particulièrement délétères, soulignant la sensibilité avec laquelle Ago1 lit ce segment central.
Flexibilité cachée au-delà de l’appariement central
Malgré cette rigidité générale, l’étude a mis au jour plusieurs soupapes d’échappement importantes qui permettent à certains sites imparfaits d’être tout de même reconnus. Un appariement supplémentaire entre l’extrémité 3′ du microARN et l’ARNm peut compenser une seule faute dans le seed, restaurant une liaison forte. Certaines configurations particulières, appelées bulges de nucléation — où un nucléotide supplémentaire fait saillie près du seed — se lient également presque aussi bien que les sites standards. L’équipe a montré par ailleurs que Ago1 peut reconnaître des sites « uniquement 3′ », où le seed n’est pas impliqué mais où l’extrémité 3′ du microARN s’apparie fortement, et qu’il peut cliver efficacement des cibles avec de longs appariements centraux. Enfin, ils ont constaté que le contexte séquentiel environnant importe : les sites entourés de régions riches en A et U, qui tendent à maintenir l’ARN non structuré et accessible, se lient plus fortement que les mêmes sites enfouis dans des contextes séquentiels plus rigides.
Pourquoi ces règles comptent pour la biologie de la mouche
Pris ensemble, ces résultats montrent que les microARN de la mouche exigent généralement des appariements quasi parfaits dans leur region seed, avec seulement un nombre limité d’exceptions tolérées. Ce jeu de règles plus simple et plus strict contraste avec la flexibilité plus large observée chez les mammifères. En fournissant des valeurs quantitatives sur la force d’affinité des différents motifs cibles, ce travail prépare le terrain pour des outils informatiques de nouvelle génération capables de prédire plus précisément quels gènes de la mouche seront contrôlés par quels microARN. Pour le grand public, la conclusion est que la régulation génique chez la mouche, bien que guidée par de minuscules ARN, obéit à des principes biochimiques clairs — principes qui peuvent désormais être utilisés pour comprendre et, éventuellement, manipuler des traits complexes tels que le développement, le comportement et la résistance aux maladies.
Citation: Vega-Badillo, J., Zamore, P.D. & Jouravleva, K. Biochemical principles of miRNA targeting in flies. Nat Commun 17, 1641 (2026). https://doi.org/10.1038/s41467-026-68360-0
Mots-clés: microARN, Drosophila, Argonaute, liaison à l'ARN, régulation génique