Clear Sky Science · fr
Élimination guidée par signature transcriptomique des cellules épithéliales alvéolaires intermédiaires atténue la fibrose pulmonaire chez la souris
Pourquoi les poumons cicatrisés comptent
La fibrose pulmonaire est une maladie grave des poumons dans laquelle les alvéoles délicates se transforment progressivement en tissu cicatriciel rigide, rendant chaque respiration pénible. Les médecins savent que cette cicatrisation commence lorsque les processus normaux de réparation dérapent, mais il était peu clair quelles cellules spécifiques en sont responsables et comment les éliminer sans endommager le tissu pulmonaire sain. Cette étude explore une nouvelle manière de « lire » les messages moléculaires à l’intérieur des cellules pulmonaires, d’utiliser ces informations pour identifier les cellules transitionnelles nocives et de les éliminer sélectivement afin de réduire la cicatrisation chez la souris.
Des cellules prises en flagrant délit de réparation défectueuse
Après une blessure pulmonaire, des cellules productrices de surfactant appelées cellules de type II se multiplient normalement puis mûrissent en cellules de type I fines qui tapissent les alvéoles et permettent le passage de l’oxygène dans le sang. Dans la fibrose, beaucoup de ces cellules restent coincées dans un état intermédiaire, ou transitionnel, au lieu d’achever cette transformation. Des études antérieures de séquençage ARN unicellulaire avaient détecté ces cellules intermédiaires chez la souris et chez l’humain, mais il n’était pas clair si elles étaient de simples témoins ou des acteurs clés de la maladie. Les auteurs se sont concentrés sur un type cellulaire transitionnel de souris appelé Krt8+ alvéolar differentiation intermediates, et sur leurs homologues humains connus sous le nom de cellules basaloïdes aberrantes, qui apparaissent en grand nombre dans les poumons cicatrisés.
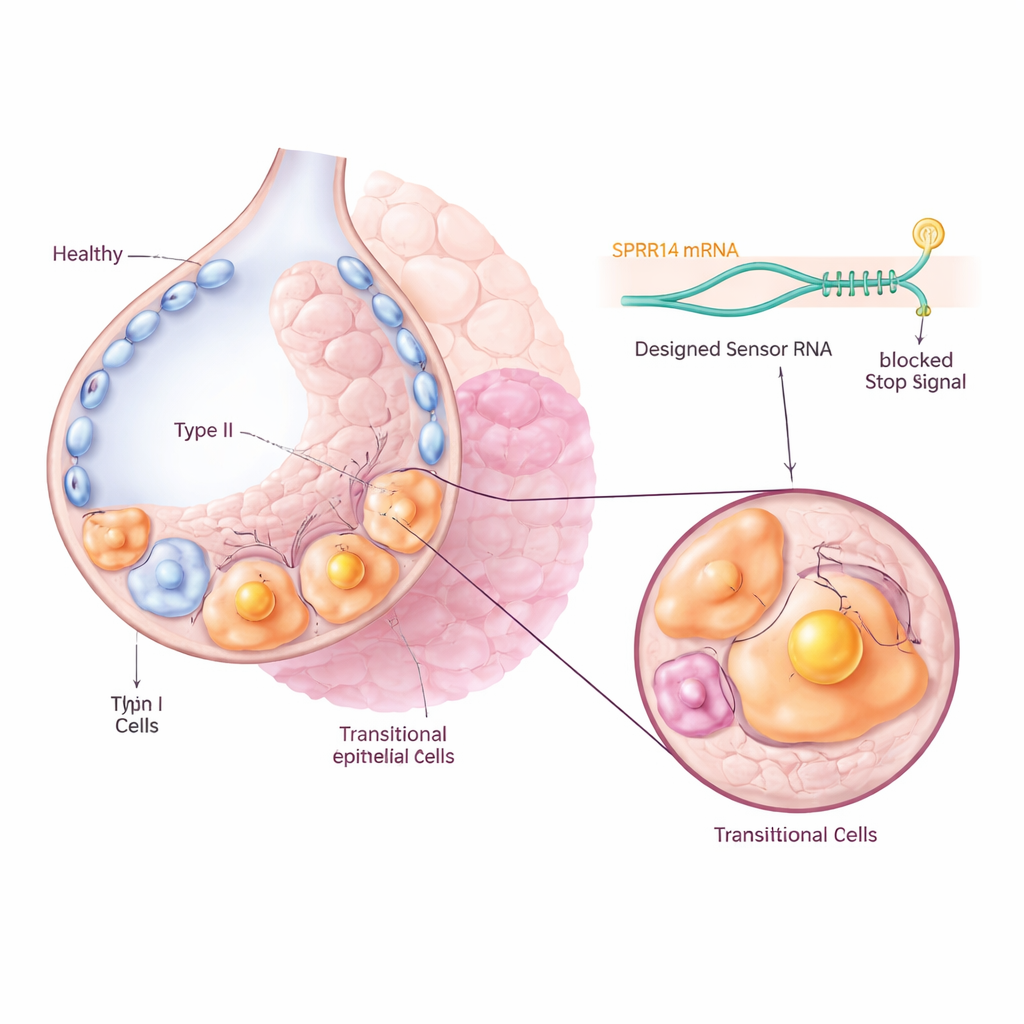
Trouver une étiquette moléculaire unique
Pour cibler ces cellules problématiques sans toucher leurs voisines saines, l’équipe a d’abord cherché dans de larges jeux de données d’expression génique un marqueur fortement et spécifiquement exprimé dans la population transitionnelle. Ils ont identifié une molécule appelée SPRR1A comme une « étiquette » remarquable : elle était fortement enrichie dans les cellules intermédiaires Krt8+ des poumons fibrosés de souris, et dans les cellules basaloïdes aberrantes KRT5-/KRT17+ de patients atteints de fibrose pulmonaire idiopathique, mais largement absente des cellules pulmonaires normales. La microscopie des tissus pulmonaires de souris et d’humain a confirmé que SPRR1A apparaissait principalement dans les régions lésées et remodelées, et non dans les alvéoles saines, ce qui suggère qu’elle pourrait servir de poignée précise pour identifier les cellules en cause.
Programmer les cellules avec un capteur d’ARN
Les chercheurs ont ensuite utilisé une technologie récemment développée appelée CellREADR, qui agit comme un capteur moléculaire interne. Ils ont conçu de courtes séquences d’ARN capables d’apparier leurs bases à l’ARN SPRR1A à l’intérieur d’une cellule. Lorsque le capteur détecte SPRR1A, il déclenche la production d’une protéine « effectrice » attachée, telle qu’un marqueur fluorescent ou un récepteur rendant la cellule sensible à un médicament. Chez la souris, des virus ont servi à délivrer ces constructions capteur–effecteur aux cellules pulmonaires. Seules les cellules produisant activement SPRR1A ont activé le signal fluorescent, permettant à l’équipe de suivre et d’isoler directement les cellules transitionnelles provenant de poumons fibrosés. Le séquençage unicellulaire a montré que les cellules marquées correspondaient étroitement au profil génique transitionnel connu, confirmant que le capteur d’ARN ciblait avec précision la population visée.
Éteindre les intermédiaires nocifs
Puis, l’effecteur a été remplacé par le récepteur de la toxine diphtérique au lieu d’une protéine fluorescente inoffensive, de sorte que les cellules SPRR1A-positives puissent être tuées sélectivement en administrant la toxine diphtérique. En synchronisant le traitement avec le pic d’abondance des cellules transitionnelles après une lésion chimique des poumons, les auteurs ont pu éliminer environ un tiers de cette population. Cette déplétion ciblée a entraîné une réduction spectaculaire de la cicatrisation pulmonaire : moins d’accumulation de collagène, des niveaux réduits de protéines fibrosantes et des structures alvéolaires d’apparence plus normale. Des analyses détaillées ont montré que la plupart des cellules SPRR1A-positives portaient des signes d’un état de stress proche de la sénescence, avec un petit sous-ensemble capable d’une prolifération élevée, suggérant que ces intermédiaires échouent à réparer correctement le tissu tout en contribuant à entretenir le processus fibrotiques.
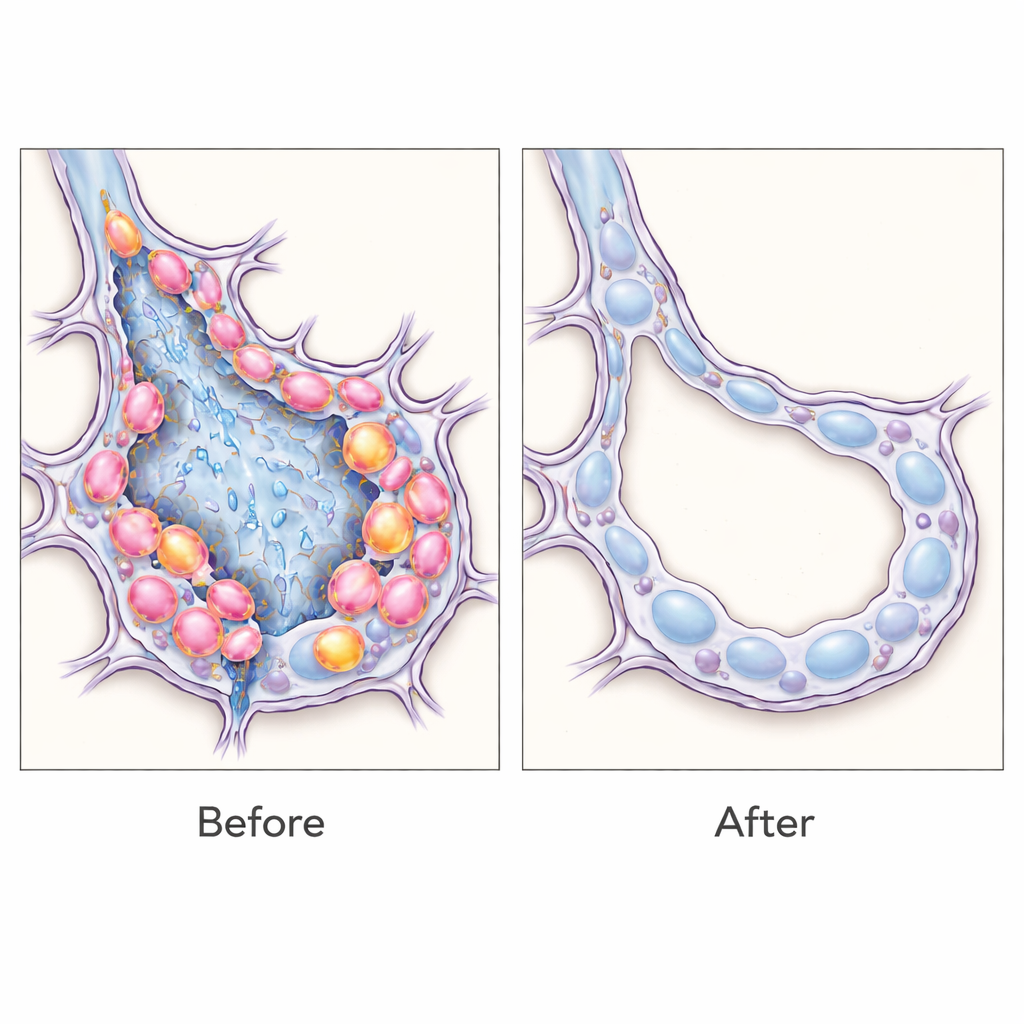
Ce que cela implique pour les traitements futurs
Ces résultats plaident en faveur de l’idée que les cellules épithéliales transitionnelles ne sont pas de simples marqueurs mais des moteurs actifs de la fibrose pulmonaire, et que leur élimination sélective peut réorienter l’équilibre vers une architecture pulmonaire plus saine chez la souris. Plus largement, ce travail démontre une stratégie flexible : en « lisant » des signatures ARN spécifiques aux cellules, les chercheurs peuvent marquer, étudier et même éliminer des populations cellulaires étroitement définies dans les tissus vivants sans créer à chaque fois des lignées animales sur mesure. Bien que beaucoup de travail reste à faire avant que de tels outils de détection ARN puissent être adaptés en toute sécurité chez l’humain, cette approche ouvre une voie vers des thérapies de précision ciblant les types cellulaires exacts qui font dérailler la réparation dans la cicatrisation pulmonaire chronique et, potentiellement, dans d’autres maladies fibrotiques.
Citation: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Mots-clés: fibrose pulmonaire, cellules épithéliales alvéolaires, séquençage ARN unicellulaire, technologie de détection ARN, sénescence cellulaire