Clear Sky Science · fr
Atlas des noyaux uniques de l’amygdale centrale révélant la dynamique de la chromatine et de la transcription génique dans le trouble lié à l’usage d’alcool
Pourquoi cette recherche importe dans la vie quotidienne
Le trouble lié à l’usage d’alcool (TUA) touche des millions de personnes et leurs proches, et pourtant nous savons encore étonnamment peu sur les effets du consommations lourdes et prolongées sur le cerveau humain au niveau des cellules individuelles. Cette étude se concentre sur une petite mais essentielle région — l’amygdale centrale, un nœud pour la peur, le stress et la motivation — pour cartographier comment l’alcool remodèle les cellules cérébrales et leurs systèmes de contrôle génétique. En associant des méthodes de séquençage « unicellulaire » de pointe à des études génétiques du risque d’addiction, les auteurs commencent à expliquer pourquoi certaines personnes sont plus vulnérables au TUA et comment l’alcool laisse des cicatrices moléculaires durables dans le cerveau.
Observation rapprochée d’un petit nœud cérébral
L’amygdale centrale est une station de sortie clé du réseau émotionnel et de stress du cerveau, fortement liée au soulagement de l’anxiété, au désir et à l’usage compulsif d’alcool. Dans ce travail, les chercheurs ont analysé environ 175 000 noyaux cellulaires individuels prélevés à l’autopsie dans l’amygdale centrale de 50 personnes — 22 avec antécédent de trouble lié à l’usage d’alcool et 28 sans TUA. En utilisant une technologie qui lit à la fois l’activité génique (ARN) et l’accessibilité de la chromatine (le degré d’« ouverture » ou de « fermeture » de l’ADN) dans la même cellule, ils ont construit un atlas détaillé de tous les principaux types cellulaires de cette région, y compris plusieurs types de neurones et des cellules de soutien comme les astrocytes et les microglies. Ils ont constaté que les neurones inhibiteurs — qui atténuent ou sculptent l’activité cérébrale — sont particulièrement abondants dans l’amygdale centrale et semblent particulièrement affectés chez les personnes atteintes de TUA. 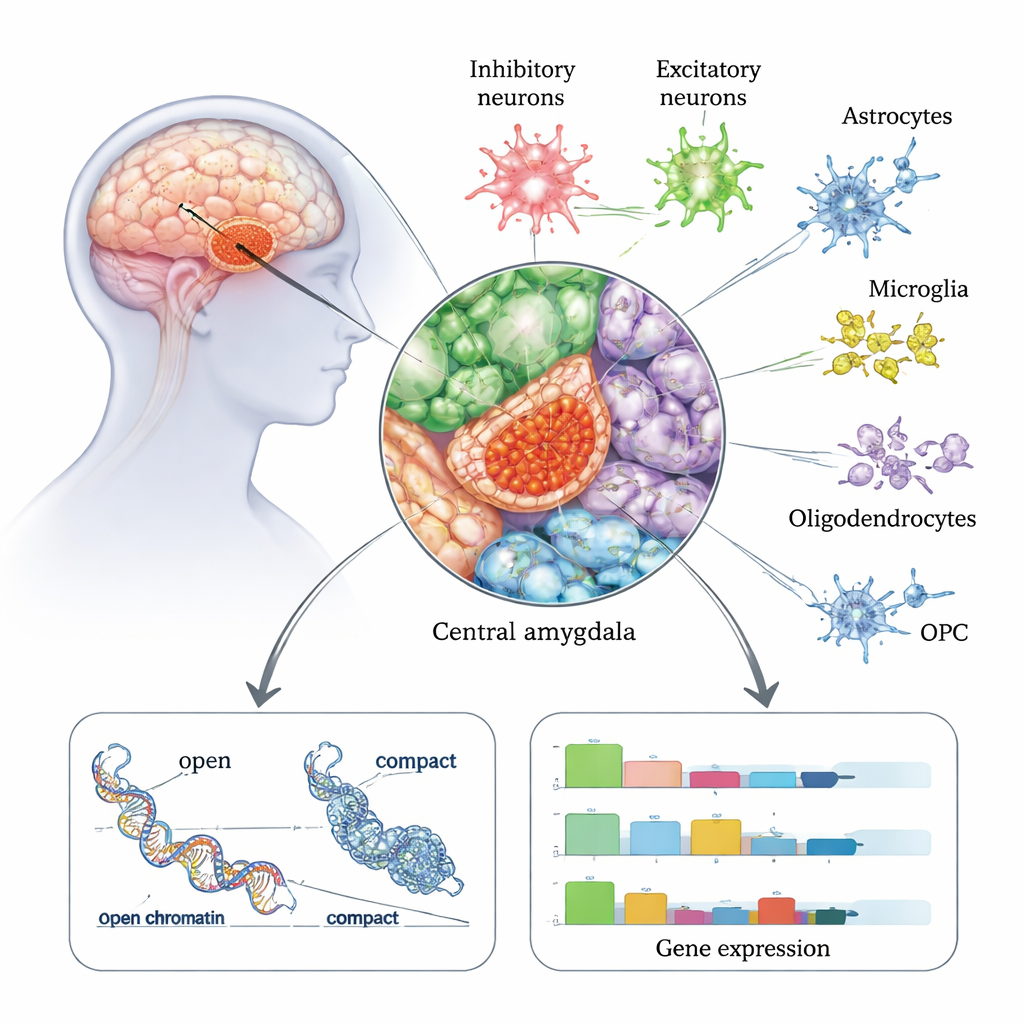
Quelles cellules et quels gènes changent dans le trouble lié à l’usage d’alcool ?
L’équipe a comparé systématiquement l’activité génique chez les personnes avec et sans TUA, type cellulaire par type cellulaire. Ils ont identifié plus de 1 800 gènes dont l’activité était modifiée dans des populations cellulaires spécifiques, les plus grands changements se produisant dans les neurones inhibiteurs, suivis des neurones excitateurs et des astrocytes. Un sous-type de neurone inhibiteur marqué par le peptide proenképhaline (PENK) a montré des altérations particulièrement marquées. De nombreux gènes affectés participent à la communication entre cellules cérébrales, en particulier l’équilibre entre le signal excitateur glutamate et le signal inhibiteur GABA. Par exemple, le gène GABRA2, qui contribue à former un type majeur de récepteur GABA, était augmenté dans certains neurones inhibiteurs, tandis que GRM8, un récepteur au glutamate, et NCAM1, une molécule d’adhésion cellulaire importante pour les synapses, évoluaient en sens opposés selon les sous-types neuronaux. Ces motifs suggèrent que le réglage fin de l’excitation et de l’inhibition dans l’amygdale centrale est perturbé dans le TUA.
Les commutateurs de contrôle du cerveau : chromatine et éléments régulateurs
Les gènes n’agissent pas seuls ; ils sont contrôlés par des segments d’ADN qui fonctionnent comme des interrupteurs et des variateurs. En examinant la chromatine — la manière dont l’ADN est emballé — les chercheurs ont identifié plus d’un demi-million d’éléments régulateurs candidats et les ont liés à des gènes proches de façon spécifique à chaque type cellulaire. Près de la moitié de ces éléments étaient uniques à un seul type cellulaire, soulignant la spécialisation des différentes cellules cérébrales. Beaucoup d’éléments régulateurs modifiés dans le TUA étaient connectés à des gènes impliqués dans la gestion du calcium et la signalisation du glutamate, tels que CALN1, un gène liant le calcium fortement actif dans les neurones. Dans les neurones inhibiteurs, CALN1 présentait à la fois une expression accrue et des grappes denses de boucles régulatrices, ce qui implique que l’exposition à l’alcool remodèle l’architecture locale de l’ADN contrôlant ce gène. 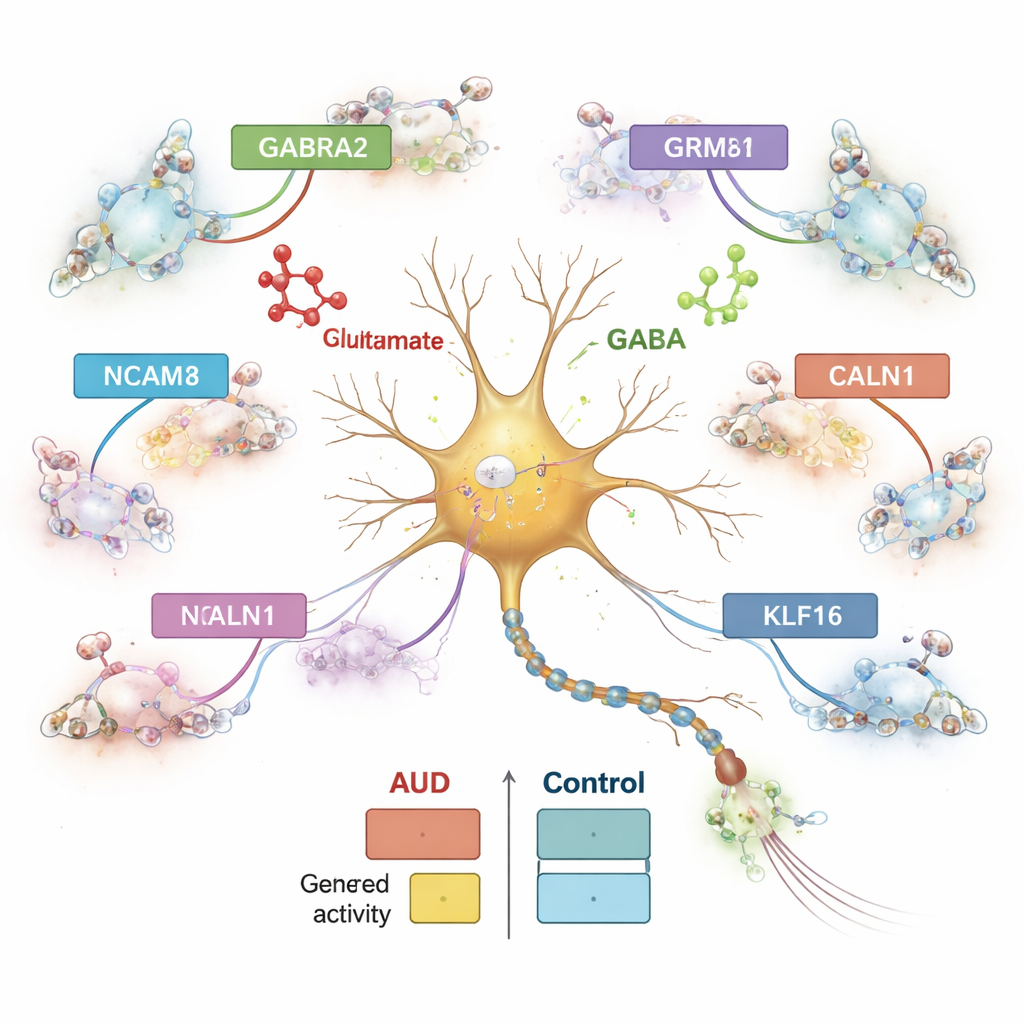
Des gènes de risque aux changements cérébraux réels
Les études génétiques ont identifié de nombreuses variantes d’ADN qui augmentent le risque de développer des problèmes liés à l’alcool, mais où et comment elles agissent dans le cerveau restait flou. En superposant leurs cartes unicellulaires à de larges études d’association pangénomique portant sur l’usage problématique d’alcool, les auteurs ont trouvé que les gènes de risque sont disproportionnellement actifs et dysrégulés dans les neurones de l’amygdale centrale, en particulier les neurones inhibiteurs. Ils ont identifié plus de 200 variantes de risque susceptibles d’être causales situées à l’intérieur d’éléments régulateurs ouverts dans des types cellulaires spécifiques. Certaines se situaient dans ou à proximité de gènes déjà associés à l’addiction, tels que CACNA1C et DRD2, qui contribuent à contrôler l’excitabilité neuronale et la signalisation dopaminergique. D’autres, y compris SEMA6D et NF1, ont émergé comme nouveaux candidats. L’équipe a également identifié une famille de facteurs de transcription appelée facteurs Kruppel-like (notamment KLF16) qui semblent coordonner des changements étendus dans les gènes liés au calcium et au glutamate, et ils ont confirmé des éléments de ce réseau régulateur dans un modèle murin d’exposition alcoolique aiguë.
Ce que cela signifie pour la compréhension et le traitement du TUA
En termes simples, cette étude montre que le trouble lié à l’usage d’alcool n’est pas seulement un problème diffus du cerveau mais une perturbation hautement organisée concentrée dans des types cellulaires et des voies moléculaires particulières au sein d’un centre émotionnel critique. Les neurones inhibiteurs de l’amygdale centrale, ainsi que les astrocytes et d’autres cellules de soutien, présentent des changements coordonnés de l’activité génique et des interrupteurs d’ADN qui contrôlent ces gènes — en particulier dans les systèmes qui régulent le glutamate, le GABA et les signaux calciques. En reliant ces changements cellulaires à des variants de risque génétique, le travail offre une feuille de route reliant une vulnérabilité héréditaire à des événements moléculaires concrets dans le cerveau. Avec le temps, de telles cartes spécifiques aux cellules pourront guider le développement de traitements plus précis qui restaurent l’équilibre entre excitation et inhibition, plutôt que d’agir de manière globale sur l’ensemble du cerveau.
Citation: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Mots-clés: trouble lié à l’usage d’alcool, amygdale centrale, génomique unicellulaire, neurones inhibiteurs, régulation des gènes