Clear Sky Science · fr
De la formation du complexe TDP-43/ARN à l’agrégation pathologique de TDP-43 : approche structurale et cellulaire
Pourquoi cette protéine cérébrale est importante
Les maladies neurodégénératives, comme la sclérose latérale amyotrophique (SLA) et la démence frontotemporale, présentent souvent des amas de protéines mal repliées à l’intérieur des cellules nerveuses. L’un des coupables les plus fréquents est une protéine appelée TDP-43, qui aide normalement au traitement de l’ARN — la copie active de nos gènes. Cette étude pose une question cruciale : que fait TDP-43 dans les cellules saines et qu’est-ce qui dysfonctionne pour transformer cet assistant utile de l’ARN en une protéine toxique formant des agrégats ?
Comment TDP-43 fonctionne dans les cellules nerveuses saines
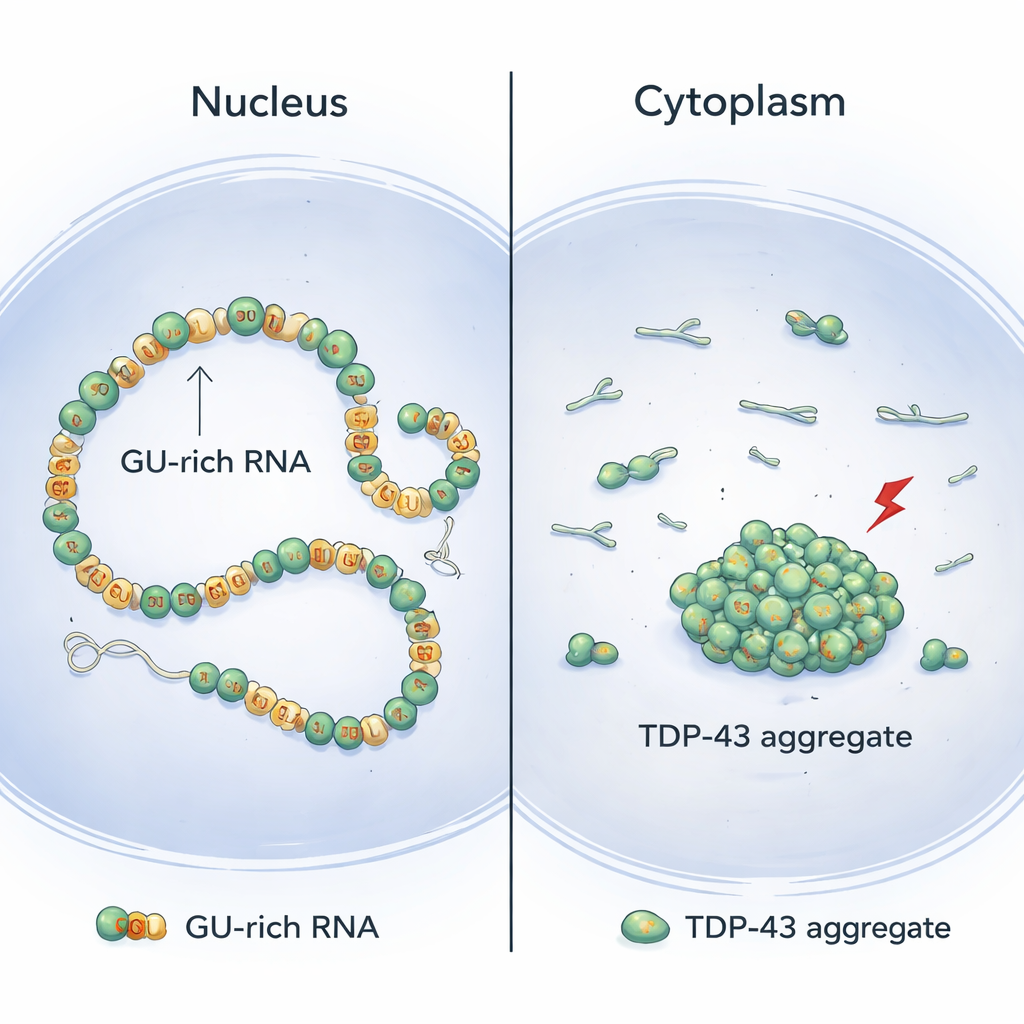
TDP-43 réside habituellement dans le noyau cellulaire, où il se lie à de longs segments d’ARN riches en répétitions « GU ». En combinant biologie structurale et expériences cellulaires, les auteurs montrent que les molécules de TDP-43 s’alignent de façon coopérative le long de ces régions riches en GU, formant des chaînes continues et régulières sur l’ARN. Ainsi disposés, l’extrémité avant de la protéine — son domaine N-terminal — reste physiquement séparée entre molécules voisines. En conséquence, ces segments N-terminaux demeurent disponibles pour atteindre et relier des sections éloignées riches en GU du même ARN, en bouclant et compactant doucement de longs introns (les régions non codantes à l’intérieur des gènes) sans former d’amas.
Une lutte interne intégrée dans la protéine
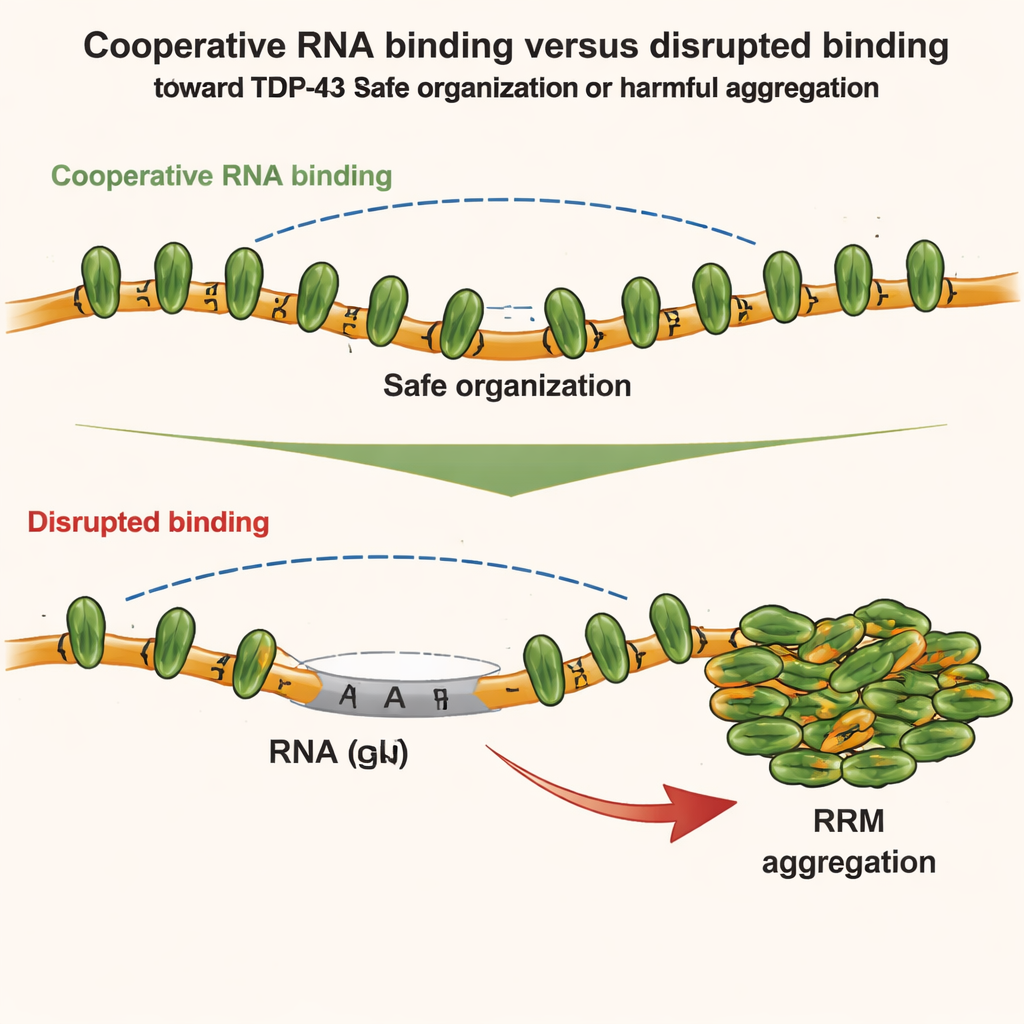
L’équipe a ensuite exploré comment les différentes parties de TDP-43 se concurrencent ou coopèrent. Ils se sont concentrés sur deux régions : le domaine N-terminal, qui peut s’attacher à d’autres domaines N-terminaux, et les modules centraux de liaison à l’ARN, qui favorisent la liaison coopérative le long des ARN riches en GU. À l’aide de techniques sensibles comme la spectroscopie RMN, la calorimétrie et la diffusion des rayons X aux petits angles, ils ont constaté que lorsque TDP-43 se lie de façon coopérative à l’ARN, la géométrie de la chaîne affaiblit en réalité les contacts directs N-terminal–N-terminal entre molécules adjacentes. Autrement dit, une forte liaison coopérative à l’ARN limite les interactions N-terminal locales. Mais lorsque cette coopération est rompue — par exemple en insérant des segments non-GU dans l’ARN ou en mutant TDP-43 — les régions N-terminal des protéines voisines se rapprochent et peuvent alors se lier entre elles.
De la compaction utile au regroupement nocif
Ces observations structurales ont été testées dans des cellules vivantes. Les auteurs ont utilisé des systèmes cellulaires conçus pour suivre comment différents mutants de TDP-43 se mélangent ou se séparent à l’intérieur de compartiments artificiels riches en ARN. Ils ont découvert que la liaison coopérative à l’ARN et les interactions N-terminal favorisent toutes deux l’organisation de TDP-43 en assemblages d’ordre supérieur, mais de manières différentes. La liaison coopérative aligne les protéines le long d’ARN riches en GU, tandis que les contacts N-terminaux relient des grappes distantes. Cependant, sous stress oxydatif modéré, le tableau change. Un agent de stress chimique (l’arsénite) provoque des modifications chimiques spécifiques — des acétylations — sur les motifs centraux de liaison à l’ARN, les rendant susceptibles de s’agglutiner. Si la liaison coopérative à l’ARN est intacte, TDP-43 reste majoritairement soluble. Si la coopération est affaiblie, les liaisons N-terminal entre molécules voisines servent d’échafaudage qui rapproche les noyaux acétylés, favorisant une agrégation irréversible.
Pourquoi TDP-43 s’agrège davantage dans le cytoplasme
Le modèle issu de ce travail aide à expliquer pourquoi les agrégats de TDP-43 se trouvent souvent dans le cytoplasme des neurones malades plutôt que dans le noyau. Dans le noyau, les longs introns contenant de nombreuses répétitions GU sont fréquents, favorisant une liaison continue et coopérative qui maintient faibles les contacts N-terminaux risqués entre voisins et permet des boucles sûres à longue portée. Dans le cytoplasme, en revanche, les ARN matures ont beaucoup moins de régions riches en GU. Cela rend la liaison de TDP-43 plus parcellaire et moins coopérative, augmentant les chances que les domaines N-terminaux voisins interagissent et préparent le terrain pour l’agrégation lorsque des modifications chimiques induites par le stress surviennent. À l’appui de ce point de vue, l’apport artificiel d’introns supplémentaires riches en GU dans le noyau a réduit l’agrégation de TDP-43 sous stress.
Ce que cela implique pour les thérapies futures
En bref, l’étude décrit TDP-43 comme une protéine en équilibre entre une organisation utile de l’ARN et un regroupement nocif, la liaison coopérative aux ARN riches en GU agissant comme un mécanisme de sécurité. Lorsque ce filet de sécurité échoue — en raison d’altérations des séquences d’ARN, de mutations protéiques ou du stress cellulaire — les mêmes domaines qui compactent normalement de longs segments d’ARN peuvent au contraire conduire à la formation d’agrégats toxiques. Pour les non-spécialistes, la conclusion principale est que maintenir le bon type d’interactions entre TDP-43 et l’ARN pourrait être une stratégie prometteuse pour prévenir ou ralentir l’agrégation protéique observée dans la SLA et les maladies cérébrales apparentées.
Citation: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Mots-clés: Agrégation de TDP-43, Protéines liant l’ARN, SLA, Interations protéine–ARN, Neurodégénérescence