Clear Sky Science · fr
Ingénierie de ligands atomiquement précise des nanoparticules d’or via le transfert de masse entre phases
Pourquoi les particules d’or ultrafines comptent pour la santé
L’imagerie médicale repose de plus en plus sur des nanoparticules — des particules minuscules des milliers de fois plus fines qu’un cheveu — pour illuminer des organes et des tumeurs profondément situés dans le corps. Cette étude montre comment les chercheurs peuvent désormais ajuster la couche extérieure de particules d’or ultrasmall presque atome par atome, de sorte que le même noyau lumineux puisse être dirigé vers différents organes, en particulier en passant du foie et de la rate vers les reins. Un tel contrôle pourrait aider à concevoir des agents d’imagerie et des vecteurs médicamenteux plus sûrs qui atteignent exactement les zones ciblées par les médecins et sont éliminés plus proprement par l’organisme.
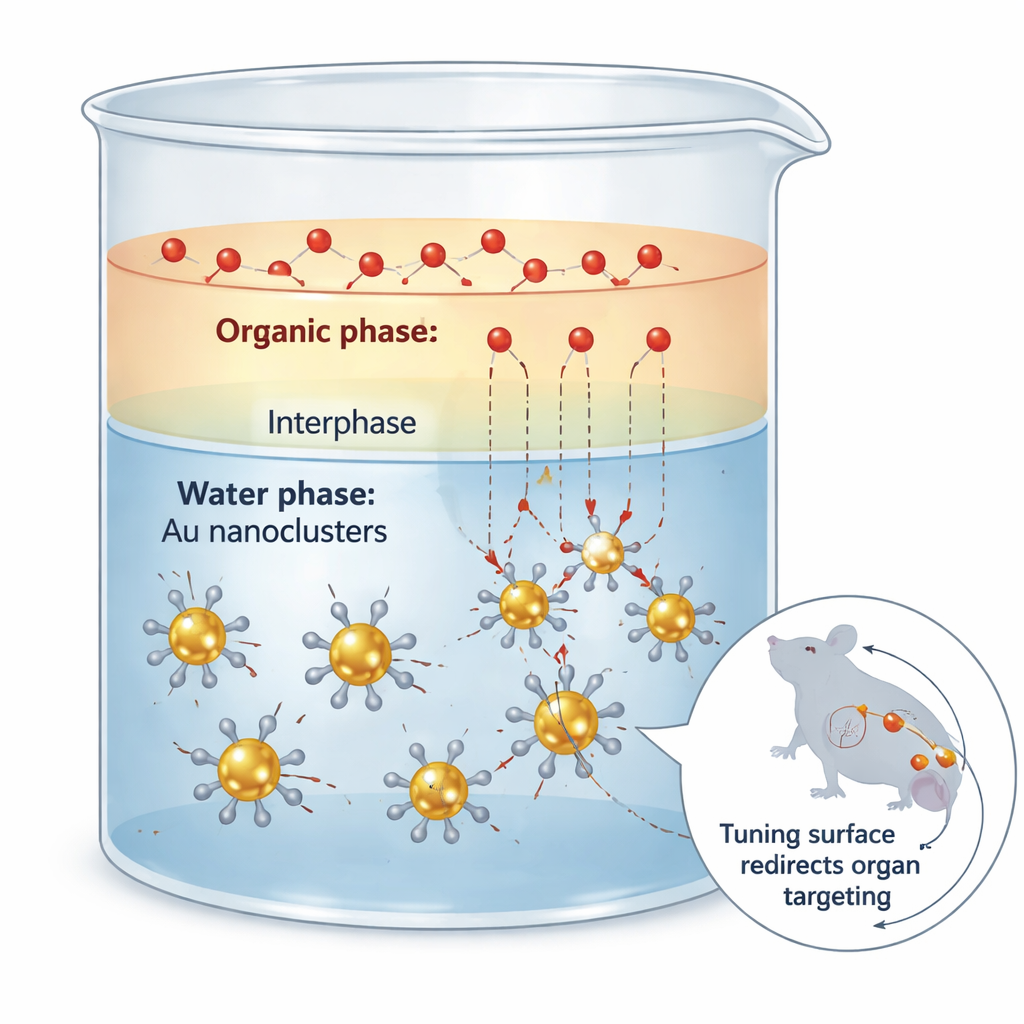
Le défi d’habiller de petits agrégats d’or
Les nanoclusters d’or sont des particules d’or ultra-petites qui se comportent davantage comme de grandes molécules que comme des grains métalliques. Ils peuvent émettre de la lumière dans la fenêtre proche infrarouge II, qui pénètre profondément dans les tissus et fournit des images nettes avec un faible bruit de fond. Cependant, presque tout ce qui détermine le comportement de ces agrégats dans le corps — où ils se déplacent, combien de temps ils circulent et comment ils sont éliminés — dépend non pas de l’or lui‑même, mais des ligands organiques, ou molécules de « coque », attachés à leur surface. Les méthodes traditionnelles pour modifier cette coque agissent souvent comme une chirurgie grossière : la réaction va trop vite, le revêtement devient inégal et le noyau d’or peut être partiellement attaqué, détruisant à la fois la structure et les propriétés optiques.
Ralentir le trafic entre deux liquides
Les chercheurs ont abordé ce problème en exploitant une idée physique simple : la résistance au transfert de masse à la frontière entre deux liquides qui ne se mélangent pas complètement. Ils ont placé les agrégats d’or dans l’eau et les ligands soufrés entrants dans un solvant organique tel que l’acétate d’éthyle. Dans la mince région où les deux liquides se mélangent partiellement, les ligands diffusent lentement vers les agrégats et s’échangent avec la coque d’origine. Des mesures cinétiques précises ont montré que l’« attaque » indésirable du noyau d’or est extrêmement sensible à la concentration en ligand libre, tandis que l’échange souhaité l’est beaucoup moins. En utilisant l’aménagement biphasique pour maintenir des niveaux de ligand libre faibles mais continuellement renouvelés, l’équipe a réduit l’attaque d’environ soixante fois tout en préservant la majeure partie du taux d’échange utile.
Construire une boîte à outils moléculaire précise
Avec cette méthode assistée par l’interface, les auteurs ont pu remplacer les ligands de surface d’un agrégat d’or modèle, Au25, de manière très contrôlée. Ils sont partis d’agrégats protégés par un ligand acide sulfonique chargé négativement et ont introduit une variété de nouveaux thiols portant des acides carboxyliques, des amines, des hydroxyles, des groupes nitro et des cycles aromatiques hydrophobes. La spectrométrie de masse a révélé des mélanges propres et bien définis, tels que des clusters Au25 portant un nombre spécifique de chaque type de ligand, plutôt que des distributions larges et désordonnées. La méthode a également fonctionné pour d’autres tailles d’agrégats et familles de ligands, ce qui suggère qu’il s’agit d’une stratégie générale pour fabriquer des nanoclusters d’or robustes et sur mesure pour différentes applications.
Diriger les nanoparticules du foie vers les reins
Le test le plus spectaculaire de cette précision est venu d’expériences d’imagerie in vivo chez la souris. En introduisant progressivement un ligand chargé positivement, le p-aminothiophénol, dans une coque par ailleurs chargée négativement, l’équipe a créé une série d’agrégats dont la charge de surface globale passait d’un fort négatif à une quasi-zwitterionique (équilibre entre groupes positifs et négatifs). Toutes les versions brillaient de façon similaire en tests de laboratoire, mais leur biodistribution chez la souris différait radicalement. Les agrégats purement négatifs s’accumulaient principalement dans le foie et la rate. À mesure que l’on ajoutait davantage de ligands positifs, le signal dans ces organes diminuait et augmentait dans les reins et la vessie, indiquant une clairance rénale améliorée. Lorsque l’on utilisait à la place un ligand neutre hydroxyle, ce basculement n’apparaissait pas, soulignant le rôle particulier des charges positives pour rediriger les particules.
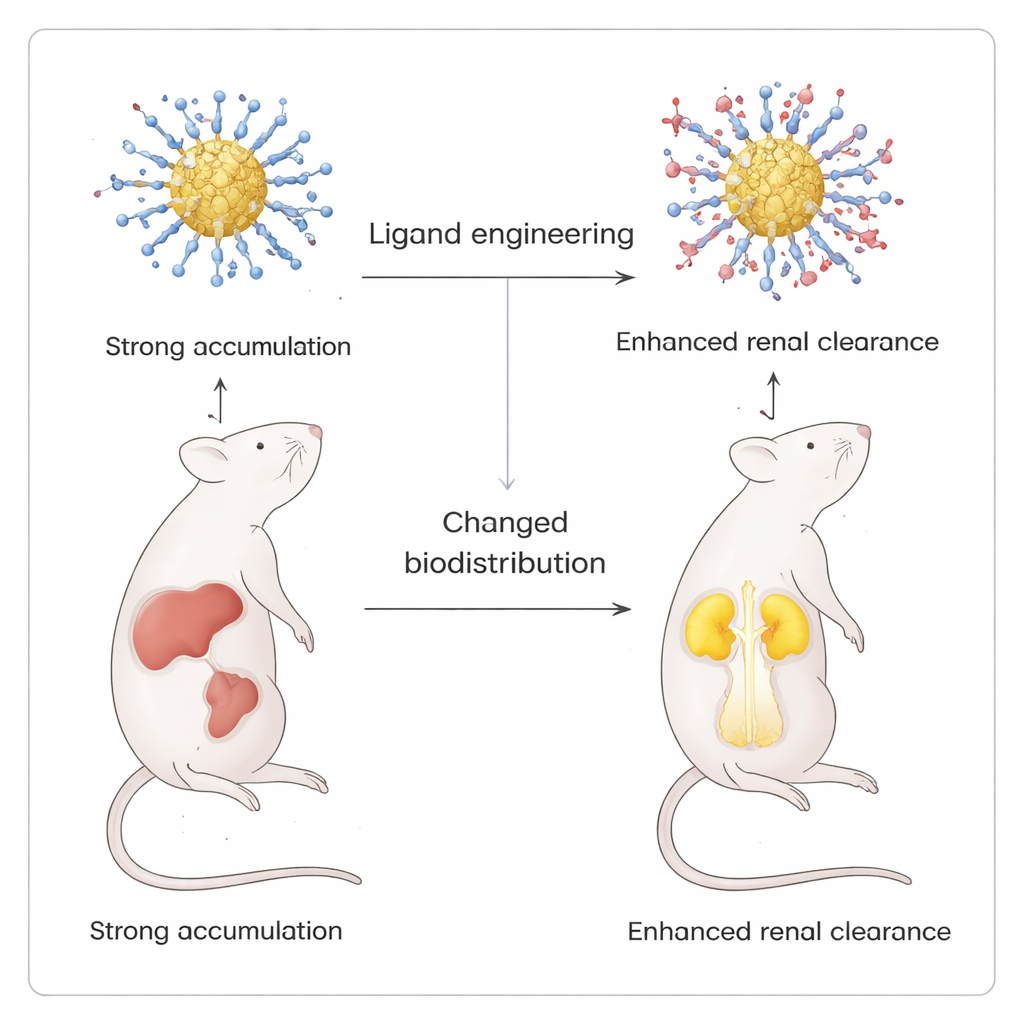
Ce que cela signifie pour les médicaments de demain
Pour le non-spécialiste, l’enseignent clé est que les scientifiques ont trouvé un moyen de « vêtir » des nanoclusters d’or lumineux avec des couches moléculaires pouvant être ajustées presque molécule par molécule, sans endommager la particule sous-jacente. En utilisant une configuration biphasique douce, ils peuvent contrôler à la fois la chimie et le destin final de ces particules dans l’organisme. Ce niveau de maîtrise permet de concevoir des agents d’imagerie et des vecteurs médicamenteux potentiels qui ciblent des organes spécifiques puis s’éliminent par les reins plutôt que de persister dans le foie et la rate, ouvrant la voie à une nanomédecine plus sûre et plus prévisible.
Citation: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Mots-clés: nanoparticules d’or, ingénierie des ligands, bioimagerie, nanomédecine, biodistribution