Clear Sky Science · fr
Un copolymère hydrosoluble pour le stockage et la conversion d’électrons dans l’évolution photocatalytique d’hydrogène à la demande
Une nouvelle façon d’« embouteiller » la lumière du soleil
Les sociétés modernes consomment d’énormes quantités d’énergie, mais le soleil n’est pas toujours présent quand nous en avons besoin. Cette recherche explore une méthode ingénieuse pour « embouteiller » l’énergie solaire dans un matériau liquide et la libérer plus tard sous forme d’hydrogène propre, à la demande. Plutôt que de recourir à de grosses batteries métalliques, les auteurs utilisent un plastique hydrosoluble spécial capable d’absorber des électrons sous illumination puis de les restituer ensuite pour produire du gaz hydrogène, un carburant vert potentiel pour l’industrie et le transport.
Transformer un plastique en batterie temporaire
Au cœur de l’étude se trouve un copolymère sur mesure, une longue molécule constituée de deux types de monomères. Une partie rend le matériau aisément soluble dans l’eau ; l’autre contient des unités dites viologènes qui se comportent un peu comme de petites cellules de batterie rechargeables. Lorsque la solution est éclairée par la lumière visible en présence d’un colorant au ruthénium et d’un additif sacrificiel simple, des électrons sont transférés de l’additif vers le polymère. En pratique, la lumière « charge » le polymère en remplissant de nombreux sites viologènes avec des électrons stockés.
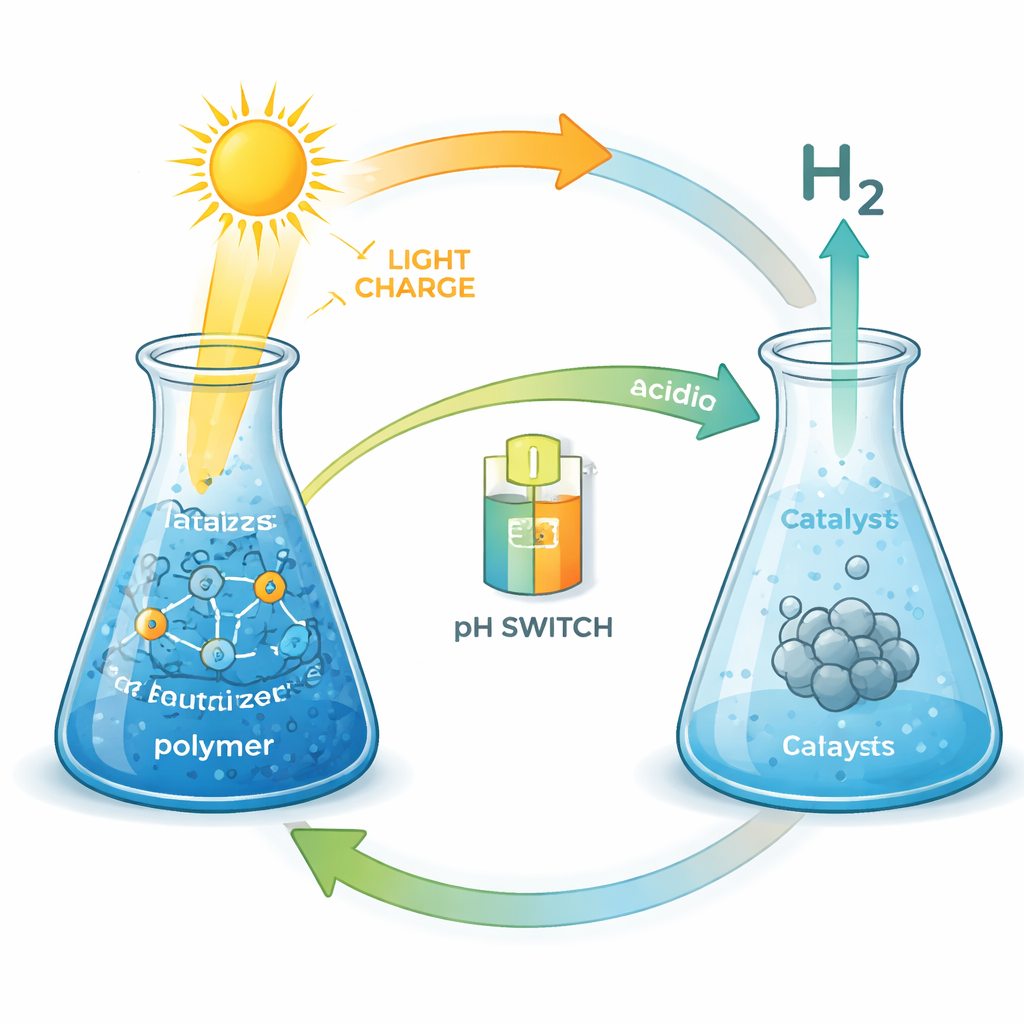
Chargement par la lumière et stockage pendant des jours
L’équipe s’est d’abord interrogée sur l’efficacité avec laquelle ce matériau mou pouvait être chargé par la lumière. En utilisant le complexe de ruthénium comme capteur de lumière et la triéthylamine comme source d’électrons, ils ont montré qu’environ 80 % des sites de stockage disponibles sur le polymère pouvaient être remplis. Des mesures précises de l’absorption de la solution à certaines longueurs d’onde leur ont permis de suivre cet état de charge au fil du temps. Une fois chargé, la solution de couleur violette est restée essentiellement inchangée dans l’obscurité pendant au moins trois jours, correspondant à une charge électrique stockée d’environ 101 coulombs par gramme de polymère—bien au‑delà de certains cadres solides récemment rapportés pour le même objectif. En comparaison, une molécule de viologène simple apparentée perdait une grande partie de sa charge dès le premier jour, soulignant l’effet stabilisant de l’environnement polymérique.
Libérer un carburant propre à la demande
Charger le polymère n’est que la moitié de l’histoire ; l’intérêt réel est de convertir les électrons stockés en hydrogène chaque fois que nécessaire. Pour déclencher cette libération, les chercheurs ont ajouté de l’acide pour abaisser le pH de la solution à 2 et ont introduit différents catalyseurs de production d’hydrogène à base de platine ou de rhodium. Dans ces conditions, les unités viologènes chargées ont remis leurs électrons aux catalyseurs, qui les ont combinés avec des protons issus de la solution acide pour former de l’hydrogène moléculaire. Des nanoparticules colloïdales de platine se sont révélées les plus performantes : elles ont rapidement « déchargé » le polymère et converti jusqu’à environ 72 % des électrons stockés en hydrogène, une efficacité remarquablement élevée pour un système aussi souple et aqueux. Les complexes de rhodium ont aussi été efficaces mais généralement plus lents ou moins efficients, selon la facilité avec laquelle leurs centres métalliques acceptaient des électrons.
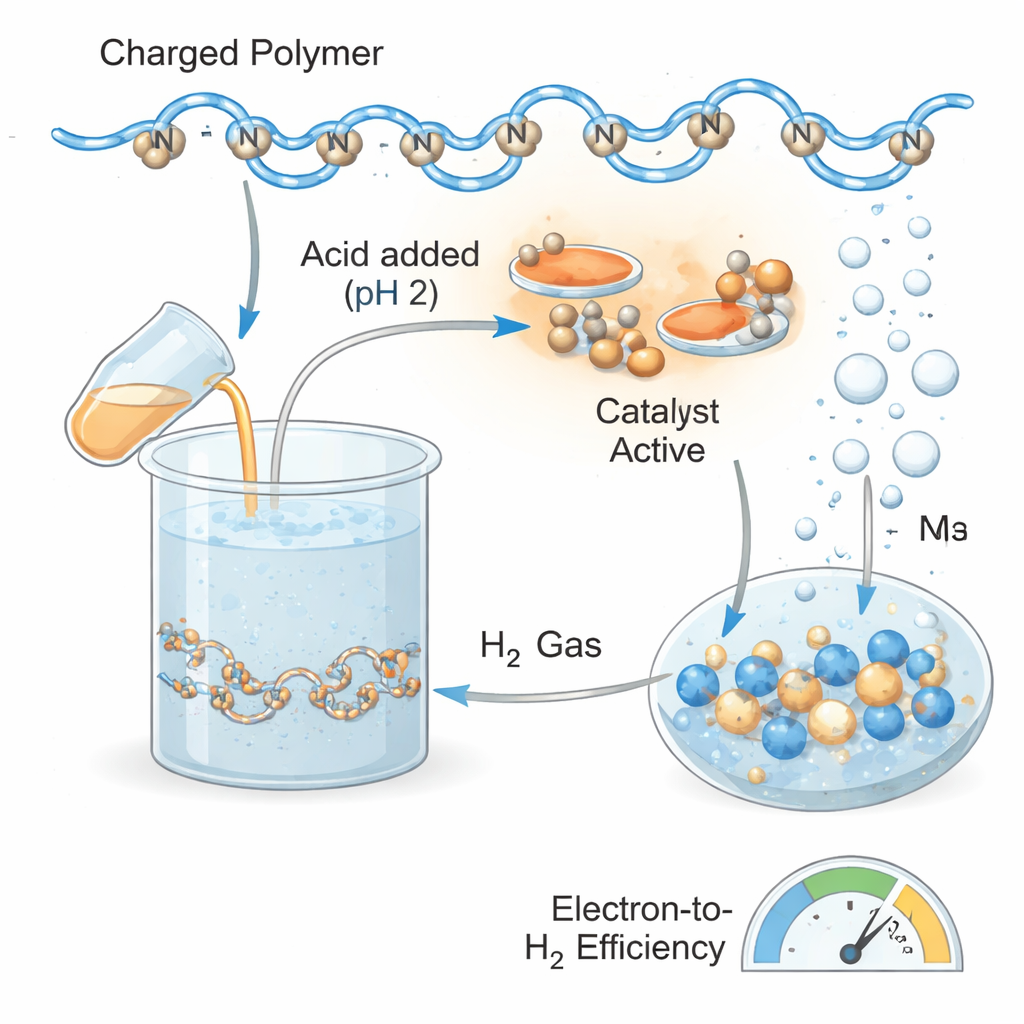
Stocker, attendre, puis carburant—encore et encore
Parce que le polymère et le colorant absorbant restent intacts sur la plage de pH utilisée, la même solution peut être utilisée de manière répétée. Après production d’hydrogène à pH faible, il suffit de neutraliser le mélange pour pouvoir le recharger à la lumière. Les auteurs ont démontré au moins quatre cycles de charge et d’évolution d’hydrogène à la demande sans jamais isoler ni remplacer le polymère. Tandis que les catalyseurs perdaient progressivement de l’activité—en partie en raison de transformations chimiques sous conditions acides et des variations répétées de pH—le polymère lui‑même continuait à stocker et libérer la charge de manière fiable. Si l’on additionne la production de tous les cycles, le système réutilisable fournit plus du double d’hydrogène que ne le ferait même un système parfait à usage unique, ce qui souligne l’avantage de la recyclabilité.
Ce que cela signifie pour les systèmes énergétiques futurs
Pour les non‑spécialistes, le message clé est que ce travail montre une voie réaliste vers des « carburants solaires » liquides capables de combler l’écart entre les heures d’ensoleillement et les besoins énergétiques. Un plastique simple, entièrement hydrosoluble peut servir de réservoir d’énergie temporaire : il se charge par la lumière via un colorant, conserve cette énergie pendant des jours sans perte notable, puis, lorsqu’on le déclenche par un acide et un catalyseur adapté, la libère sous forme d’hydrogène gazeux avec une haute efficacité. L’ensemble du processus peut être répété plusieurs fois en utilisant la même solution, contrôlé par quelque chose d’aussi simple qu’un interrupteur de pH. Bien qu’il reste un système de laboratoire, il ouvre la voie à des solutions flexibles et extensibles pour stocker l’énergie renouvelable sous forme de carburant propre pour des procédés énergivores, comme la future production d’acier vert.
Citation: Hartkorn, M., Kampes, R., Müller, F. et al. A water-soluble copolymer for storage and electron conversion in photocatalytic on-demand hydrogen evolution. Nat Commun 17, 1141 (2026). https://doi.org/10.1038/s41467-026-68342-2
Mots-clés: stockage d’énergie solaire, carburant hydrogène, photocatalyse, polymère rédox, énergie renouvelable