Clear Sky Science · fr
Un LcrV intranasal sans adjuvant renforce l’immunité pulmonaire induite par un priming parental par OMV de Yersinia contre la peste pneumonique chez la souris
Une défense en deux temps contre un tueur célèbre
La peste peut évoquer une maladie médiévale, mais sa forme pulmonaire, la peste pneumonique, tue encore rapidement et se propage par voie aérienne. Les antibiotiques sont efficaces, cependant des souches résistantes et la menace d’une dissémination volontaire maintiennent la peste sur les listes de surveillance modernes. Cette étude chez la souris explore une nouvelle stratégie vaccinale en deux étapes qui vise non seulement à élever le taux d’anticorps dans le sang, mais aussi à entraîner des « sentinelles » immunitaires durables logées dans les poumons, prêtes à arrêter une infection mortelle avant qu’elle ne s’installe.
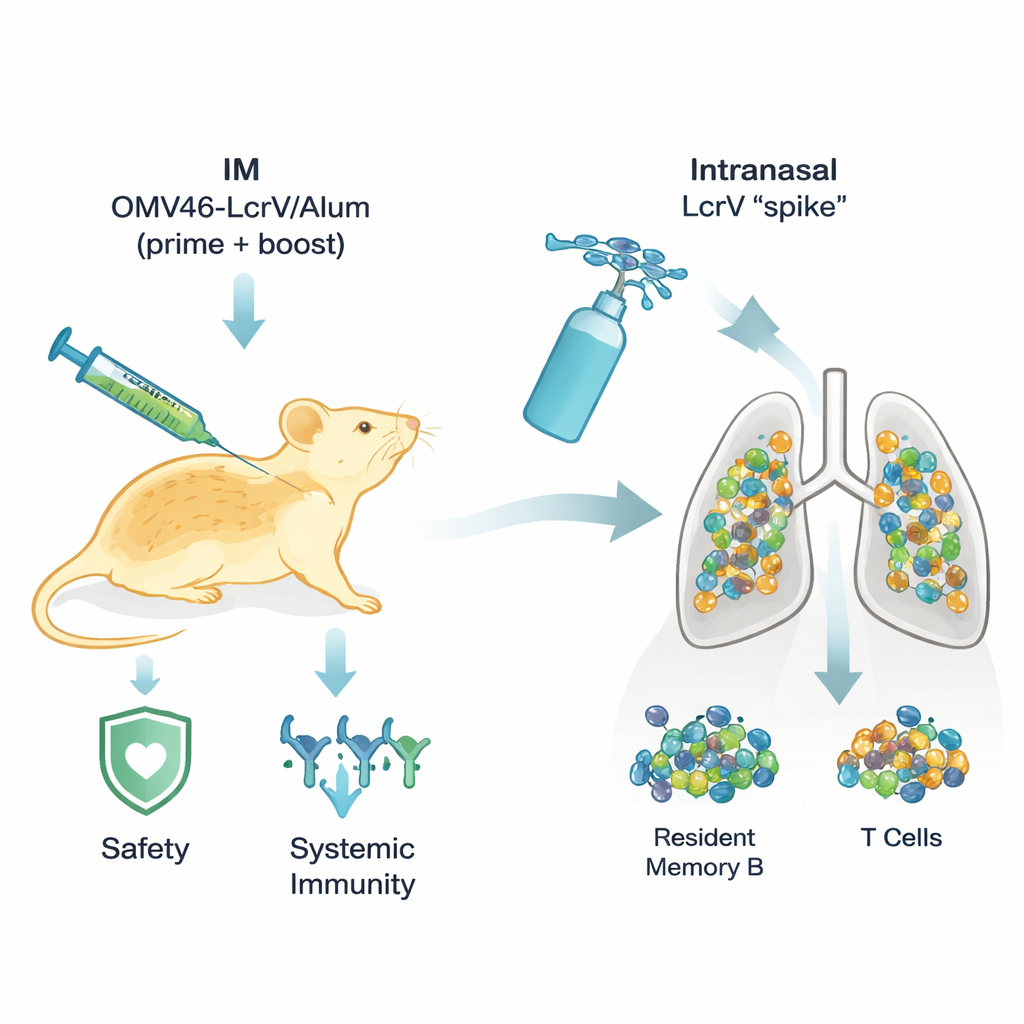
Pourquoi la protection axée sur les poumons importe
La peste se manifeste principalement sous deux formes : bubonique, qui débute généralement par des ganglions enflés après une piqûre de puce, et pneumonique, qui attaque les poumons et peut être presque toujours fatale si le traitement est retardé d’un jour. Les vaccins expérimentaux existants protègent raisonnablement contre la forme bubonique mais ont eu du mal contre la forme pulmonaire. Une raison est que la plupart des injections sont administrées en intramusculaire et instruisent surtout le système immunitaire sanguin, pas les surfaces humides des voies aériennes où débute la peste pneumonique. Pour protéger véritablement les poumons, les chercheurs estiment de plus en plus que les vaccins doivent ensemencer des cellules immunitaires « résidentes » qui prennent place à long terme dans le tissu pulmonaire lui‑même.
Concevoir un vaccin de première ligne plus sûr
L’équipe avait précédemment développé un vaccin prometteur contre la peste basé sur des vésicules de membrane externe (OMV) d’un proche parent de Yersinia, décorées d’une protéine clé de la peste appelée LcrV. Ce vaccin OMV46‑LcrV protégeait fortement les poumons de la souris mais provoquait quelques réactions à court terme. Pour atténuer ces effets indésirables, les chercheurs ont adsorbé les OMV sur des sels d’aluminium (« alum »), un ingrédient vaccinal utilisé de longue date qui améliore généralement la sécurité et favorise la production d’anticorps. Chez la souris, cette version liée à l’alum (OMV46‑LcrV/Alum) n’induisait plus de perte de poids ni de signes inquiétants d’inflammation sanguine, tout en protégeant la plupart des animaux contre des défis de peste à très forte dose. Cependant, sa protection a légèrement diminué aux doses d’infection les plus élevées, suggérant qu’une meilleure sécurité s’était obtenue au prix d’une petite baisse de puissance.
Ajouter un « boost » nasal pour suralimenter les poumons
Pour restaurer et même améliorer la protection sans ajouter d’ingrédients agressifs dans les poumons, les chercheurs ont emprunté un concept testé initialement pour la COVID‑19 : « prime and spike ». Les souris ont d’abord été primées et relancées par les injections intramusculaires OMV46‑LcrV/Alum plus sûres, puis ont reçu une petite dose de protéine LcrV purifiée pulvérisée dans le nez, sans adjuvant ajouté. Ce « spike » intranasal n’a pas perturbé le poids, les numérations sanguines ou la structure pulmonaire. Pourtant, il a complètement changé l’immunité des voies aériennes. Après le rappel nasal, le liquide de lavage pulmonaire contenait beaucoup plus d’anticorps spécifiques de LcrV, y compris des IgA, une forme particulièrement adaptée à enrober et protéger les surfaces muqueuses. Les poumons se sont également enrichis en cellules B mémoire résidentes (qui peuvent rapidement devenir des usines à anticorps), en cellules T mémoire résidentes, et en macrophages spécialisés qui patrouillent dans les espaces aériens. Ces cellules produisaient un mélange de protéines de signalisation utiles — telles que l’interféron‑γ, l’IL‑17A et l’IL‑4 — qui soutenaient ensemble l’élimination bactérienne tout en équilibrant l’inflammation.
Évaluer la protection dans des conditions difficiles
Ces modifications immunitaires se sont traduites par une protection spectaculaire en conditions réelles. Les souris ayant reçu uniquement les injections OMV liées à l’alum ont survécu à de nombreux défis, mais une fraction est morte après les doses bactériennes les plus massives. Les souris ayant également reçu le boost intranasal LcrV ont survécu aux infections pulmonaires les plus extrêmes, y compris avec des souches dépourvues d’un composant majeur de la capsule et chez des animaux âgés présentant une surcharge en fer qui aggrave habituellement les infections à Yersinia. Dans ces souris « prime‑spike », les bactéries étaient presque totalement absentes des poumons, du foie et de la rate en quelques jours. Lorsque les scientifiques ont neutralisé des molécules clés de signalisation des cellules T, ou bloqué la circulation des lymphocytes des ganglions vers les tissus, la protection a fortement chuté, montrant que les cellules résidentes pulmonaires générées par le protocole sont essentielles. Le transfert de ces cellules B et T résidentes vers d’autres souris a directement amélioré leur survie, soulignant que ce sont bien les cellules elles‑mêmes, et non seulement les anticorps circulants, qui fournissent le bouclier supplémentaire.
Mémoire pulmonaire durable et perspectives
L’équipe a aussi testé si un rappel nasal administré plusieurs mois après les injections pouvait encore réveiller l’immunité pulmonaire. Quand la dose intranasale de LcrV a été retardée d’environ six mois, elle a de nouveau fortement stimulé les anticorps et les cellules mémoire résidentes dans les poumons et a rétabli une protection totale contre un défi lourd de peste pneumonique, tandis que les animaux ayant seulement reçu les injections intramusculaires restaient partiellement non protégés. Cela suggère que des personnes vaccinées auparavant avec une préparation similaire pourraient, en principe, recevoir un simple rappel nasal lors d’une épidémie pour rafraîchir rapidement leurs défenses pulmonaires. Bien que ces expériences n’aient été menées que chez la souris et que des essais humains nécessiteront d’abord d’autres modèles animaux, ce travail oriente vers des stratégies vaccinales combinant la praticité des injections standards et la protection localisée et puissante de l’immunité muqueuse.
Ce que cela signifie pour le public
Pour un non‑spécialiste, le message central est que l’endroit où un vaccin envoie vos défenseurs immunitaires peut compter autant que leur nombre. En entraînant d’abord le système immunitaire par une injection sûre, puis en dirigeant une protéine clé de la peste directement dans le nez, cette approche en deux étapes apprend aux poumons eux‑mêmes à reconnaître et repousser les bactéries de la peste. Si des stratégies similaires fonctionnent chez l’humain, elles pourraient offrir un moyen rapide et durable de se protéger contre la peste pneumonique — et inspirer de nouveaux vaccins qui protègent mieux nos voies aériennes contre une variété d’agents respiratoires dangereux.
Citation: Majumder, S., Das, S., Saqib, M. et al. Intranasal unadjuvanted LcrV boosts parental Yersinia OMV primed lung immunity against pneumonic plague in mice. Nat Commun 17, 1624 (2026). https://doi.org/10.1038/s41467-026-68334-2
Mots-clés: peste pneumonique, vaccin muqueux, rappel intranasal, immunité pulmonaire, Yersinia pestis