Clear Sky Science · fr
L’activité de DOT1L limite la vitesse d’élongation transcriptionnelle et favorise la pause de l’ARNP II pour faciliter la mutagenèse par AID
Comment nos cellules immunitaires ajustent des altérations ADN risquées
Notre système immunitaire produit des anticorps puissants en mutant délibérément son propre ADN, une stratégie risquée qui peut parfois favoriser l’apparition de cancers. Cette étude pose une question apparemment simple mais aux grandes implications : qu’est-ce qui contrôle où et avec quelle efficacité ces mutations intentionnelles se produisent ? La réponse se concentre sur une protéine appelée DOT1L, qui ajuste la vitesse de lecture des gènes dans les cellules B et, ce faisant, aide à cibler la machinerie de mutation sur les endroits appropriés.
Activer la mutation pour affiner les anticorps
Lorsque les cellules B rencontrent une infection, elles améliorent leurs anticorps de deux manières. Elles introduisent de petites modifications dans la région de liaison de l’anticorps pour augmenter son affinité pour les agents pathogènes, et elles remplacent la « queue » de l’anticorps pour modifier la réponse immunitaire. Les deux améliorations commencent par une enzyme appelée AID, qui entaille et modifie l’ADN dans les gènes activement lus. Si AID est crucial pour une bonne immunité, il peut aussi toucher d’autres gènes, créant des cassures dangereuses qui favorisent les cancers du sang. Des travaux antérieurs ont montré qu’AID préfère les gènes fortement transcrits et régulés par de puissants commutateurs d’ADN appelés super-enhancers, mais cela n’expliquait pas entièrement pourquoi seul un sous-ensemble restreint de gènes est réellement vulnérable.
Un marqueur chromatinien qui signale les gènes sensibles à AID
Les auteurs se sont intéressés aux protéines qui se trouvent à proximité d’AID dans le noyau. En utilisant une technique de marquage par proximité dans des cellules humaines, ils ont découvert qu’AID se regroupe près de DOT1L, une enzyme qui appose une modification sur un site spécifique des histones autour desquelles l’ADN est enroulé. Cette modification, une marque chimique sur l’histone H3 en position K79, est fréquente sur les gènes actifs. Dans les cellules B de souris, les gènes que AID mutile fréquemment — y compris les gènes d’anticorps et des cibles hors site liées au cancer — portent des niveaux particulièrement élevés de ces marques catalysées par DOT1L. Lorsque les chercheurs ont désactivé DOT1L dans des lignées de cellules B ou bloqué son activité avec un médicament, le « changement de classe » des anticorps a diminué, tout comme les cassures d’ADN induites par AID et les fusions propices au cancer entre gènes d’anticorps et le gène de croissance cMyc. Il est important de noter que la fonction catalytique de DOT1L, et non sa simple présence, était requise : des versions mutantes incapables de placer la marque sur l’histone n’ont pas pu rétablir un changement de classe normal.
Ralentir le lecteur de gènes pour laisser du temps à AID
À première vue, cela paraît paradoxal parce que DOT1L est associé à des gènes actifs, et pourtant son retrait n’a pas simplement éteint ces gènes. En utilisant une méthode qui capture les ARN nouvellement synthétisés, l’équipe a découvert que les cellules B privées de DOT1L produisaient en réalité davantage de transcrits naissants sur de nombreux gènes marqués par DOT1L — bien qu’il y ait légèrement moins de l’enzyme principale de lecture des gènes, l’ARN polymérase II, présente sur ces gènes. En combinant cette mesure des ARN naissants avec des cartographies de l’occupation de la polymérase, ils ont inféré que, dans des conditions normales, les marques d’histone déposées par DOT1L agissent comme de légers ralentisseurs. Elles freinent la polymérase au fur et à mesure de sa progression le long du gène et prolongent de courtes pauses près du début et dans le corps des gènes marqués par DOT1L. Sans DOT1L, la polymérase file plus vite et marque moins de pauses. Parce qu’AID a besoin de fenêtres brèves pendant lesquelles l’ADN est exposé et la polymérase traîne, cette accélération réduit paradoxalement la capacité d’AID à se fixer et à accomplir son rôle, même si la transcription globale augmente.
Dissocier l’activité génique du risque de mutation
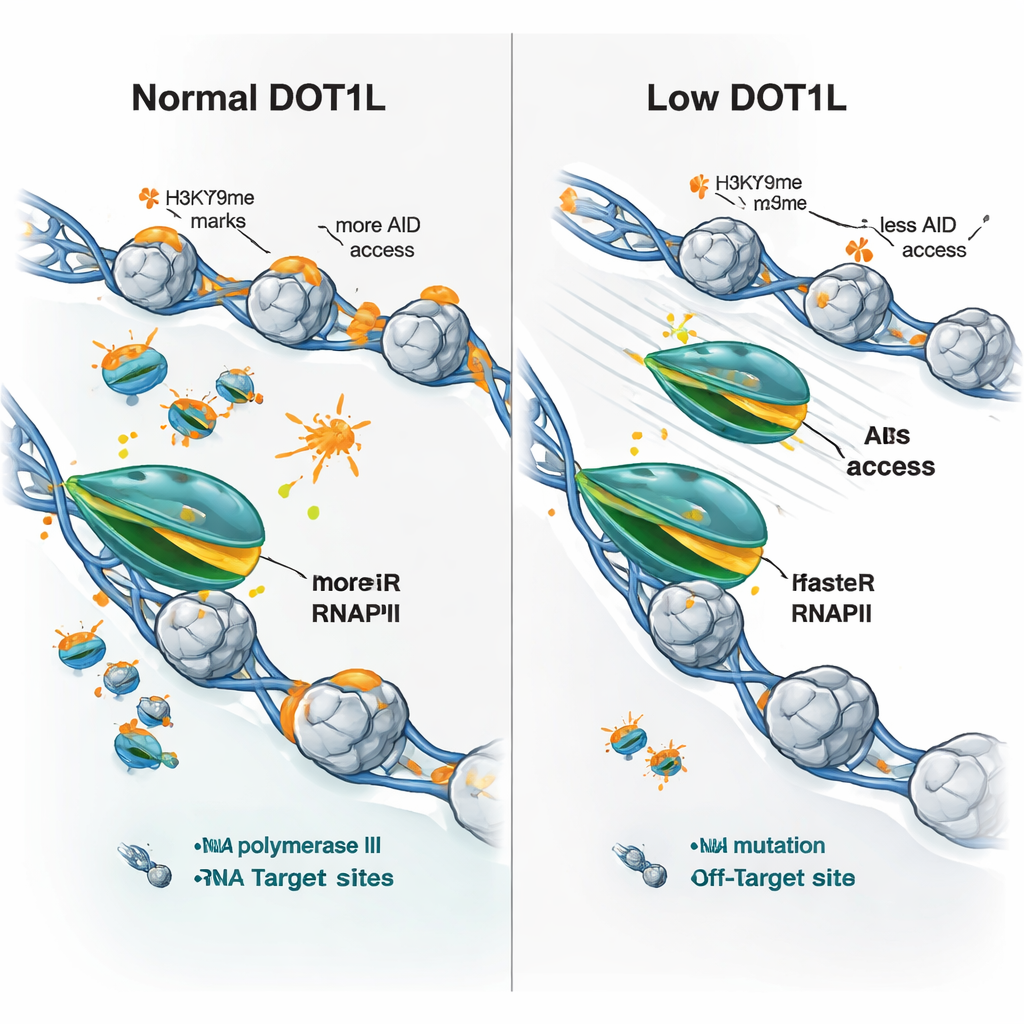
Les chercheurs se sont ensuite demandé si ces changements de vitesse pouvaient expliquer le profil mixte d’expression génique observé lors de la perte de DOT1L — certains gènes augmentent, d’autres diminuent. Ils ont constaté que presque tous les gènes marqués par DOT1L partageaient une caractéristique dans les cellules knock-out : une élongation plus rapide par l’ARN polymérase II. Mais l’issue dépendait de l’état initial. Les gènes lents, faiblement exprimés, avaient tendance à produire plus d’ARN lorsque la polymérase s’accélérait, tandis que les gènes longs et fortement actifs, dont la polymérase était déjà rapide, en produisaient parfois moins, probablement parce qu’un passage trop rapide perturbe un traitement efficient ou l’achèvement de la transcription. De façon cruciale, tant aux gènes d’anticorps qu’aux cibles hors site classiques d’AID, la perte de DOT1L entraînait une progression plus rapide de la polymérase, moins de signes de « blocage » de la polymérase et une occupation d’AID nettement réduite, même lorsque l’expression des gènes n’était pas diminuée.
Pourquoi cela compte pour l’immunité et le cancer
Pris ensemble, ces travaux présentent DOT1L comme un contrôleur subtil du trafic pour la machinerie de lecture des gènes dans les cellules B. En installant des marques d’histone spécifiques, DOT1L ralentit légèrement l’ARN polymérase II et prolonge ses pauses, créant un environnement transcriptionnel où AID peut s’engager de manière productive sur les gènes d’anticorps — et, malheureusement, sur un ensemble limité d’autres gènes vulnérables — pour introduire des mutations. Lorsque DOT1L fait défaut ou est inhibé, la polymérase traverse plus rapidement, laissant AID avec moins d’occasions d’agir, ce qui atténue la diversification des anticorps et réduit simultanément le risque de certaines réarrangements délétères. Ce mécanisme explique pourquoi la perte de DOT1L peut à la fois augmenter et diminuer l’expression génique, et il relie le contrôle fin de la vitesse de transcription à l’endroit où notre système immunitaire s’autorise à réécrire son propre ADN.
Citation: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Mots-clés: diversification des anticorps, enzyme AID, DOT1L, transcription génique, cellules B