Clear Sky Science · fr
Base moléculaire de l’antagonisme du récepteur humain d’arginine–vasopressine 1A dimérique
Pourquoi un récepteur hormonal cérébral compte
Des hormones comme la vasopressine et l’ocytocine sont surtout connues pour réguler l’équilibre hydrique, la pression artérielle, l’accouchement et les liens affectifs. Mais le fonctionnement atomique de leurs récepteurs est resté en grande partie caché. Cet article dévoile des structures 3D détaillées d’un récepteur clé, le récepteur humain de la vasopressine V1a, lié au comportement social, au stress et à plusieurs troubles cérébraux. Comprendre sa forme et la façon dont les médicaments le bloquent pourrait aider les chercheurs à concevoir de meilleurs traitements pour des affections telles que l’autisme, le trouble de stress post‑traumatique et la maladie de Huntington.
Un récepteur jumeau qui module le cœur, le rein et les signaux cérébraux
Le récepteur V1a se trouve à la surface de nombreuses cellules de l’organisme, en particulier dans les vaisseaux sanguins, les reins et certaines régions du cerveau. Lorsque l’hormone vasopressine s’y fixe, le récepteur active des voies de signalisation internes qui contrôlent la pression artérielle, l’équilibre des fluides et des circuits cérébraux impliqués dans l’interaction sociale, l’émotion et le stress. Des études génétiques et cliniques ont associé une signalisation V1a anormale aux troubles du spectre autistique, au TSPT et à la maladie de Huntington, faisant de ce récepteur une cible médicamenteuse intéressante. Plusieurs antagonistes du V1a sont déjà utilisés ou en essais cliniques, mais jusqu’à présent personne n’avait observé le récepteur humain V1a à haute résolution, laissant d’importantes questions sur son assemblage et sur la façon précise dont ces médicaments l’inactivent. 
Capturer la structure du récepteur dans plusieurs états liés aux médicaments
Les auteurs ont utilisé la cryo‑microscopie électronique, une technique qui vitrifie les protéines et les image au faisceau d’électrons, pour visualiser le récepteur humain V1a. Pour stabiliser la protéine, ils ont conçu une forme légèrement modifiée qui conserve une bonne affinité pour les médicaments et l’ont associée à un petit fragment d’anticorps (un nanocorps) pour faciliter l’imagerie. Ils ont résolu les structures du récepteur seul et lié à trois antagonistes d’intérêt médical : l’atosiban (un peptide utilisé pour prévenir l’accouchement prématuré) et deux petites molécules capables de traverser la barrière hémato‑encéphalique, balovaptan et SRX246, testées chez des personnes autistes ou atteintes de la maladie de Huntington. Toutes les structures ont atteint une résolution proche de l’atomique, révélant la position des sept hélices transmembranaires du récepteur, des boucles flexibles et des médicaments liés.
Un récepteur qui préfère fonctionner par paires
Contrairement à des récepteurs apparentés qui n’avaient été observés que comme unités simples, V1a apparaît en paire — un dimère — dans les quatre structures cryo‑EM. Les deux récepteurs sont côte à côte dans la membrane et établissent des contacts serrés principalement via l’une de leurs hélices, aidés par des interactions polaires et hydrophobes. Pour vérifier si cette association se produit aussi dans des cellules vivantes, l’équipe a fusionné V1a à une protéine fluorescente lumineuse et utilisé une méthode d’extinction photométrique au niveau d’une seule molécule : si un point à la surface cellulaire contenait deux copies du récepteur, sa lumière s’éteindrait en deux étapes. Environ les trois quarts des points observés s’éteignaient en exactement deux étapes, ce qui soutient fortement l’idée que V1a forme naturellement des dimères à la surface cellulaire. Lorsque les chercheurs ont muté des résidus clés de contact pour perturber l’interface, le récepteur a basculé vers des unités simples et a montré une réponse réduite à l’hormone et au médicament, suggérant que le dimère n’est pas qu’une simple décoration structurelle mais qu’il est fonctionnellement important. 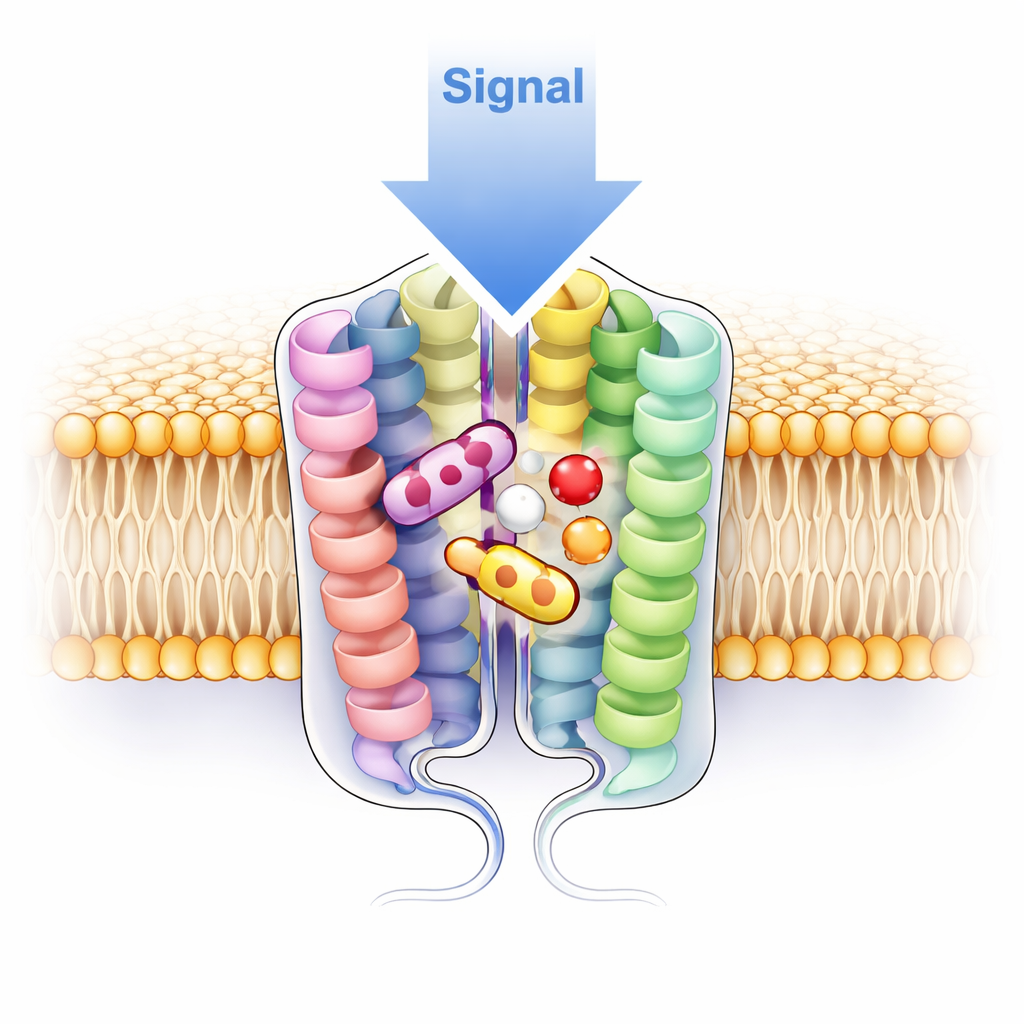
Une porte flexible à l’entrée de l’hormone
L’équipe a mis au jour une région de « porte » inattendue appelée boucle extracellulaire 2 (ECL2), qui se situe au sommet de la cavité de liaison de l’hormone. À l’état sans médicament (apo), cette boucle repose à plat au‑dessus de la cavité comme un couvercle et ne forme pas la liaison disulfure habituelle (liaison soufre–soufre) observée dans de nombreux récepteurs apparentés. À la place, des segments de la boucle se replient dans la cavité et sont maintenus par un réseau d’interactions avec les hélices environnantes, couvrant partiellement la large cavité d’emblée adhésive. Lorsque l’un des trois antagonistes se lie, ECL2 bascule vers le haut et l’extérieur, forme la disulfure classique et crée une cavité large, remplie de solvant, que les molécules pharmacologiques occupent. Ce mouvement spectaculaire suggère que V1a pourrait utiliser ECL2 comme une barrière dynamique pour limiter les activations aléatoires par des molécules errantes, et que des médicaments pourraient être conçus soit pour piéger la boucle dans son état plat « fondamental », soit pour exploiter sa conformation relevée et ouverte.
Comment trois médicaments désactivent le même récepteur de façons différentes
L’atosiban, qui mime étroitement l’ocytocine naturelle, s’étend du sommet de la cavité jusqu’à sa base, s’ancrant grâce à une combinaison de liaisons hydrogène et de contacts hydrophobes. En modifiant quelques positions clés par rapport à l’ocytocine, il ne parvient pas à déclencher la chaîne de déplacements internes normalement requise pour l’activation du récepteur : des résidus « microrupteurs » cruciaux qui bougent durant la signalisation restent verrouillés en positions inactives, la cavité interne qui reçoit la protéine G ne s’ouvre jamais, et un site de liaison au magnésium important pour l’activation est perturbé. En revanche, balovaptan et SRX246 sont de petites molécules non peptidiques et compactes qui s’enfoncent profondément dans la cavité mais adoptent des stratégies distinctes. Balovaptan s’appuie sur un noyau rigide et hydrophobe qui se compacte dans une fente profonde, plus une queue polaire flexible qui s’étend vers l’entrée de la cavité. SRX246 utilise une architecture modulaire, fragmentaire, ancrée par un noyau β‑lactame, avec différentes « zones » bouchant des sous‑poches et s’étendant vers les boucles extracellulaires. Dans les deux cas, les médicaments stabilisent une conformation inactive incompatible avec la liaison de la protéine G. Des différences subtiles de forme et de chimie de la cavité — en particulier à deux positions situées sur les hélices 5 et 7 — aident à expliquer pourquoi balovaptan et SRX246 préfèrent V1a à des récepteurs étroitement apparentés.
Implications pour les thérapies futures
En fournissant des instantanés haute résolution de V1a sous forme de dimère, en révélant une conformation de boucle « plate » jusque‑là inconnue à l’état sans médicament, et en détaillant comment trois antagonistes très différents neutralisent le récepteur, ce travail offre aux concepteurs de médicaments une carte structurale précise pour cibler V1a. Il suggère des voies pour élaborer des médicaments de nouvelle génération qui exploitent soit des caractéristiques spécifiques au dimère, soit qui verrouillent le récepteur dans un état fondamental particulièrement inactif, dans le but ultime de traiter de manière plus ciblée les troubles cérébraux et liés au stress, avec moins d’effets secondaires.
Citation: Zhong, P., Chu, B., Yu, Z. et al. Molecular basis of antagonism of the dimeric human arginine vasopressin receptor 1A. Nat Commun 17, 1622 (2026). https://doi.org/10.1038/s41467-026-68331-5
Mots-clés: récepteur de la vasopressine V1a, récepteur couplé aux protéines G, dimérisation des récepteurs, structure cryo‑EM, conception de médicaments neuropsychiatriques