Clear Sky Science · fr
Signatures génomiques et physiologiques de l’adaptation chez des champignons pathogènes
Pourquoi les champignons sur notre peau et dans notre sol comptent
On imagine souvent les champignons comme des champignons dans la forêt ou de la moisissure sur du pain rassis, mais de nombreux champignons microscopiques vivent discrètement dans le sol, sur les plantes et même sur notre peau. Certaines de ces espèces inoffensives peuvent soudainement se transformer en menaces sérieuses, provoquant des infections potentiellement mortelles chez des personnes immunodéprimées. Cette étude pose une question apparemment simple : qu’est‑ce qui change à l’intérieur de ces champignons lorsqu’ils passent de la vie sur des feuilles mortes à l’invasion du corps humain ?
Retracer les liens de parenté entre champignons amis et nuisibles
Les auteurs se sont concentrés sur un groupe de levures appelé Trichosporonales, qui comprend à la fois des espèces environnementales se nourrissant de matière en décomposition et des espèces opportunistes capables d’infecter des humains. En comparant les génomes de 45 souches fongiques, ils ont construit un arbre généalogique montrant les relations entre ces espèces. L’arbre révèle que les champignons infectant l’homme sont dispersés sur différentes branches plutôt que regroupés dans une seule lignée. Ce schéma suggère que la capacité d’infecter les humains a évolué plusieurs fois de manière indépendante, plutôt que d’apparaître une fois et d’être héritée.
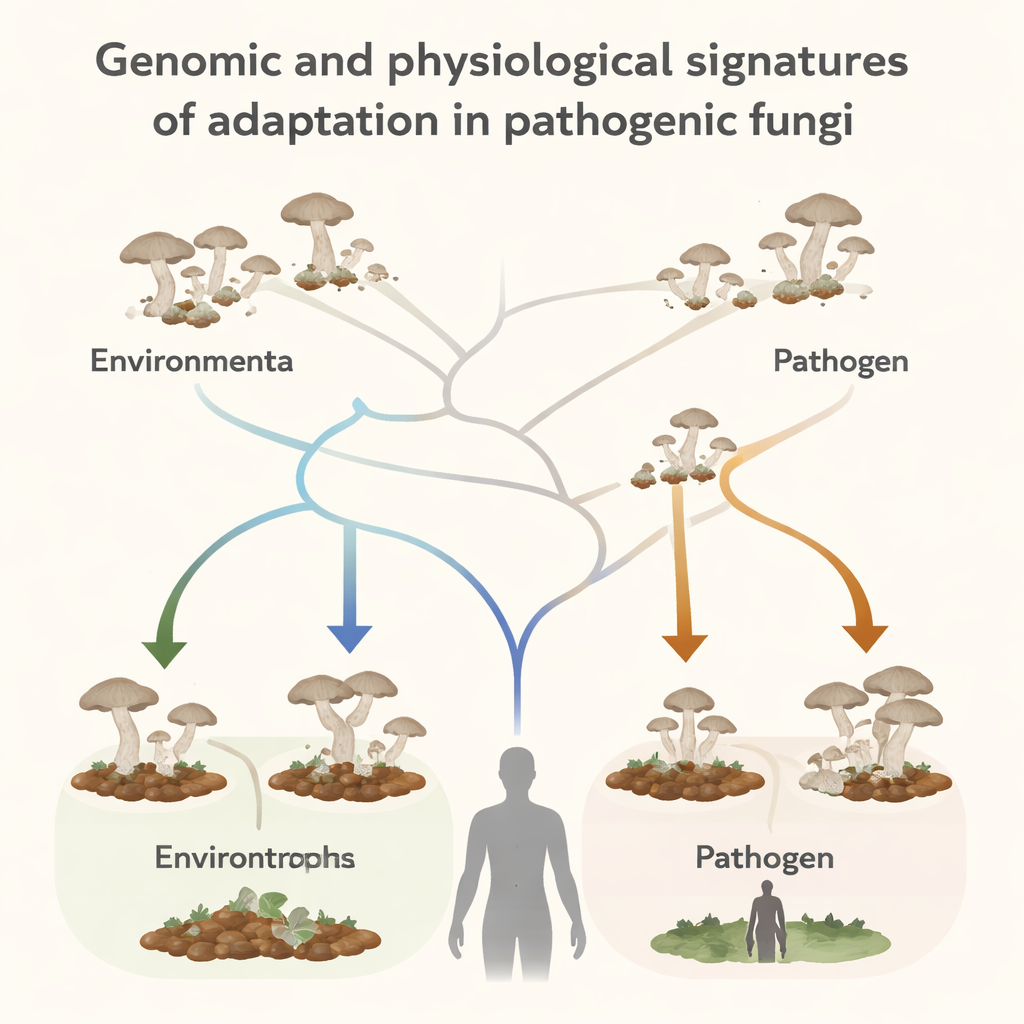
Même boîte à outils, façon différente de l’utiliser
Une hypothèse naturelle est que les champignons dangereux pourraient porter des ensembles particuliers de gènes — comme des outils supplémentaires — que les champignons inoffensifs n’auraient pas. Pour tester cela, l’équipe a compté les gènes impliqués dans la dégradation des glucides (importants pour la vie sur les débris végétaux) et ceux impliqués dans le traitement des lipides et huiles (importants à l’intérieur des animaux). De manière surprenante, ils ont trouvé que les pathogènes et les saprotrophes ont des nombres très similaires de ces gènes, ainsi que des tailles de génome, des éléments répétés et des enzymes sécrétées comparables. Autrement dit, le simple fait de posséder certains gènes ne sépare pas clairement les champignons qui infectent les humains de ceux qui ne le font pas. La différence cruciale semble résider non pas dans les gènes présents, mais dans l’efficacité avec laquelle ils sont utilisés.
Ajuster la vitesse de l’usine à protéines
Pour approfondir, les auteurs se sont intéressés au processus de traduction — l’étape où les cellules lisent l’information génétique et fabriquent des protéines. La traduction dépend des ARN de transfert (ARNt), de petites molécules qui associent les « codons » génétiques aux acides aminés. Si les codons d’un gène correspondent aux ARNt les plus abondants, sa protéine peut être produite plus rapidement et plus efficacement. L’équipe a mesuré à quel point les codons des gènes liés aux glucides et aux lipides étaient « optimisés » pour les ARNt disponibles dans chaque espèce. Ils ont constaté que les champignons saprotrophes étaient plutôt mieux réglés pour le métabolisme des glucides, tandis que les pathogènes opportunistes montraient une optimisation relativement plus élevée pour le métabolisme des lipides. Ce schéma était suffisamment marqué pour qu’un modèle simple en arbre de décision puisse généralement prédire si une espèce était un pathogène ou un saprotrophe uniquement à partir de l’optimisation relative des voies lipidiques versus glucidiques.
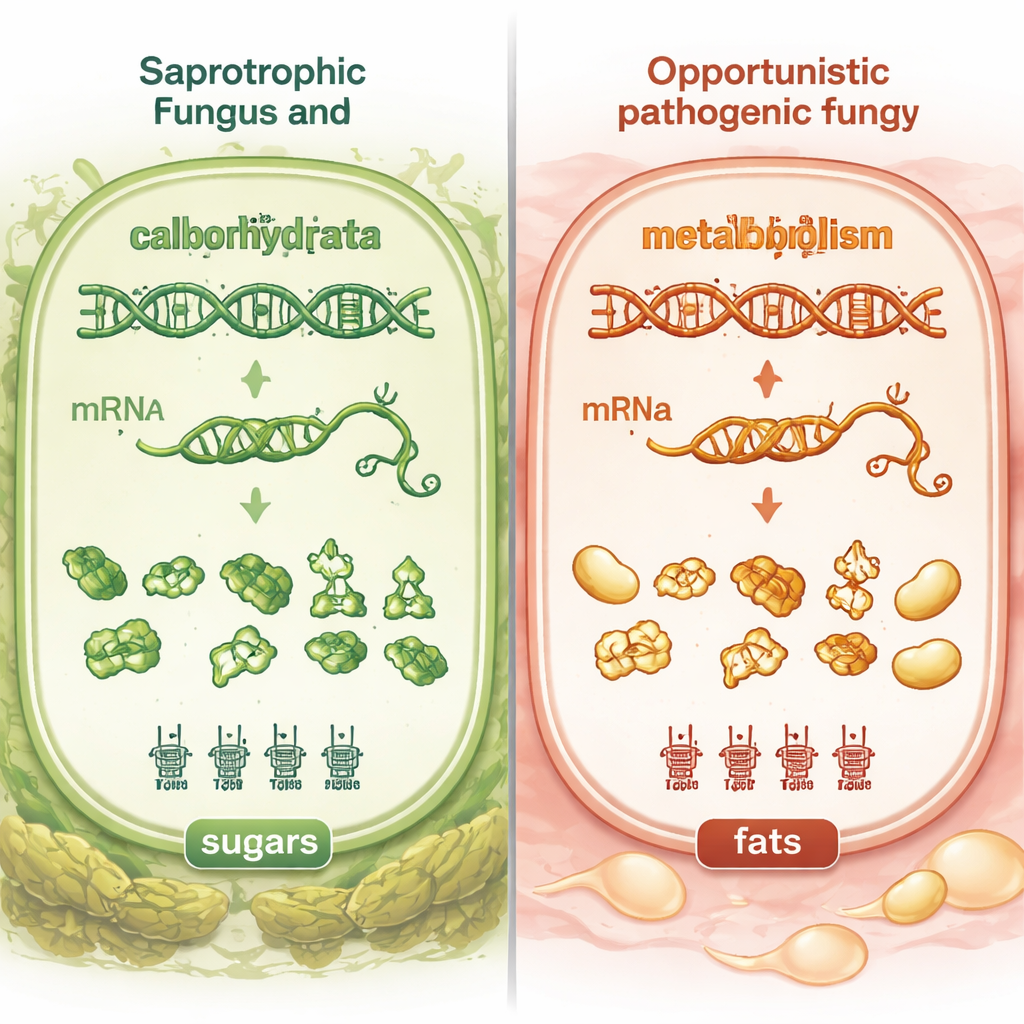
De l’accord génétique à la croissance en conditions réelles
Les signatures génomiques ne sont utiles que si elles ont un impact pratique, aussi les chercheurs ont‑ils testé la croissance des différents champignons en laboratoire. Ils ont mesuré la croissance sur milieux riches en sucres et sur milieux riches en lipides, et ont aussi suivi la rapidité avec laquelle les champignons s’adaptaient à de nouvelles conditions. Si les taux de croissance globaux ne suivaient pas fortement l’optimisation des codons, la durée de la phase de latence — le temps d’attente avant le début d’une croissance rapide — oui. Les champignons dont les gènes métaboliques étaient encodés de façon plus optimale pour une source alimentaire donnée commençaient à croître plus vite sur ce substrat. L’équipe a également testé la croissance à des températures plus élevées, notamment 33 °C et 37 °C, proches de la chaleur corporelle des mammifères. Beaucoup de pathogènes connus croissaient bien à ces températures, mais certaines espèces dites « environnementales » le faisaient aussi, et certains pathogènes ne le faisaient pas, montrant que la tolérance à la chaleur est importante mais pas le seul facteur de la pathogénicité.
Candidats cachés pour de futures menaces fongiques
Un résultat marquant est que certains champignons actuellement classés comme saprotrophes inoffensifs présentaient des patrons translationnels et une tolérance à la température similaires à ceux de pathogènes opportunistes connus. En particulier, certaines espèces d’Apiotrichum et de Vanrija semblent génétiquement prêtes à gérer des environnements riches en lipides et à croître près de la température corporelle, même si elles ne sont pas encore fréquentes dans les rapports cliniques. Cela suggère que la frontière entre champignons environnementaux et pathogènes potentiels est plus mince qu’il n’y paraît, et que certains habitants discrets du sol ou de la litière foliaire pourraient devenir de futures menaces pour la santé dans les bonnes conditions.
Ce que cela signifie pour la santé humaine
Pour les non‑spécialistes, le message clé est que les traits dangereux chez les champignons peuvent ne pas dépendre de « gènes de virulence » exotiques, mais de l’efficacité de traduction des gènes métaboliques courants lorsque les champignons rencontrent de nouveaux environnements, comme le corps humain. En lisant des signatures subtiles dans l’usage des codons et la composition en ARNt, les scientifiques peuvent commencer à repérer les champignons environnementaux prêts à s’adapter rapidement aux hôtes. De tels marqueurs génomiques et physiologiques pourraient enfin aider les médecins et les responsables de la santé publique à anticiper quelles espèces sont les plus susceptibles d’émerger comme prochains pathogènes opportunistes, améliorant la surveillance et la préparation avant que des foyers n’apparaissent.
Citation: Guerreiro, M.A., Yurkov, A., Nowrousian, M. et al. Genomic and physiological signatures of adaptation in pathogenic fungi. Nat Commun 17, 748 (2026). https://doi.org/10.1038/s41467-026-68330-6
Mots-clés: pathogènes fongiques, évolution du génome, optimisation des codons, infections opportunistes, adaptation à l’hôte