Clear Sky Science · fr
La glycérol‑3‑phosphate acyltransférase aggrave la toxicité induite par l’α‑synucléine en augmentant la peroxydation lipidique
Pourquoi les lipides du cerveau comptent pour la maladie de Parkinson
La maladie de Parkinson est généralement décrite comme un problème lié à une protéine appelée alpha‑synucléine qui s’agrège et endommage les cellules cérébrales contrôlant le mouvement. Cette étude montre que les lipides du cerveau — et plus particulièrement la façon dont ils sont synthétisés et abîmés — jouent un rôle étonnamment puissant dans la toxicité de l’alpha‑synucléine. En identifiant une enzyme de synthèse lipidique qui amplifie les lésions neuronales, ce travail met en lumière une voie pharmacologiquement exploitable pouvant compléter les approches existantes visant la cause de la maladie de Parkinson.
Une protéine qui se comporte mal dans la maladie de Parkinson
Les personnes atteintes de Parkinson perdent progressivement les neurones producteurs de dopamine dans une région profonde du cerveau qui coordonne le mouvement. Dans ces cellules en voie de mort, les chercheurs trouvent souvent des dépôts denses appelés corps de Lewy, riches en alpha‑synucléine. Dans de rares familles, des mutations ou des copies supplémentaires du gène codant l’alpha‑synucléine provoquent directement la maladie, mais les variantes génétiques communes de ce gène n’augmentent le risque que modestement. Cela suggère que d’autres gènes et voies modulent la nocivité de l’alpha‑synucléine. De plus en plus, les données pointent vers les lipides — graisses et molécules apparentées qui forment les membranes cellulaires et les réserves énergétiques — comme partenaires clés de l’agrégation de l’alpha‑synucléine et de la mort neuronale.
Identification d’une enzyme lipidique puissante dans des modèles de drosophile
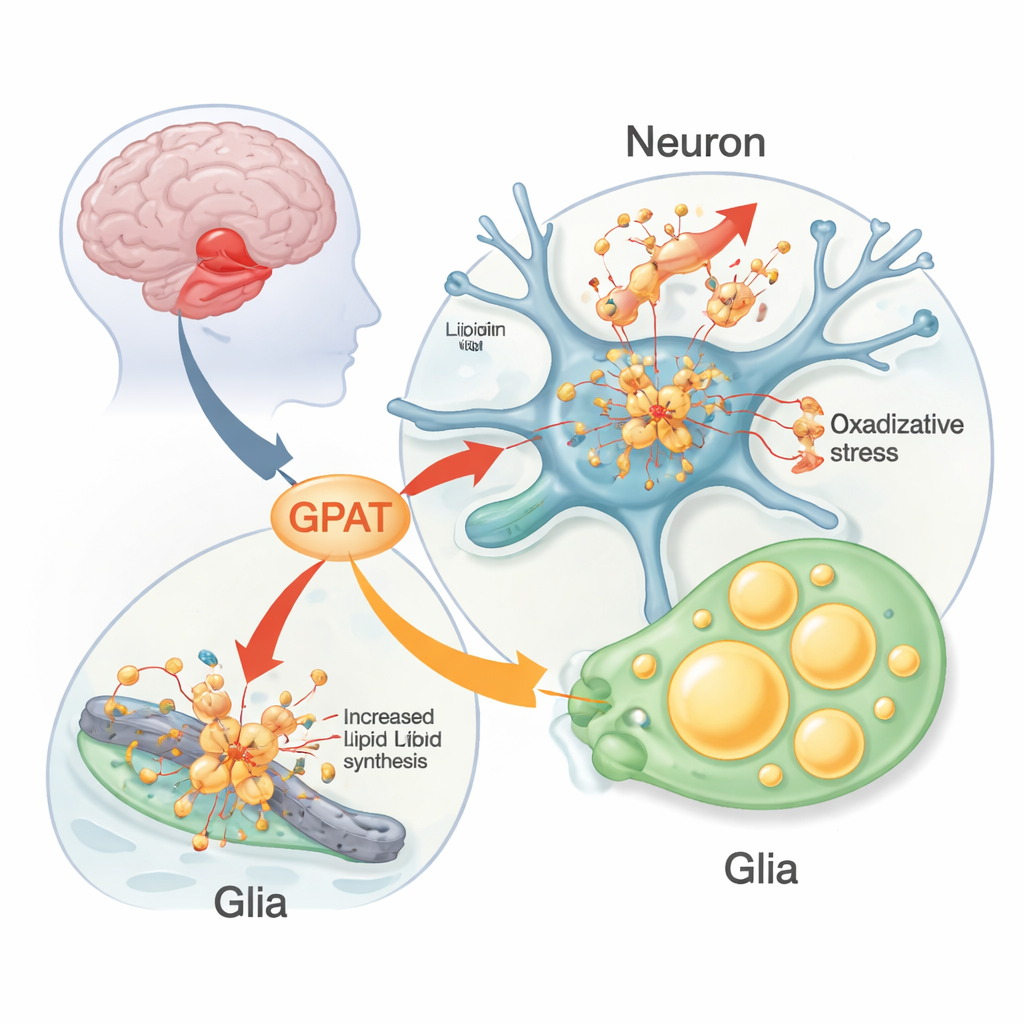
Les chercheurs ont utilisé des mouches drosophiles modifiées pour exprimer l’alpha‑synucléine humaine dans leur système nerveux comme modèle vivant. Ces mouches développent des troubles rappelant la maladie de Parkinson : perte de neurones producteurs de dopamine, difficultés à grimper et perturbation des rythmes d’activité quotidiens. L’équipe a systématiquement manipulé les homologues de gènes de risque Parkinsoniens chez la mouche pour voir lesquels modifiaient l’impact de l’alpha‑synucléine. Un gène s’est distingué : mino, qui code une forme mitochondriale de l’enzyme glycérol‑3‑phosphate acyltransférase (GPAT). GPAT se situe au point d’entrée de la synthèse des phospholipides et des triglycérides — les lipides qui composent membranes et gouttelettes de graisse. Lorsque l’équipe a réduit l’activité de mino dans les neurones, les mouches exprimant l’alpha‑synucléine conservaient davantage de neurones dopaminergiques et restaient plus mobiles plus longtemps ; l’augmentation de l’expression de mino avait l’effet inverse et délétère.
Lipides abîmés, mitochondries stressées et gouttelettes lipidiques gliales
En approfondissant, les scientifiques ont découvert que la GPAT modifiait la quantité de dommages oxydatifs accumulés dans les lipides cérébraux. Chez les mouches alpha‑synucléine maintenues à température plus élevée (ce qui aggrave les caractéristiques de la maladie), la peroxydation lipidique — le « rouillage » chimique des graisses — augmentait dans les membranes cérébrales. La diminution de mino réduisait ces dommages, tandis que sa surexpression les amplifiait ; en l’absence d’alpha‑synucléine, modifier mino avait peu d’effet. Les marqueurs de mort cellulaire dans la région visuelle du cerveau reflétaient ce schéma. L’équipe a aussi observé une accumulation frappante de gouttelettes lipidiques — petites sphères de stockage de graisse — non pas dans les neurones eux‑mêmes mais dans les cellules gliales voisines. Ces gouttelettes augmentaient avec l’âge chez les mouches alpha‑synucléine et étaient modulées par des enzymes impliquées dans la synthèse ou la dégradation des triglycérides, soulignant un partenariat métabolique actif entre neurones et glie en situation de stress.
Réorientation métabolique et agrégation de l’alpha‑synucléine
Les mesures de métabolites dans les cerveaux de mouches ont révélé que l’expression d’alpha‑synucléine était associée à un goulet d’étranglement dans le cycle énergétique cellulaire : le citrate et l’isocitrate, deux intermédiaires du cycle tricarboxylique (TCA), s’accumulaient fortement, tandis que les étapes en aval étaient moins affectées. Les taux de lactate augmentaient également, compatible avec une glycolyse accrue. Simultanément, un profilage lipidique détaillé montrait des changements dans l’équilibre des phospholipides membranaires et leur composition en acides gras, favorisant des espèces plus sujettes aux dommages oxydatifs. Lorsque l’équipe a réduit plusieurs enzymes GPAT — mino dans les mitochondries et des enzymes apparentées sur le réticulum endoplasmique — l’alpha‑synucléine continuait de s’accumuler, mais sa propension à former des oligomères de haut ordre (amas protéiques) diminuait, et les mitochondries présentaient moins de signes de stress oxydatif et de « vieillissement ».
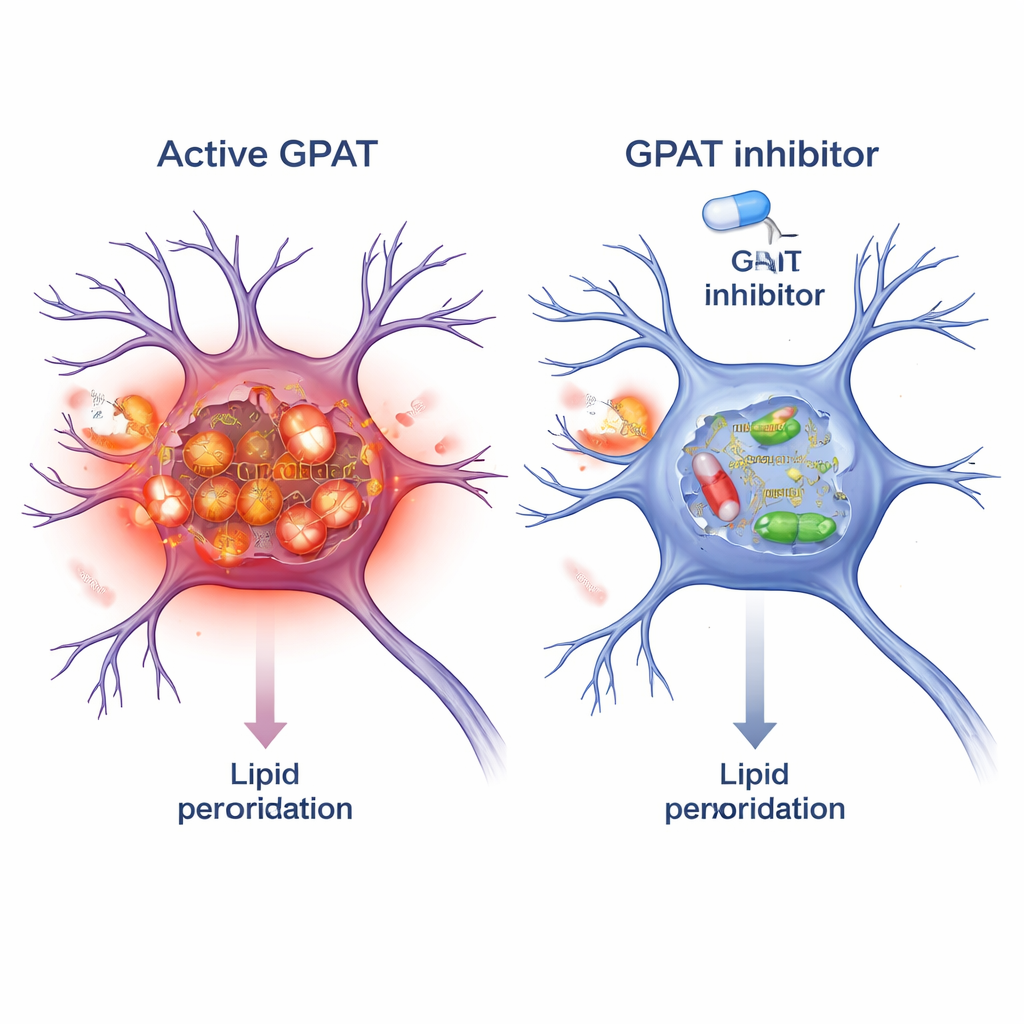
Bloquer la GPAT comme stratégie protectrice
Parce que la GPAT est une enzyme, elle peut être ciblée par de petites molécules. Les chercheurs ont testé le FSG67, un inhibiteur de GPAT déjà développé pour l’obésité et le diabète. Chez les mouches alpha‑synucléine, l’ajout de FSG67 dans la nourriture reproduisait les bénéfices du knock‑down génétique de la GPAT : amélioration des déplacements, meilleure survie des neurones dopaminergiques, moins d’oligomères toxiques d’alpha‑synucléine et réduction du stress oxydatif mitochondrial. Pour savoir si ce concept s’appliquait aux mammifères, ils ont traité des neurones corticaux de souris en culture avec des fibrilles d’alpha‑synucléine préformées, qui catalysent la formation d’agrégats toxiques. Le cotraitement par le FSG67 réduisait l’accumulation d’alpha‑synucléine phosphorylée et abaissait plusieurs marqueurs indépendants de peroxydation lipidique au sein de ces neurones.
Qu’est‑ce que cela signifie pour les personnes atteintes de Parkinson
En termes simples, ce travail montre que la manière dont le cerveau gère les lipides peut augmenter ou diminuer la toxicité de l’alpha‑synucléine. Quand la GPAT est très active, des lipides vulnérables sont intégrés aux membranes et aux gouttelettes de stockage, les rendant plus susceptibles à l’oxydation ; ce milieu lipidique endommagé semble favoriser des formes nuisibles d’alpha‑synucléine et mettre à rude épreuve les mitochondries, centrales énergétiques de la cellule. Réduire l’activité de la GPAT — génétiquement ou avec un médicament — renverse la balance vers moins de « rouille » lipidique, moins d’assemblages protéiques toxiques et des neurones en meilleure santé. Bien que ces résultats soient préliminaires et issus de mouches et de cultures cellulaires de souris, ils mettent en avant le métabolisme lipidique, et la GPAT en particulier, comme un angle nouveau et prometteur pour des thérapies de la maladie de Parkinson pouvant compléter les stratégies ciblant directement l’alpha‑synucléine.
Citation: Ren, M., Lim, G.G.Y., Tang, W. et al. Glycerol 3-phosphate acyltransferase exacerbates α-synuclein-induced toxicity by increasing lipid peroxidation. Nat Commun 17, 1618 (2026). https://doi.org/10.1038/s41467-026-68325-3
Mots-clés: maladie de Parkinson, alpha‑synucléine, peroxydation lipidique, inhibiteur de GPAT, neurodégénérescence