Clear Sky Science · fr
Dynamiques évolutives de la détermination sexuelle chez Branchiostoma belcheri entraînées par la transposition répétée d’un seul gène nouveau
Comment une minuscule créature marine remanie les règles du mâle et de la femelle
Dans la plupart des manuels scolaires, le sexe est présenté comme une simple affaire de chromosomes X et Y, mais dans une grande partie du vivant les règles sont bien plus flexibles. Cette étude examine un petit animal ressemblant à un poisson, l’amphioxus, proche parent des vertébrés, et révèle un système étonnamment dynamique pour décider qui devient mâle ou femelle. En suivant les déplacements d’un seul gène à travers le génome, les auteurs montrent comment des interrupteurs de détermination sexuelle peuvent naître, se déplacer et partiellement perdre leur fonction, le tout au sein d’une même espèce.
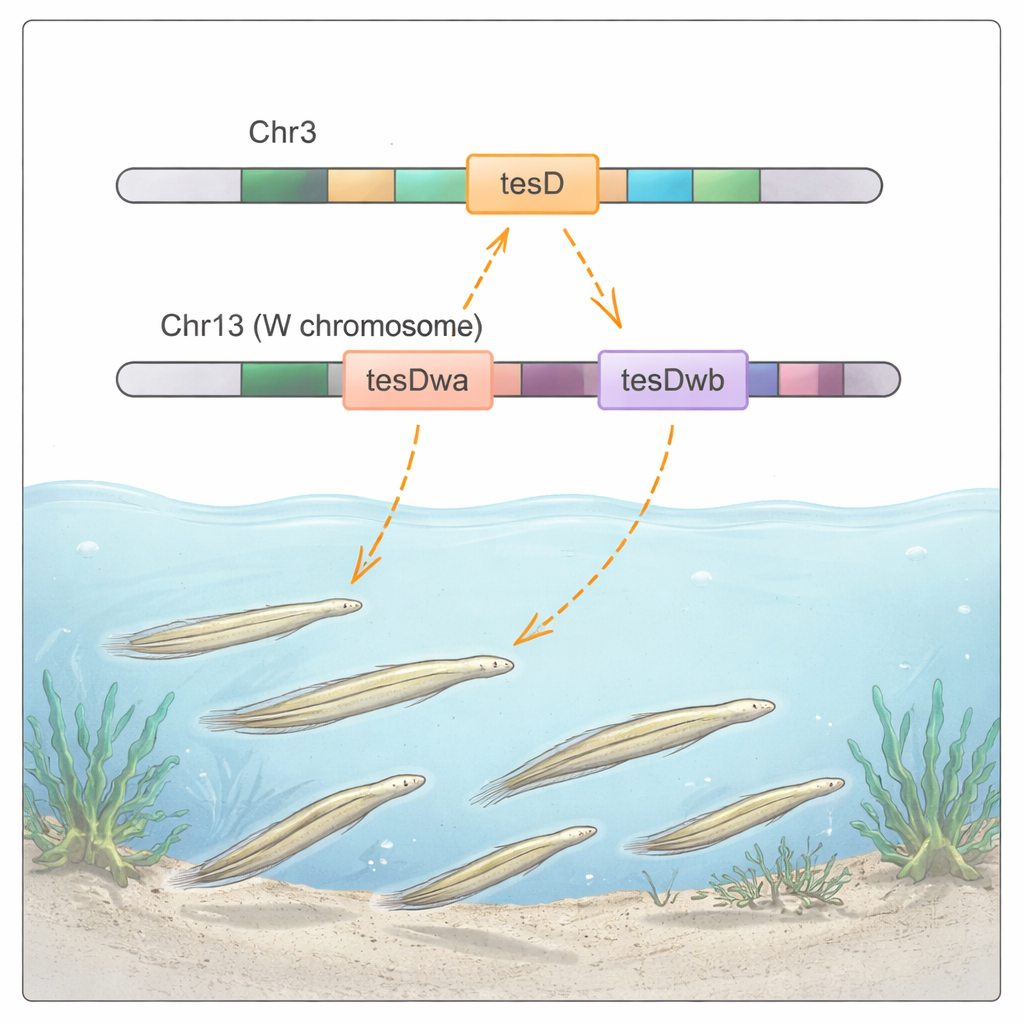
Un animal simple avec un interrupteur sexuel complexe
L’amphioxus, ou lancette, vit enfoui dans les sables peu profonds et occupe une position clé sur l’arbre évolutif entre les invertébrés et les vertébrés. Des travaux antérieurs ont montré que plusieurs espèces d’amphioxus, dont Branchiostoma belcheri, possèdent un système ZW, où les femelles portent des chromosomes sexuels Z et W, mais ces chromosomes paraissent presque identiques au microscope. Cela rend difficile l’identification précise des régions d’ADN qui déterminent le sexe. En utilisant de nouvelles assemblées de génome de haute qualité provenant de plusieurs individus de B. belcheri, les chercheurs ont réexaminé l’emplacement des régions déterminant le sexe et comment elles diffèrent entre mâles et femelles.
Un gène clé, copié et déplacé
L’équipe s’est concentrée sur un gène nommé tesD, qui n’est actif que dans les testicules chez trois espèces d’amphioxus. En utilisant l’édition génique CRISPR dans l’espèce apparentée B. floridae, ils ont inactivé tesD. Les mâles génétiques dépourvus d’un tesD fonctionnel ne formaient plus de testicules et ont développé des ovaires, tout en restant par ailleurs en bonne santé. Cela montre que tesD est essentiel et spécifique au développement mâle, agissant comme un commutateur maître dans la voie menant aux organes produisant les spermatozoïdes. Fait intrigant, des gènes similaires sont absents des vertébrés, ce qui suggère qu’il s’agit d’une solution ancienne des chordés qui a été remplacée plus tard dans notre propre lignée.
Deux régions propres aux femelles nées d’un ADN sautillant
Chez B. belcheri lui‑même, les auteurs ont découvert non pas une mais deux régions distinctes spécifiques aux femelles sur le chromosome 13. Les deux régions contiennent des copies supplémentaires de tesD, nommées tesDwa et tesDwb. Ces copies ne sont pas apparues par une simple duplication en tandem près du gène original ; elles ont été transportées par des éléments mobiles d’ADN appelés transposons, capables de se couper et de se coller ailleurs dans le génome. Une région déterminant le sexe s’est insérée à l’intérieur d’un gène nommé twai, et l’autre s’est insérée dans la partie terminale d’un gène nommé vps9c. Des enquêtes génétiques et des tests PCR ciblés ont montré qu’environ la moitié des femelles portent la région la plus ancienne avec tesDwa, et l’autre moitié porte la région plus récente avec tesDwb, tandis que les mâles en sont généralement dépourvus.
Comment des gènes copiés contribuent à créer des femelles
Avoir des copies supplémentaires d’un gène favorisant le développement mâle sur le chromosome W femelle peut sembler paradoxal. La solution tient à la façon dont ces copies sont exploitées. Dans les ovaires, les copies liées au W, tesDwa et tesDwb, sont lues dans la direction opposée par rapport à l’tesD autosomal d’origine, produisant des ARN longs non codants plutôt que des protéines. Ces longs ARN s’alignent en antisens avec le message normal de tesD et sont transcrits conjointement avec leurs gènes hôtes, ce qui suggère qu’ils détournent des promoteurs locaux. La présence de ces ARN antisens s’accompagne d’un arrêt de l’expression du gène tesD d’origine au niveau de l’ADN chez les femelles, comme le montrent des essais d’accessibilité de la chromatine. En pratique, les copies liées au W agissent comme des silencieux, éteignant le commutateur mâle et orientant le développement vers des ovaires.
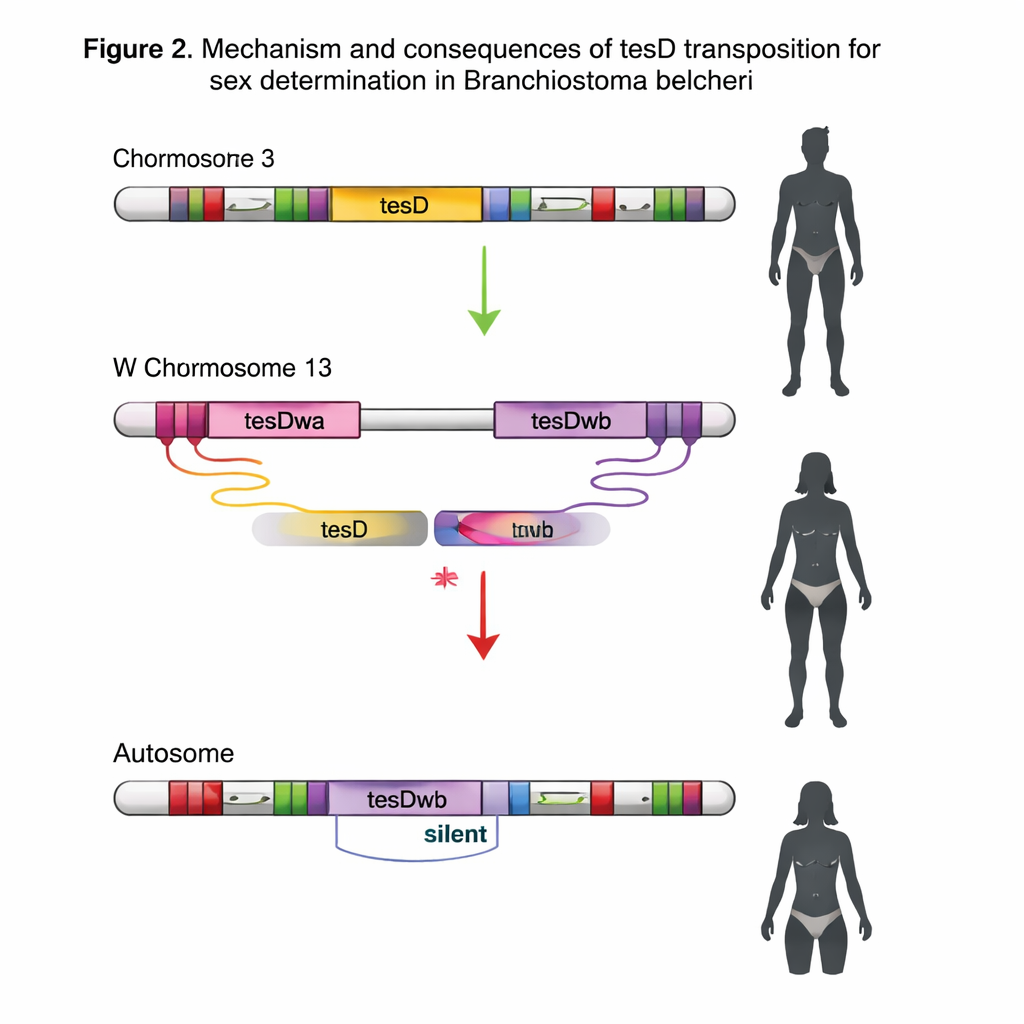
Quand l’interrupteur sexuel saute et se tait
La région la plus jeune contenant tesDwb est encore mobile. Les transposons qui l’entourent portent des structures répétées intactes signalant une activité récente, et les auteurs ont trouvé des individus où ce cassette a sauté du chromosome W vers des chromosomes ordinaires (autosomiques), incluant un télomère et un intron d’un autre gène. Dans ces nouveaux emplacements, cependant, tesDwb n’est pas transcrit, son effet d’inhibition sur tesD est perdu, et il ne coïncide plus avec le sexe. Environ 5–10 % des mâles et des femelles portent de telles copies « silencieuses », illustrant comment des modules de détermination sexuelle mobiles peuvent se répandre, devenir inactifs, et peut‑être être remplacés au fil du temps évolutif.
Ce que cela signifie pour l’évolution du sexe
Pour un non‑spécialiste, le message principal est que la détermination du sexe n’est pas figée une fois pour toutes, même au sein d’une seule espèce. Chez B. belcheri, un seul gène qui produit le phénotype mâle, tesD, a été copié, déplacé par un ADN sautillant, et réaffecté pour aider à produire des femelles en bloquant sa propre activité. Des régions déterminant le sexe anciennes et nouvelles coexistent désormais, et la plus récente est encore en mouvement dans le génome. Ce type de remaniement continu peut aider à expliquer pourquoi de nombreux animaux conservent des chromosomes sexuels d’apparence ordinaire, sans la dégénérescence importante observée sur le chromosome Y humain, et il offre un instantané vivant de la manière dont de nouveaux systèmes de détermination sexuelle naissent et entrent en compétition au cours du temps évolutif.
Citation: Li, H., Liu, F., Li, J. et al. Evolutionary dynamics of sex determination in Branchiostoma belcheri driven by repeated transposition of a single novel gene. Nat Commun 17, 1616 (2026). https://doi.org/10.1038/s41467-026-68322-6
Mots-clés: détermination du sexe, amphioxus, éléments transposables, lncRNA, génétique évolutive