Clear Sky Science · fr
La structure du complexe SHOC2-KRAS-PP1C révèle des déterminants spécifiques aux isoformes RAS et des perspectives pour cibler l’assemblage du complexe par des inhibiteurs de RAS
Comment les cellules décident de croître
Nos cellules s’appuient sur un câblage interne pour décider quand croître, se diviser ou rester au repos. Au cœur de ce système se trouvent les protéines RAS, de petits interrupteurs moléculaires qui dysfonctionnent souvent dans le cancer. Cette étude examine en profondeur comment un groupe particulier de protéines — SHOC2, RAS et PP1C — s’assemble pour actionner un interrupteur clé de croissance, et comment les médicaments anticancéreux modernes pourraient être ajustés pour mieux bloquer ce processus et empêcher les tumeurs de contourner le traitement.
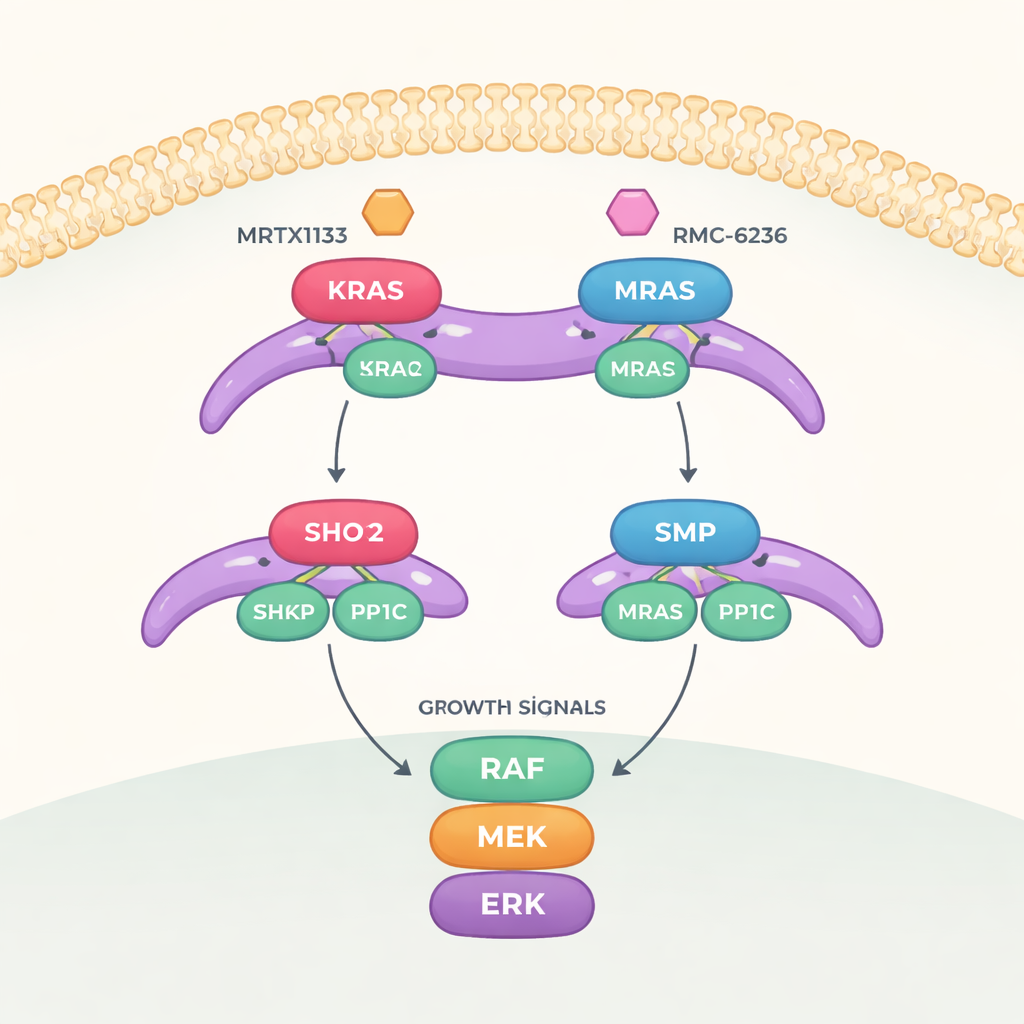
Un interrupteur de croissance à trois éléments critiques
Le travail se concentre sur une voie de signalisation appelée voie MAPK, qui transmet les signaux de croissance de la surface cellulaire jusqu’au noyau. Pour activer pleinement cette voie, une autre protéine nommée RAF doit passer d’un état « éteint » à un état « allumé ». Ce basculement est contrôlé par un complexe tripartite composé de SHOC2 (un échafaudage qui maintient les éléments ensemble), PP1C (une enzyme qui retire une marque phosphate) et une protéine RAS active. Une fois assemblé, ce trio enlève une marque phosphate spécifique de RAF, lui permettant d’activer la cascade de croissance en aval.
Pourquoi un partenaire de faible affinité compte malgré tout en cancérologie
Il existe plusieurs types de protéines RAS. MRAS forme un complexe très stable avec SHOC2 et PP1C, tandis que les plus connus KRAS, HRAS et NRAS forment des versions plus faibles du même complexe. De façon surprenante, les cellules cancéreuses conduites par des mutants de KRAS, HRAS ou NRAS sont fortement dépendantes de SHOC2, même si leurs complexes sont moins stables. De larges jeux de données de criblage génétique montrent que de nombreuses tumeurs portant certaines mutations RAS — en particulier celles touchant des positions clés comme Q61 et G13 — sont très sensibles à la perte de SHOC2, ce qui signifie que cet assemblage est essentiel à leur survie.
Révéler la forme du complexe KRAS
Jusqu’à présent, les scientifiques n’avaient obtenu qu’une structure haute résolution du complexe étroit à base de MRAS. La version plus faible à base de KRAS se désorganisait trop facilement pour être capturée. Dans cette étude, les auteurs ont utilisé des mutations associées à la maladie qui renforcent subtilement les contacts entre les composants afin de stabiliser le complexe SHOC2–KRAS–PP1C suffisamment longtemps pour l’imager par cryo‑microscopie électronique. Ils ont constaté que l’architecture générale correspond étroitement à celle du complexe MRAS, mais que KRAS manque de plusieurs petites caractéristiques structurelles que MRAS utilise pour saisir SHOC2 et PP1C plus fermement. En conséquence, l’assemblage à base de KRAS présente une surface de contact moindre et forme moins de liaisons, expliquant pourquoi il est intrinsèquement moins stable, même s’il reste très important dans les tumeurs où KRAS est hyperactif.
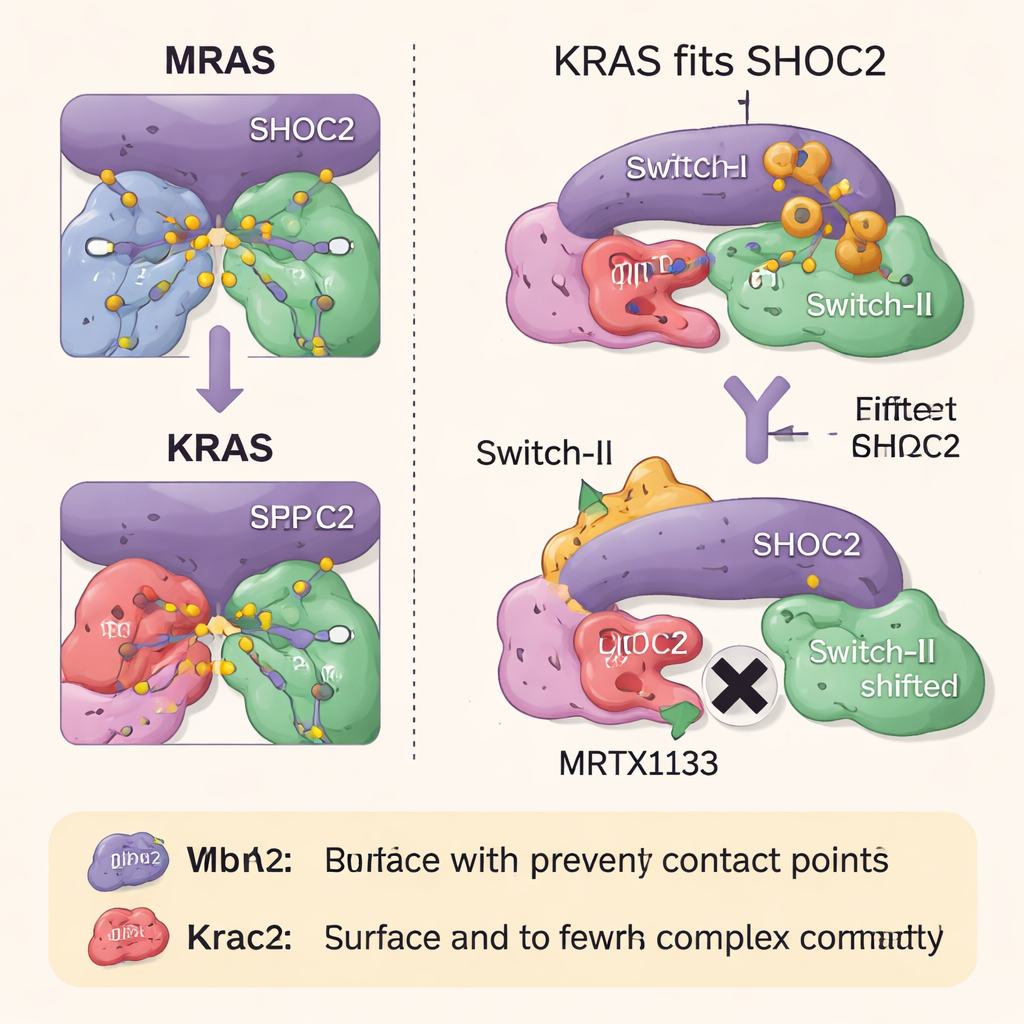
Comment les médicaments ciblant RAS bloquent l’assemblage du complexe
L’équipe a ensuite étudié comment deux classes de médicaments ciblant RAS influencent ce complexe tripartite. MRTX1133, conçu pour se lier à une poche proche d’une région flexible de KRAS appelée Switch‑II, verrouille cette région dans une conformation qui entre en conflit avec la surface de SHOC2. Cela empêche fortement la formation de nouveaux complexes SHOC2–KRAS–PP1C, bien que le composé soit moins efficace pour dissocier ceux déjà formés. Un deuxième médicament, RMC‑6236, agit en association avec une protéine auxiliaire (la cyclophiline A) et bloque également les mêmes surfaces de KRAS nécessaires à la liaison de SHOC2. Aucun des deux médicaments ne se lie naturellement à MRAS, si bien que le complexe à haute affinité MRAS reste intact et peut contribuer à réactiver la voie de croissance lorsque KRAS est inhibé.
Vers un double ciblage pour prévenir la résistance
Pour tester la faisabilité d’un double ciblage, les chercheurs ont conçu une version de MRAS dont la poche Switch‑II avait été modifiée de sorte que MRTX1133 puisse désormais s’y lier. Ce mutant formait toujours un complexe solide avec SHOC2 et PP1C, mais le médicament bloquait à présent son assemblage et réduisait sa capacité à activer RAF dans des essais in vitro. Avec les données sur des composés liant SHOC2, ces résultats montrent qu’il est réaliste de concevoir des médicaments qui inhibent à la fois les complexes fondés sur KRAS et ceux fondés sur MRAS. Pour un non‑spécialiste, le message clé est que les cellules cancéreuses utilisent plusieurs interrupteurs étroitement apparentés pour maintenir la transmission des signaux de croissance, surtout lorsqu’un interrupteur est ciblé par un médicament. En comprenant précisément les formes et les contacts au sein de ces assemblages protéiques, les chercheurs peuvent désormais concevoir des thérapies qui visent simultanément les voies de secours, rendant plus difficile l’adaptation et la résistance des cancers pilotés par RAS.
Citation: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Mots-clés: signalisation RAS, inhibiteurs de KRAS, voie MAPK, complexes protéiques, résistance aux médicaments