Clear Sky Science · fr
Contrôle réversible par les lipides de l’ouverture pH‑dépendante de connexine‑46/50 révélé par cryo‑EM
Pourquoi de minuscules canaux cellulaires comptent pour la santé et la maladie
Chaque seconde, nos cellules échangent des signaux électriques et de petites molécules via des tunnels microscopiques appelés jonctions communicantes. Ces canaux synchronisent les battements du cœur, aident le cerveau à éliminer des sous‑produits toxiques et contribuent à la transparence du cristallin. Lorsque l’intérieur des cellules devient acide, comme cela se produit lors d’un AVC, d’un infarctus ou de la formation d’une cataracte, beaucoup de ces canaux se ferment — mais la façon dont ils détectent et répondent à l’acidité est restée longtemps mystérieuse. Cette étude utilise la cryo‑microscopie électronique à haute résolution pour montrer, presque atome par atome, comment des canaux spécifiques du cristallin se ferment en réponse à l’acidité et comment ce processus peut être entièrement réversible.
Des tunnels cellulaires qui maintiennent la cohérence des tissus
Les jonctions communicantes sont composées de protéines appelées connexines, qui s’assemblent en canaux annulaires traversant les membranes de deux cellules voisines. Ce travail se concentre sur une paire de connexines étroitement apparentées, connexine‑46 et connexine‑50, qui forment des canaux dans le cristallin de l’œil. Ces canaux permettent le passage direct d’ions et de petites molécules entre les cellules, contribuant à la clarté du cristallin et à la santé des tissus. Toutefois, lorsque les cellules sont stressées, ces mêmes canaux peuvent devenir des voies de transmission de signaux dommageables. Pour protéger les tissus, les jonctions communicantes se ferment lorsque l’intérieur des cellules devient plus acide. Comprendre le mécanisme détaillé de cette « ouverture dépendante du pH » est important pour expliquer comment les tissus survivent au stress et pourquoi certaines mutations entraînent des maladies comme la cataracte.
Observer les mouvements des canaux par cryo‑EM
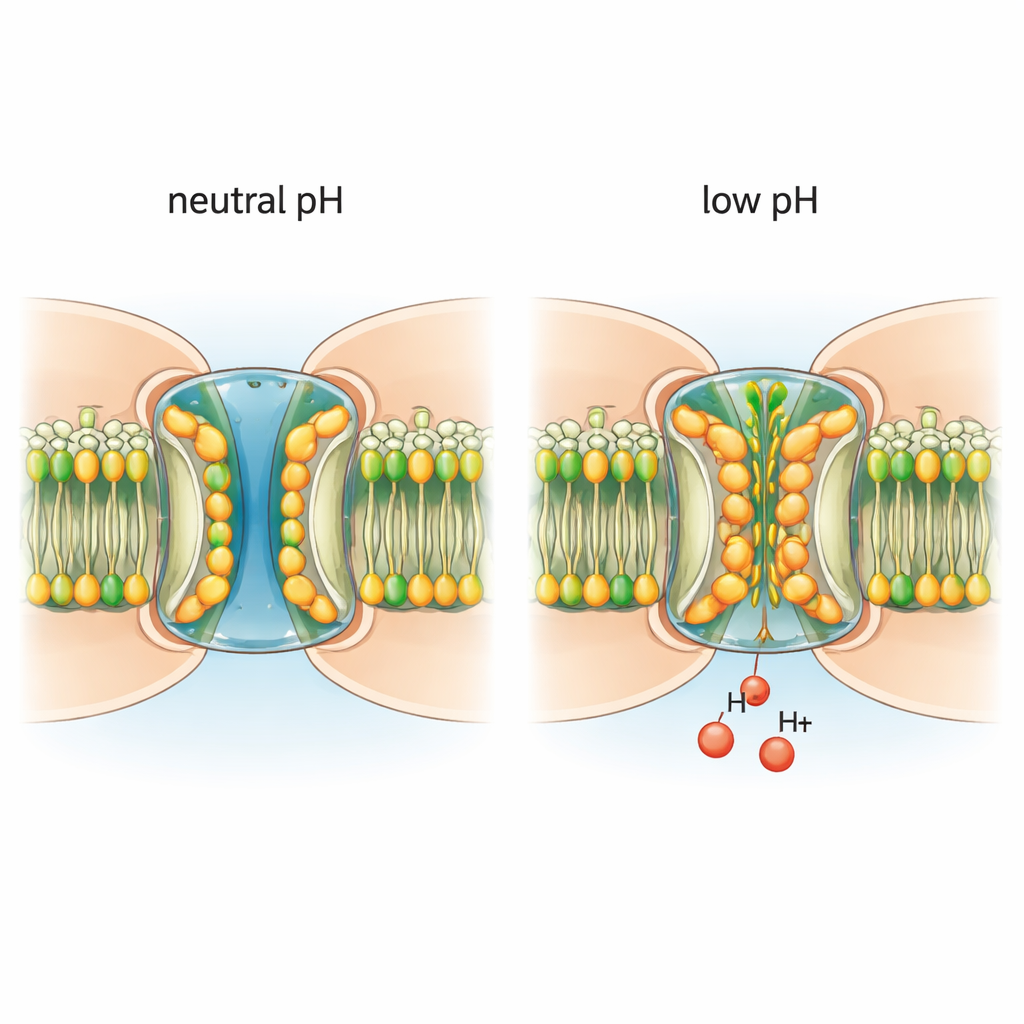
Les chercheurs ont purifié des canaux natifs connexine‑46/50 à partir de cristallins de moutons âgés et les ont incorporés dans une membrane modèle. En utilisant la cryo‑microscopie électronique, ils ont imagé les canaux à résolution quasi‑atomique en conditions neutres, favorisant un pore ouvert, et en conditions légèrement acides, déclenchant la fermeture. À pH neutre, les canaux adoptent majoritairement un état ouvert stable, avec un tunnel central suffisamment large pour les ions et petites molécules et un segment flexible, le domaine N‑terminal, qui borde l’entrée du pore. Dans ces conditions, le pore est dégagé : aucune molécule étrangère ne l’obstrue et les lipides membranaires environnants restent organisés en couches régulières.
L’acidité attire les lipides à l’intérieur du pore
Lorsque l’environnement devient légèrement acide, l’architecture du canal change de façon spectaculaire. Des molécules lipidiques de la membrane environnante sont aspirées dans le pore, se glissant entre et sous les segments N‑terminaux. Ces lipides envahissants forment un « joint » hydrophobe à deux couches qui pousse les domaines N‑terminaux vers l’intérieur, rétrécissant le canal et contribuant à bloquer le passage. Des lipides supplémentaires se coincent entre des sous‑unités protéiques voisines au niveau de leurs interfaces, apparemment en tant que voies d’entrée depuis la membrane vers le pore. Fait important, lorsque les canaux sont placés dans un environnement détergent dépourvu d’une vraie membrane lipidique, le pH bas n’induit plus ces changements structuraux. Cela démontre que les lipides réels ne sont pas de simples spectateurs : ce sont des partenaires nécessaires au processus d’ouverture dépendante du pH.
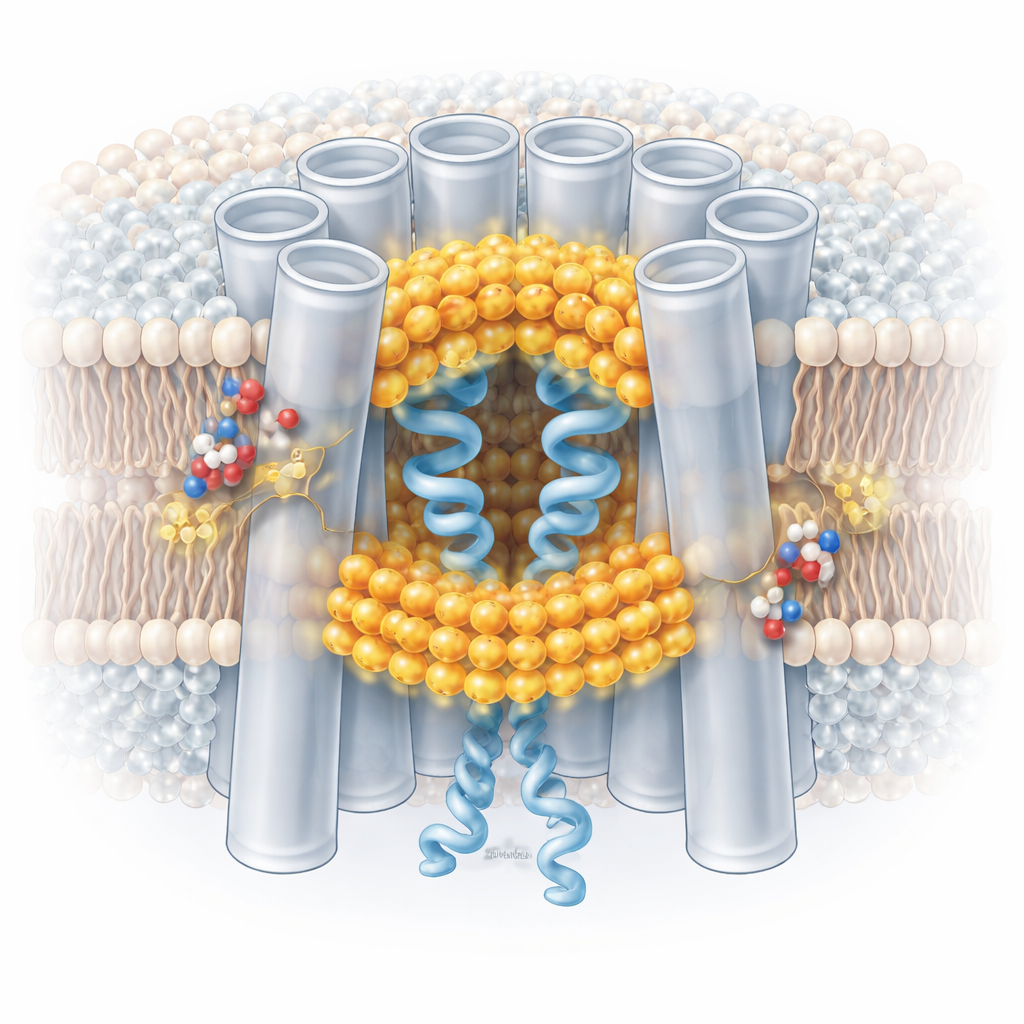
Un capteur de sécurité réversible et finement réglé
En suivant des millions de particules de canaux individuellement, les auteurs ont constaté que le pH bas ne bascule pas simplement les canaux d’un état complètement ouvert à un état complètement fermé. Au contraire, il déplace la population vers un mélange d’états : certaines sous‑unités au sein d’un canal présentent des conformations fermées stabilisées par des lipides tandis que d’autres restent plus ouvertes. Le comportement de fermeture est en grande partie non coopératif — chaque unité constitutive du canal peut répondre de manière plutôt indépendante. Les conditions acides favorisent ces conformations fermées, mais lorsque le pH revient à la neutralité, les lipides du pore se rétractent dans la membrane et les canaux retournent à l’état ouvert. Des acides aminés conservés appelés histidines, qui gagnent une charge positive à faible pH, semblent aider à recruter et stabiliser les lipides interfaciaux qui initient ce processus, offrant un capteur moléculaire plausible du pH.
Implications pour les cataractes et la protection tissulaire
Ces résultats soutiennent un modèle dans lequel les lipides agissent comme des bouchons mobiles qui contrôlent de manière réversible le flux à travers les jonctions communicantes en réponse à l’acidité. Dans le cristallin, un tel mécanisme peut aider à isoler les cellules endommagées et à empêcher la propagation de signaux toxiques, mais une fermeture chronique ou mal régulée pourrait aussi contribuer à la formation de cataractes liées à l’âge. Parce que des intrusions lipidiques similaires ont été observées dans des familles de canaux apparentées, ce travail suggère un principe plus général : en cas de stress, les membranes cellulaires elles‑mêmes peuvent fournir des composants dynamiques qui aident à commuter des canaux vitaux en position ouverte ou fermée, ouvrant de nouvelles pistes pour des médicaments qui stabilisent l’un ou l’autre état en cas de maladie.
Citation: Jarodsky, J.M., Myers, J.B. & Reichow, S.L. Reversible lipid-mediated pH-gating of connexin-46/50 by cryo-EM. Nat Commun 17, 1606 (2026). https://doi.org/10.1038/s41467-026-68311-9
Mots-clés: jonctions communicantes, connexine 46/50, ouverture dépendante du pH, cataracte, cryo‑EM