Clear Sky Science · fr
La transcriptomique dynamique unicellulaire révèle la formation d’un réseau neural guidé par lsamp chez les mâles de S. japonicum stimulant la reproduction des femelles
Pourquoi la vie amoureuse d’un parasite compte
La schistosomiase est une maladie parasitaire qui rend malades plus de 250 millions de personnes, principalement dans des régions pauvres où les soins médicaux sont limités. La maladie n’est pas causée par des morsures ou des toxines des vers, mais par l’énorme nombre d’œufs pondus par les femelles à l’intérieur du corps. De manière surprenante, les femelles ne peuvent mûrir et commencer à pondre qu’après s’être accouplées avec un mâle. Cette étude pose une question simple mais cruciale : qu’est-ce que le mâle fait exactement pour déclencher la fertilité de la femelle — et pourrait-on interrompre ce déclencheur pour arrêter la maladie ?
Cartographier un monde caché cellule par cellule
Pour répondre à cette question, les chercheurs ont construit un « atlas cellulaire » détaillé du trématode hématophage Schistosoma japonicum pendant la fenêtre clé où mâles et femelles s’apparient et deviennent sexuellement matures. En utilisant le séquençage d’ARN unicellulaire, une technique qui révèle quels gènes sont actifs dans chaque cellule individuelle, ils ont analysé plus de 100 000 cellules provenant de vers collectés à quatre moments après l’infection chez la souris. Ils ont identifié 76 types cellulaires distincts, y compris de nombreux types de neurones, des cellules souches et des cellules reproductrices. Cela leur a permis de suivre comment des populations cellulaires spécifiques s’étendent, se réduisent ou changent d’identité à mesure que les vers croissent et commencent à se reproduire.
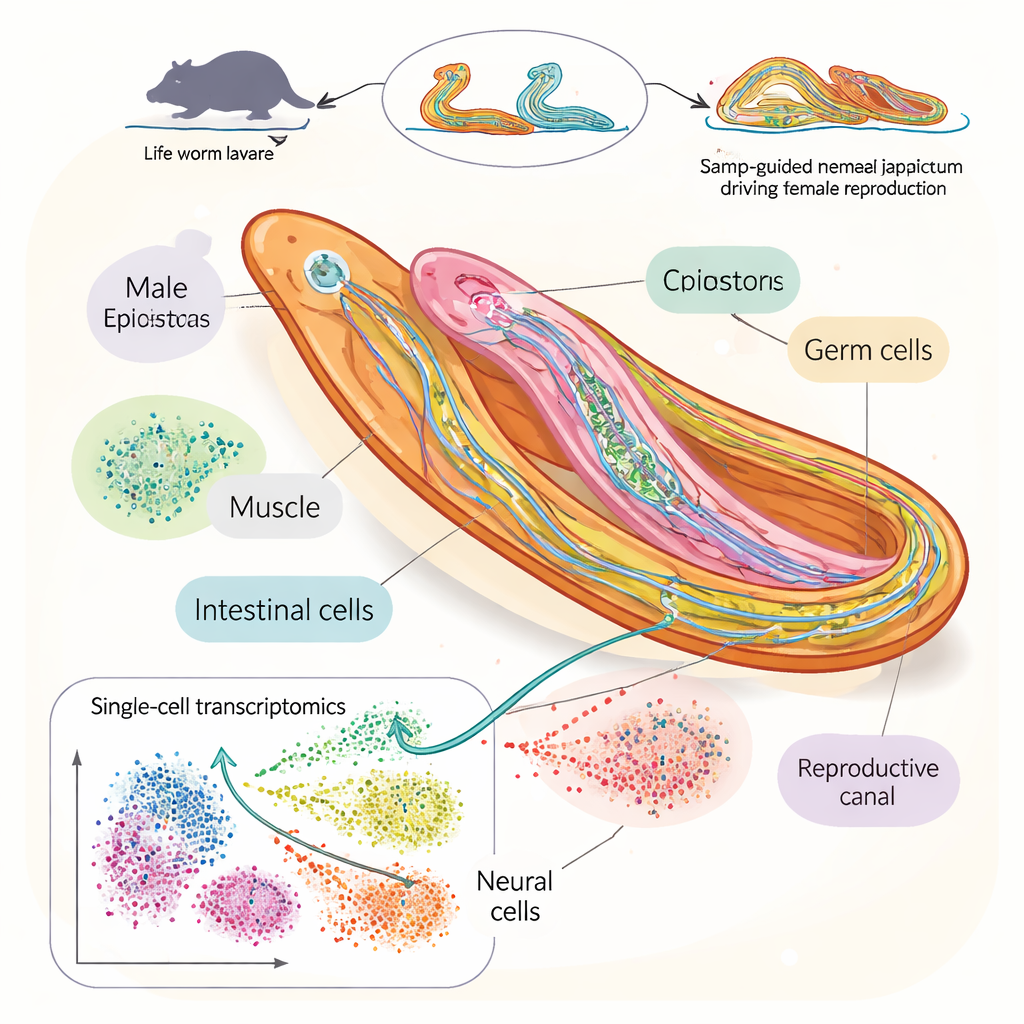
Suivre l’essor des œufs et des spermatozoïdes
En se concentrant sur les cellules des testicules, des ovaires et des tissus associés, l’équipe a reconstruit le développement progressif des spermatozoïdes et des ovules. Ils ont montré comment les cellules souches germinales donnent naissance à des spermatozoïdes et des ovocytes de stade avancé via des programmes d’activité génique distincts chez les mâles et les femelles. Chez les femelles, les gènes soutenant la croissance des œufs mettent l’accent sur la production et l’emballage de protéines, tandis que chez les mâles ils portent davantage sur des structures comme les cils et les microtubules qui favorisent la mobilité des spermatozoïdes. L’étude a également cartographié le développement de l’organe massif de soutien aux œufs chez la femelle, la vitellaire, à travers des stades intermédiaires, et identifié de nouveaux marqueurs génétiques révélant le degré de maturité de chaque tissu reproducteur.
Un circuit nerveux uniquement masculin dans un canal d’accolade
Une des découvertes les plus marquantes provient du système nerveux. L’atlas a révélé, non pas une collection lâche de neurones, mais cinq lignées neuronales distinctes, dont plusieurs différaient entre mâles et femelles. Trois types de neurones — nommés N2.2, N3.2 et N4.3 — étaient fortement enrichis chez les mâles et s’agrégeaient à l’intérieur du canal gyécophorique, une rainure spécialisée que le mâle utilise pour enserrer la femelle. Parmi eux, les neurones N4.3 se distinguaient car ils exprimaient un gène appelé nrps, qui code pour l’enzyme produisant BATT, un petit peptide phéromonal auparavant montré pour stimuler le développement sexuel des femelles. Autrement dit, ces cellules N4.3 constituent les « postes d’émission » mâles qui activent la fertilité féminine.
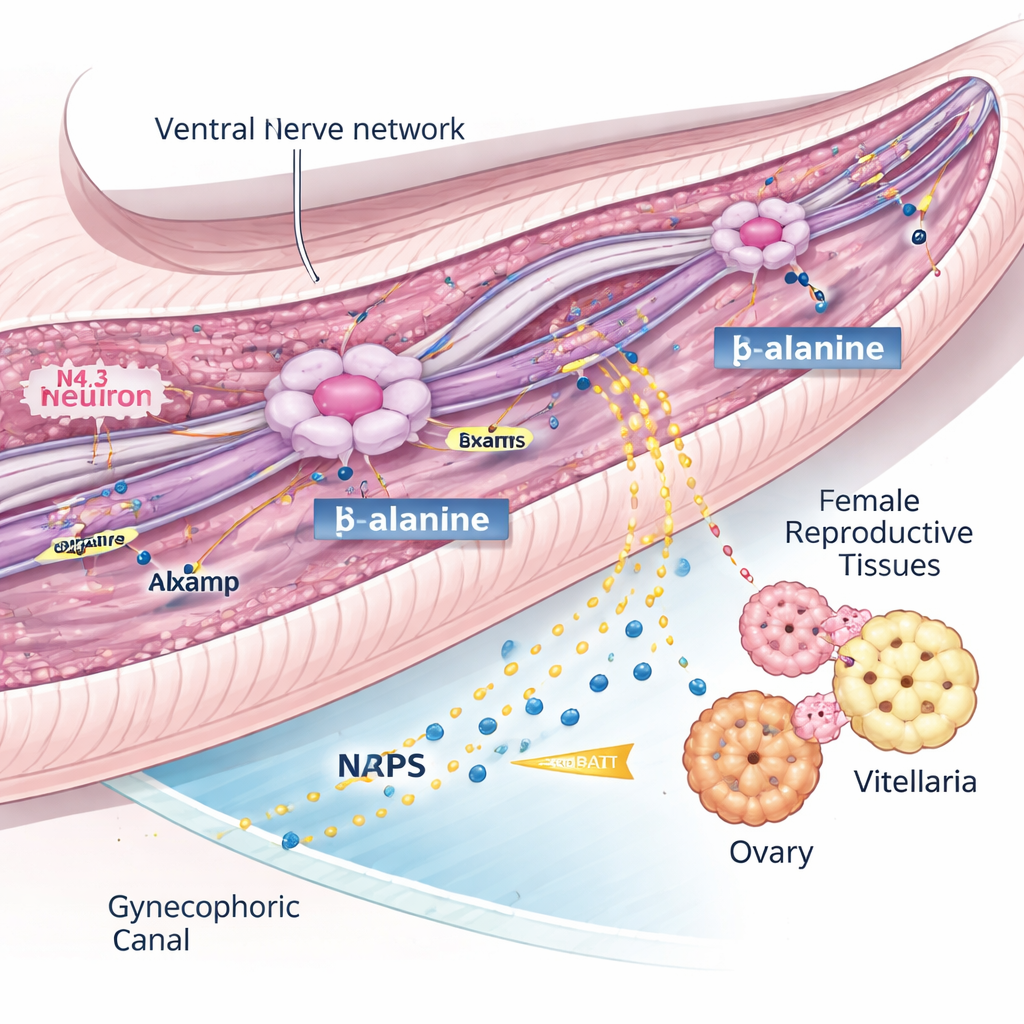
Une molécule guide qui maintient le signal
Pour comprendre le fonctionnement des neurones N4.3, les chercheurs ont cherché des gènes susceptibles d’orienter leur développement et leur fonction. Ils ont mis en avant lsamp, un gène connu chez d’autres animaux pour aider les neurones à se connecter et à maintenir leurs axones. Chez les trématodes mâles, lsamp était activé dans les mêmes neurones N4.3 producteurs de l’enzyme BATT, et son activité augmentait fortement à mesure que les vers mûrissaient. En réduisant lsamp chez les mâles par interférence ARN, l’équipe a constaté que les femelles accouplées ne parvenaient pas à développer complètement leurs ovaires et leur vitellaire et ne pondaient presque pas d’œufs. Pourtant, les neurones N4.3 restaient présents, le gène nrps restait actif, et les précurseurs chimiques de BATT n’étaient pas modifiés. En revanche, les mâles déficients en lsamp présentaient des fibres nerveuses endommagées et un transport vésiculaire perturbé le long de microtubules stabilisés, et ils produisaient beaucoup moins de BATT à l’intérieur de leur corps et dans le milieu environnant. Cela suggère que lsamp est essentiel pour maintenir un réseau nerveux ventral qui livre un précurseur clé, probablement la β-alanine, aux neurones N4.3 afin qu’ils puissent synthétiser suffisamment de phéromone pour activer la femelle.
Atténuer l’interrupteur reproducteur
Pour les non-spécialistes, le message principal est que la capacité de ce parasite à provoquer la maladie dépend d’une conversation intime entre vers mâles et femelles, menée par un réseau nerveux spécialisé et une petite phéromone. L’étude montre qu’une seule molécule guide, lsamp, aide à construire et maintenir le câblage nerveux ventral du mâle ; lorsque ce câblage échoue, le mâle ne peut plus envoyer un signal chimique suffisamment fort pour faire mûrir pleinement les organes reproducteurs de la femelle, et la ponte chute fortement. En cartographiant les cellules du parasite à haute résolution et en découvrant ce circuit neural exclusif aux mâles, le travail ouvre des pistes pour bloquer la production d’œufs — offrant une stratégie potentielle pour lutter contre la schistosomiase là où le traitement actuel repose sur un seul médicament de plus en plus âgé.
Citation: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Mots-clés: schistosomiase, transcriptomique unicellulaire, reproduction du parasite, circuits neuronaux, signalisation par phéromones