Clear Sky Science · fr
Mécanisme de résistance du SARS-CoV-2 aux antiviraux à base d’analogues nucléotidiques
Comment le virus contourne des médicaments antiviraux clés
Le virus responsable de la COVID-19 appartient à un groupe rare de virus à ARN capables de relire leur matériel génétique, ce qui le rend particulièrement performant pour résister à certains de nos meilleurs antiviraux. Cette étude explore les détails à l’échelle atomique de la manière dont le SARS‑CoV‑2 détecte et élimine une classe largement utilisée de médicaments appelés analogues nucléotidiques, et explique pourquoi des médicaments efficaces contre d’autres virus sont souvent moins performants contre les coronavirus.
Une lutte pour l’ARN viral
Le SARS‑CoV‑2 copie son génome ARN d’environ 30 000 lettres à l’aide d’une grande machinerie moléculaire appelée complexe de réplication‑transcription. Au centre se trouve l’ARN‑dépendante ARN polymérase (RdRp), qui synthétise de nouveaux brins d’ARN, et une unité distincte, l’exonucléase (ExoN), qui relit et émonde les erreurs. De nombreuses pilules antivirales, y compris des médicaments développés à l’origine contre l’hépatite C, imitent suffisamment les unités de base de l’ARN pour être incorporées par la RdRp, mais avec des modifications subtiles qui bloquent la copie ou introduisent des erreurs. Malheureusement, les coronavirus possèdent ExoN, qui peut reconnaître ces imposteurs une fois intégrés dans la chaîne d’ARN et les exciser, sauvant ainsi la réplication virale.
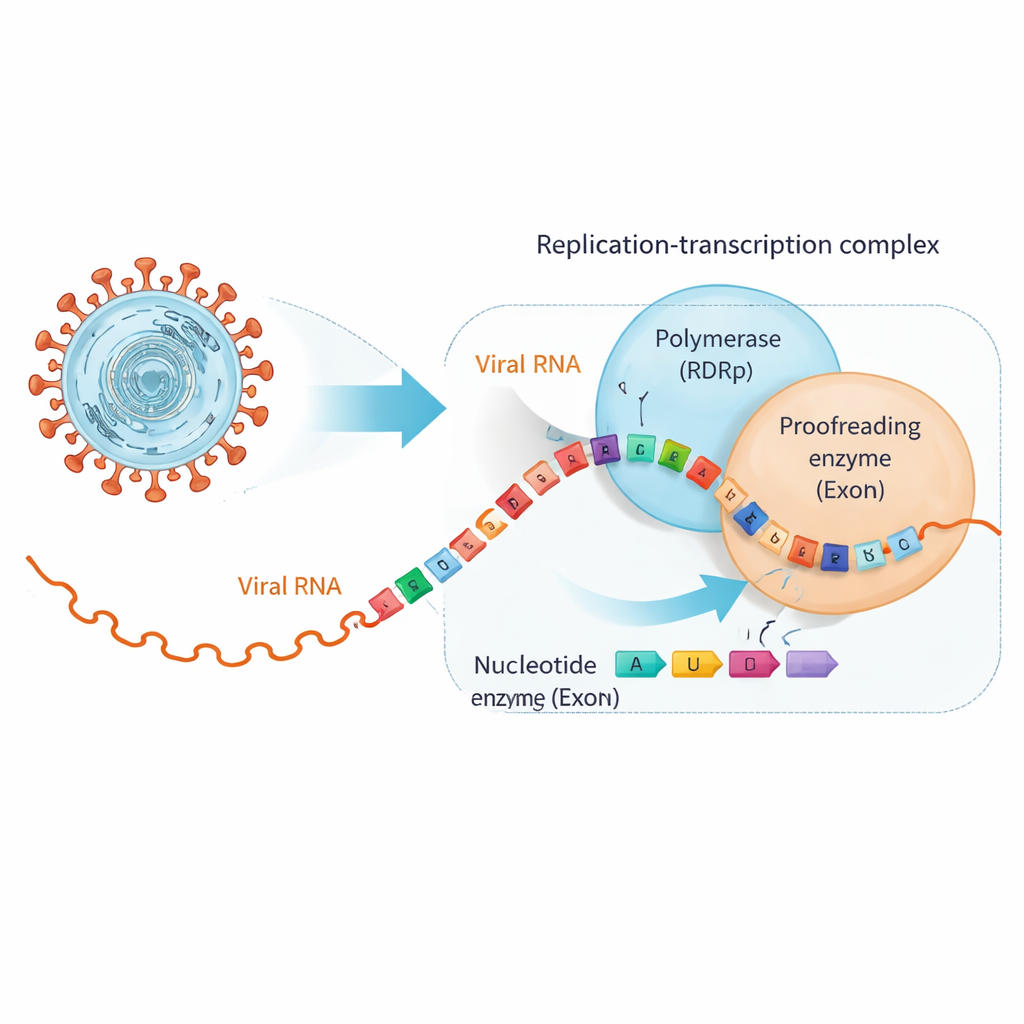
Quand des médicaments utiles font changer de partenaire à l’ARN
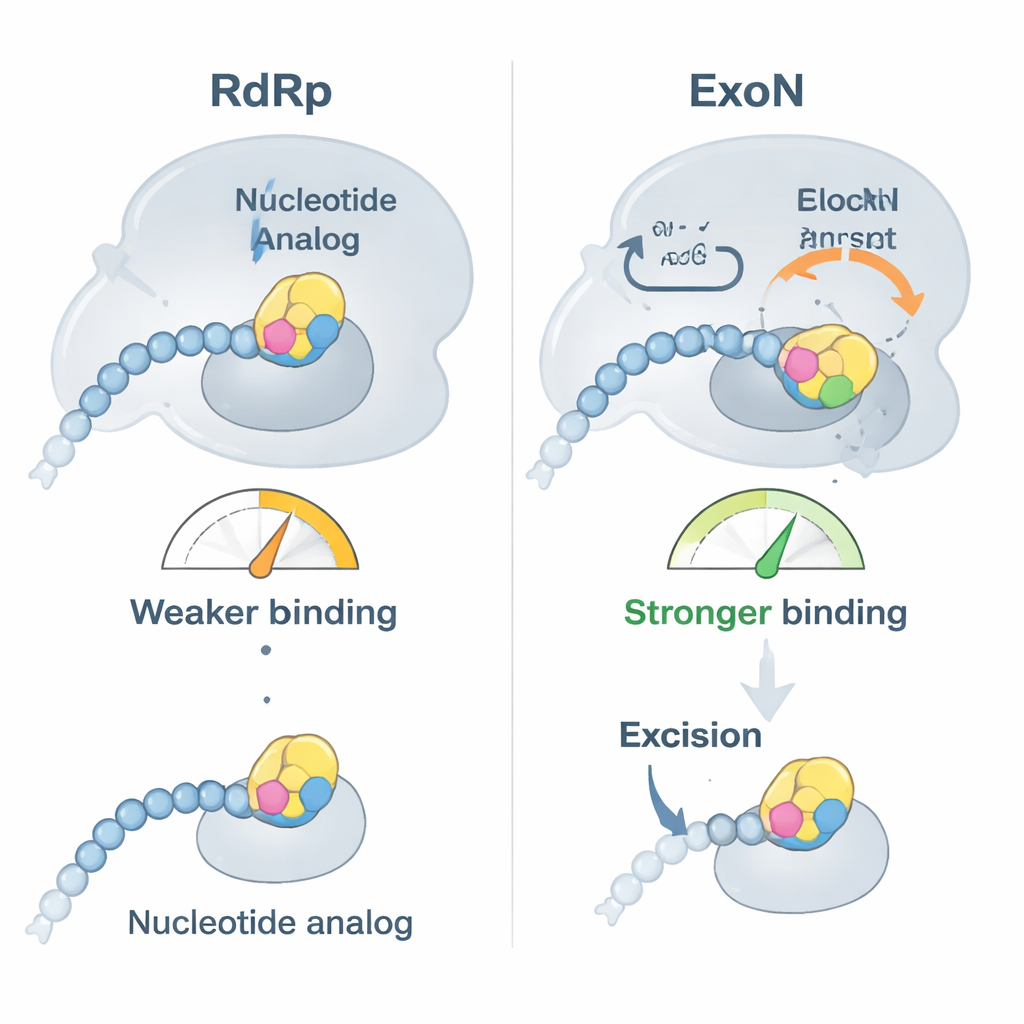
Les chercheurs se sont concentrés sur deux antiviraux d’intérêt clinique, le bemnifosbuvir et le sofosbuvir, conçus pour agir comme des unités bâtardes de l’ARN. Ils ont d’abord montré que la polymérase du SARS‑CoV‑2 insère facilement ces analogues à l’extrémité d’un brin d’ARN puis cesse en grande partie d’allonger la chaîne, comme prévu. Cependant, des tests d’affinité ont révélé une torsion : une fois qu’un analogue se trouve à la pointe de l’ARN, l’ARN ne se lie plus aussi fermement à la polymérase mais se fixe plus fortement à ExoN. En pratique, l’ARN modifié par le médicament est poussé hors de la machine de copie et remis au correcteur, qui a alors la possibilité de couper le nucléotide problématique et de permettre à la réplication de reprendre.
Une relecture ralentie mais non stoppée
Des expériences biochimiques de suivi temporel ont montré qu’ExoN retire bien le bemnifosbuvir et le sofosbuvir de l’ARN, mais plus lentement qu’il n’élimine les nucléotides normaux. Dans des réactions sans cellules, les deux analogues bloquaient fortement la synthèse d’ARN ultérieure — pourtant, lorsque ExoN actif était ajouté, une fraction notable des chaînes d’ARN arrêtées était sauvée et prolongée. Un mutant d’ExoN inactivé ne pouvait pas le faire, confirmant que l’activité de relecture est responsable d’une grande partie de l’annulation de l’effet des médicaments. La présence de la polymérase en parallèle d’ExoN accélère en fait l’élimination des analogues, suggérant que les deux enzymes virales travaillent de concert pour dégager les obstacles et maintenir la réplication.
Observer le correcteur à résolution atomique
Pour comprendre comment ExoN reconnaît et réagit à ces médicaments, l’équipe a utilisé la cryo‑microscopie électronique à haute résolution pour résoudre les structures du complexe ExoN lié à des brins d’ARN se terminant soit par le bemnifosbuvir soit par le sofosbuvir. Ces structures, suffisamment nettes pour distinguer des groupes chimiques individuels, ont révélé que l’anneau de sucre modifié de chaque médicament s’insère dans une poche hydrophobe formée par une courte boucle de la protéine ExoN. Cette affinité accrue explique la liaison plus forte de l’ARN contenant le médicament à ExoN. Mais cela a aussi un effet secondaire inattendu : en tirant sur cette boucle, les médicaments perturbent l’agencement précis d’une boucle catalytique voisine qui maintient en place une histidine clé. Lorsque cette histidine bascule hors du site de coupe, le centre actif d’ExoN devient partiellement désactivé, ralentissant mais n’empêchant pas complètement l’excision de l’analogue.
Un commutateur intégré qui module la relecture virale
La mutation d’acides aminés individuels au sein de la boucle sensible a confirmé son importance. Des changements sur quatre résidus conservés ont fortement réduit la capacité d’ExoN à couper aussi bien les extrémités ARN standards que les extrémités terminées par des médicaments, et ont aussi modifié le nucléotide final que ExoN préfère retirer. Cela identifie la boucle comme un régulateur allostérique — un commutateur mécanique intégré qui détecte quel type de nucléotide se trouve à la pointe de l’ARN et ajuste l’activité de l’enzyme. Les structures montrent en outre qu’ExoN reconnaît différentes bases (A, U, C ou G) par des liaisons hydrogène flexibles, mais a le plus de difficulté à accueillir les bases de type guanine, ce qui est pertinent car le bemnifosbuvir mime la guanosine.
Ce que cela signifie pour les futurs comprimés contre la COVID‑19
Pour les non‑spécialistes, le message clé est que le SARS‑CoV‑2 possède un « correcteur orthographique » sophistiqué capable d’extraire certains médicaments de son génome après qu’ils ont accompli leur effet d’arrêter la réplication. Le bemnifosbuvir et le sofosbuvir affaiblissent bien la machine de copie du virus, mais en même temps ils orientent l’ARN vers le correcteur qui peut partiellement annuler leurs effets. En révélant précisément comment le correcteur viral saisit ces médicaments, et comment une petite boucle régulatrice bascule l’enzyme entre des états plus ou moins actifs, ce travail offre une feuille de route pour concevoir de nouveaux nucléotides antiviraux qui se lient mal à ExoN, qui le verrouillent dans une conformation inactive, ou qui exploitent sa difficulté à traiter des structures de type guanine. De telles molécules de nouvelle génération pourraient être bien plus difficiles à « effacer » par le virus, améliorant notre capacité à traiter la COVID‑19 et de futures épidémies de coronavirus.
Citation: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Mots-clés: SARS-CoV-2, résistance aux antiviraux, analogues nucléotidiques, relecture de l’ARN, réplication des coronavirus