Clear Sky Science · fr
L’acide de Lewis induisant le débordement d’hydroxyde permet l’électro-oxydation sélective de l’urée en nitrite avec production d’hydrogène économisant de l’énergie
Transformer les déchets en produits utiles et en carburant propre
L’urée est surtout connue comme composant de l’urine et des engrais, mais dans les eaux usées elle devient un polluant tenace. Cette étude montre comment l’urée peut être transformée d’un fardeau en ressource : grâce à un catalyseur conçu de façon intelligente, les auteurs convertissent l’urée en nitrite, un produit chimique de valeur pour les engrais et la pharmacie, tout en produisant simultanément de l’hydrogène avec une consommation électrique inférieure à celle du fractionnement conventionnel de l’eau. Ce travail donne un aperçu d’installations de traitement futures qui nettoient l’eau, fabriquent des produits utiles et génèrent de l’énergie propre en même temps.
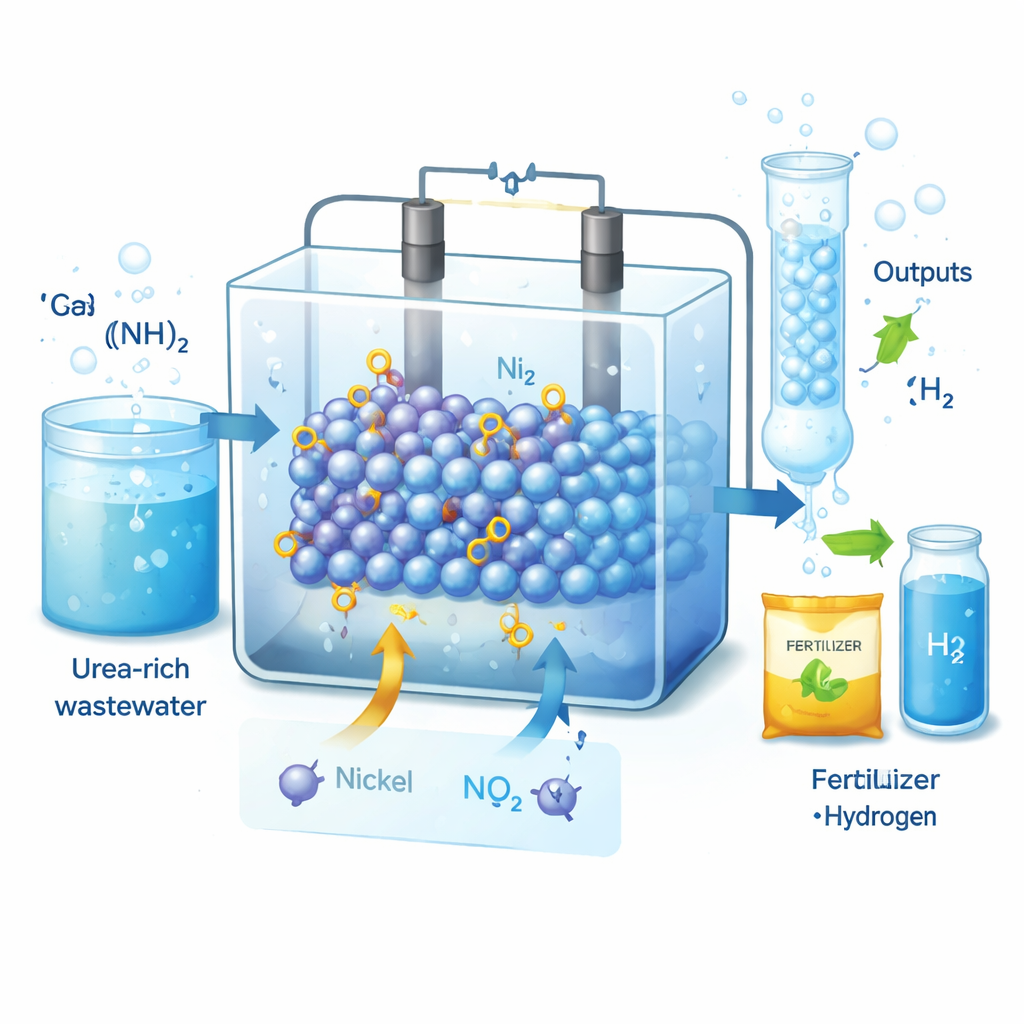
Pourquoi le nitrite et l’hydrogène sont importants
Le nitrite est un ingrédient clé en agriculture, conservation alimentaire et en pharmacie, et la demande mondiale se compte en millions de tonnes par an. Aujourd’hui, la plupart des nitrites sont produits par le procédé Ostwald, qui fonctionne à haute température, consomme beaucoup d’énergie et émet des oxydes d’azote polluants. Parallèlement, les eaux usées domestiques et industrielles contiennent une forte charge d’urée, représentant 70–80 % des polluants azotés. Si cette urée pouvait être électrochimiquement valorisée en nitrite tout en produisant du gaz hydrogène, on pourrait à la fois épurer l’eau et fournir deux produits de grande valeur — à condition que le procédé soit suffisamment efficace et sélectif.
Orienter les réactions dans la bonne direction
Lorsque l’urée est oxydée en solution alcaline, elle peut suivre deux voies principales. L’une conduit à l’azote moléculaire inerte et au dioxyde de carbone ; l’autre, plus souhaitable, mène au nitrite et au nitrate, des produits commercialisables. Le problème est que la plupart des catalyseurs à base de nickel, qui sont les plus utilisés pour cette réaction, sont peu sélectifs : ils produisent un mélange de produits et gaspillent de l’énergie en favorisant la réaction d’évolution de l’oxygène, qui génère de l’oxygène gazeux sans valeur commerciale. Les auteurs ont cherché à repenser la surface catalytique pour concentrer et diriger les ions hydroxyde, l’espèce réactive OH⁻ en milieu alcalin, de façon à favoriser la rupture des liaisons carbone–azote et la formation de nitrite plutôt que l’association des atomes d’azote en N₂.
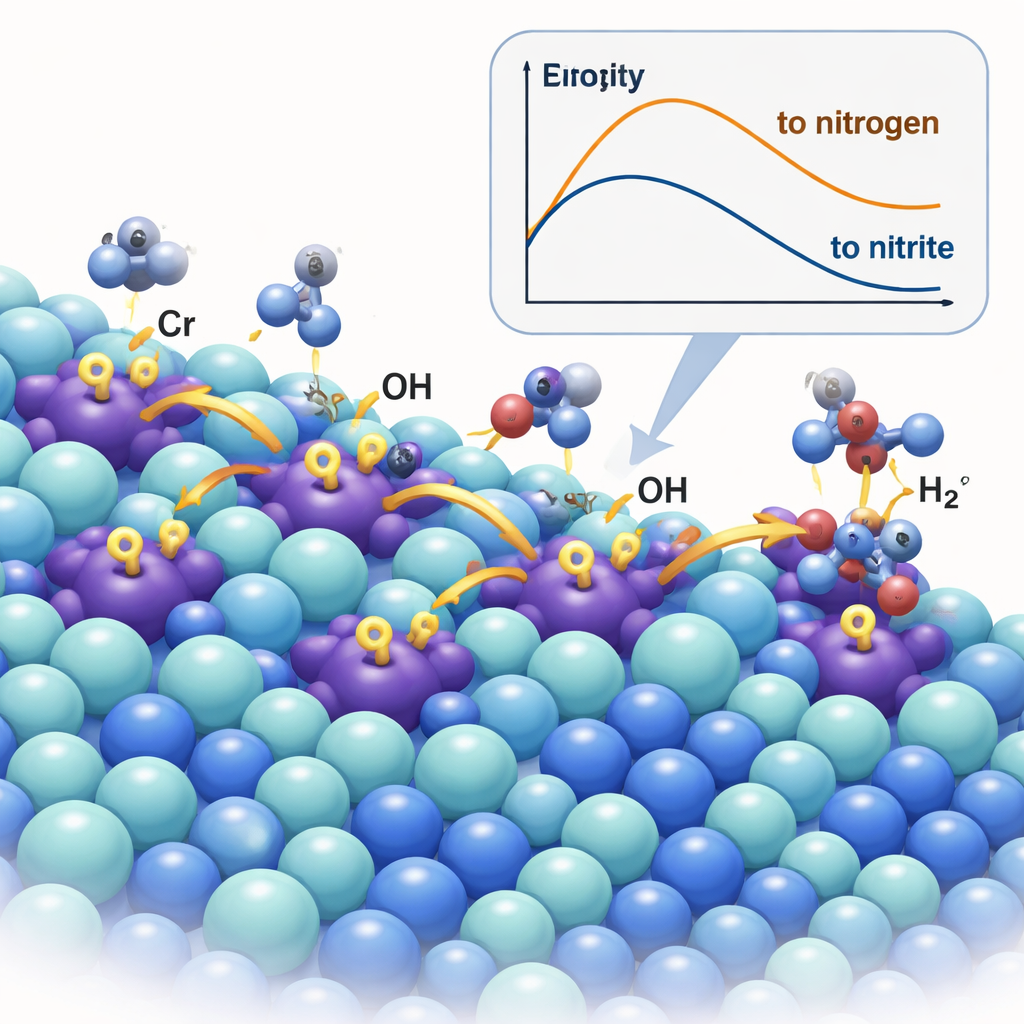
Un catalyseur qui pompe les espèces réactives
L’équipe a créé un nouveau matériau en dopant le sulfure de nickel (Ni₃S₂) avec une petite quantité de chrome, formant Cr–Ni₃S₂. Les ions chrome agissent comme des sites dits acides de Lewis — des centres appauvris en électrons qui attirent fortement les ions hydroxyde. À l’aide de microscopies avancées, de techniques au rayons X et de spectroscopies, les chercheurs ont confirmé que les atomes de Cr se positionnent dans le réseau du sulfure de nickel et le contractent/distordent légèrement, modifiant la répartition électronique. En conditions de réaction, les sites au chrome fonctionnent comme de petites pompes : ils capturent les OH⁻ puis les « déversent » sur des sites nickel voisins, où se déroule l’oxydation de l’urée. Des mesures in situ par Raman et infrarouge, ainsi que des expériences de marquage isotopique, ont suivi directement ce débordement d’hydroxyde du Cr vers le Ni et montré qu’il accélère la formation de sites actifs d’oxyhydroxyde de nickel (NiOOH) qui pilotent la chimie désirée.
Rendements élevés, moins d’énergie et bonne stabilité
Parce que l’OH⁻ est délivré efficacement aux bons endroits, le catalyseur Cr–Ni₃S₂ convertit l’urée en nitrite avec une sélectivité remarquable. À des densités de courant pertinentes industriellement, il atteint un rendement en nitrite d’environ 121 milligrammes par heure et par centimètre carré, avec des efficacités faradiques pour le nitrite supérieures à 80 %, tout en maintenant l’évolution de l’oxygène concurrente en dessous de 1,5 %. Le catalyseur reste stable pendant des centaines d’heures d’opération continue avec une lixiviation en chrome négligeable. Le même matériau réduit aussi fortement la tension requise lorsqu’il est associé à une cathode produisant de l’hydrogène dans un dispositif d’électrolyse assistée par l’urée, abaissant le coût électrique de la production d’hydrogène à environ 3,7 kilowattheures par mètre cube de H₂ — moins que l’électrolyse alcaline conventionnelle. Une analyse techno-économique suggère qu’à 400 milliampères par centimètre carré, le traitement d’une tonne d’urée dans ce système pourrait générer de l’ordre de 1 200 $ de valeur nette lorsque l’on compte à la fois le nitrite et l’hydrogène.
De la cellule de laboratoire aux dispositifs énergétiques pratiques
Pour démontrer un potentiel réel, les auteurs ont construit une cellule d’écoulement pour l’électrolyse continue assistée par l’urée et une batterie Zn–urée–air. Dans la batterie, le remplacement de la réaction d’évolution de l’oxygène habituelle pendant la charge par l’oxydation de l’urée a réduit la tension de charge de près de 0,3 volt tout en maintenant une performance stable pendant plus de 100 heures. Cela signifie que l’appareil peut à la fois épurer des flux contenant de l’urée et fournir un stockage électrique avec une efficacité énergétique supérieure. La même stratégie de conception basée sur des acides de Lewis a également fonctionné avec d’autres métaux comme l’étain et le titane, ou avec un hôte différent comme le sulfure de cuivre, ce qui suggère que l’approche est largement applicable.
Une idée simple derrière une réaction complexe
Pour les non-spécialistes, l’idée clé est que les chercheurs ont appris à guider où et comment un ingrédient réactif courant — l’hydroxyde — se fixe et se déplace à la surface d’un catalyseur. En ajoutant des sites au chrome qui agissent comme de forts attracteurs et relais pour OH⁻, ils facilitent la découpe des molécules d’urée en nitrite au lieu d’être complètement oxydées en gaz azote. Parallèlement, cette voie demande moins d’énergie électrique et produit naturellement du carburant hydrogène. Essentiellement, le travail montre que la conception atomique précise des « flux » sur un catalyseur peut transformer les eaux usées en source à la fois de produits chimiques et d’énergie propre.
Citation: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Mots-clés: oxydation de l’urée, production de nitrite, génération d’hydrogène, électrocatalyse, valorisation des eaux usées