Clear Sky Science · fr
Atlas multi-omique intégré révèle la hiérarchie des réseaux régulateurs spatio-temporels de la gastrulation chez la souris
Cet embryon qui bâtit son plan corporel
Tous les mammifères, y compris les humains, commencent la vie sous la forme d’une petite boule de cellules qui doit rapidement s’organiser en un corps complexe avec une tête, une queue, un dos, un ventre et des organes internes. Cette transformation spectaculaire a lieu pendant une fenêtre brève appelée gastrulation. L’article résumé ici construit une carte détaillée et multicouche de ce processus chez l’embryon de souris, montrant comment les gènes, les interrupteurs d’ADN et les signaux chimiques coopèrent dans l’espace et le temps pour guider les cellules vers leurs destinées futures.
Observer des milliers de cellules faire leurs choix
Pour suivre la gastrulation en action, les chercheurs ont analysé plus de 35 000 cellules individuelles d’embryons de souris sur cinq stades rapprochés, de la gastrulation précoce à tardive. Pour chaque cellule, ils ont mesuré non seulement quels gènes étaient activés, mais aussi quelles régions d’ADN étaient ouvertes et accessibles, signe qu’elles peuvent agir comme éléments régulateurs. À partir de ces données, ils ont identifié 31 types cellulaires distincts et retracé comment des cellules initialement flexibles se ramifient progressivement en trois feuillets germinaux principaux — ectoderme, mésoderme et endoderme — qui forment ensuite tous les tissus et organes. Ils ont aussi développé une nouvelle méthode computationnelle, BioCRE, pour relier plus précisément les gènes à leurs éléments d’ADN contrôleurs, révélant que de nombreux interrupteurs importants se trouvent loin des gènes qu’ils régulent.
Construire un atlas moléculaire 3D dans l’espace embryonnaire réel
La plupart des méthodes unicellulaires perdent la position d’origine de chaque cellule dans l’embryon, or la localisation est critique pour comprendre le patterning. L’équipe a contourné ce problème en alignant leurs données unicellulaires sur une carte tridimensionnelle existante de l’activité génique dans l’embryon de souris. Le résultat est ST-MAGIC, un « embryon numérique » où chaque petit emplacement est annoté avec les types cellulaires probables présents, les gènes qu’ils expriment et l’accessibilité de l’ADN environnant. Cet atlas montre, par exemple, comment différents sous-types mésodermiques — futurs cœur, muscle et tissus de soutien — émergent dans des régions distinctes et comment des gènes largement exprimés comme Otx2 utilisent différents éléments régulateurs à la surface externe de l’embryon (épiblaste) et à la surface interne (endoderme viscéral).
Quand la symétrie se brise et que la gauche devient différente de la droite
Une caractéristique marquante des plans corporels est que les côtés gauche et droit ne sont pas identiques — pensez au cœur légèrement décalé vers la gauche. Les auteurs ont utilisé leur atlas spatial pour zoomer sur le mésoderme latéral, où les différences gauche–droite apparaissent en premier. Ils ont trouvé des asymétries subtiles mais consistantes dans les types cellulaires enrichis de chaque côté et dans les régions d’ADN plus accessibles. À droite, des régions liées à une voie de signalisation de croissance nommée BMP étaient plus accessibles ; à gauche, des régions associées à des gènes nécessaires à la formation de segments et de structures cardiaques étaient favorisées. Certains de ces éléments d’ADN, y compris des éléments nouvellement découverts contrôlant le gène Lefty2, s’ouvrent avant l’apparition de différences visibles d’expression génique, suggérant qu’un « amorçage » précoce du paysage chromatine prépare chaque côté de l’embryon à interpréter différemment les signaux.
Une relève de facteurs guide la ligne médiane du corps
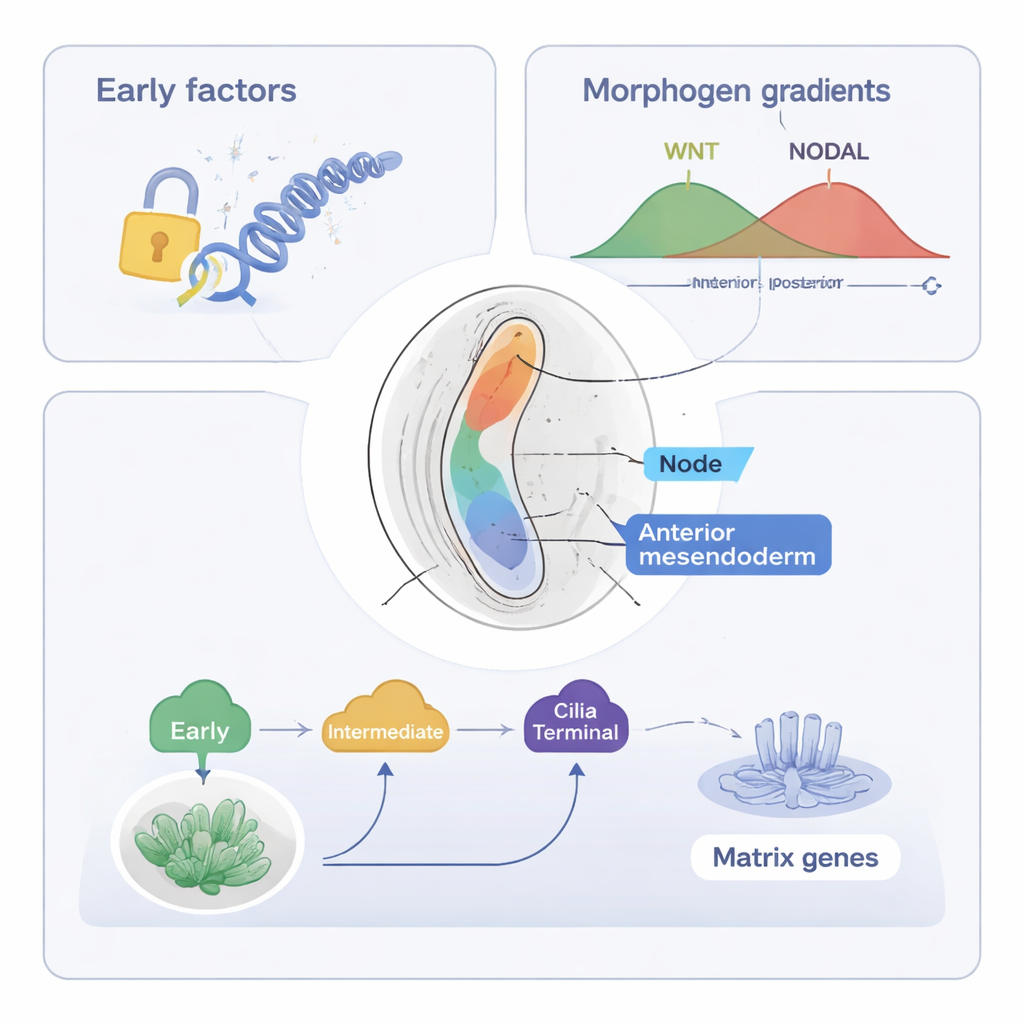
L’étude se concentre ensuite sur le mésendoderme axial, une population de cellules qui formera la notochorde — une structure en forme de tige le long de la ligne médiane qui aide à organiser la colonne vertébrale et le système nerveux. À l’aide de leurs outils combinés (ST-MAGIC et une version étendue appelée ST-MAGIC (+)), les auteurs ont suivi comment ces cellules naissent de la gouttière primitive antérieure et se divisent en deux branches : les cellules du nœud, qui construisent une structure ciliée importante pour la détection gauche–droite, et le mésendoderme antérieur, qui contribue aux tissus de la ligne médiane. Ils ont mis au jour une relève hiérarchique de facteurs de transcription — des protéines qui contrôlent l’activité génique. Des facteurs précoces, tels qu’EOMES, et des facteurs intermédiaires, dont FOXA2 et LHX1, ouvrent d’abord des régions clés d’ADN et établissent la réceptivité aux signaux majeurs comme WNT et NODAL. Plus tard, des facteurs « terminaux » tels que NOTO, SOX9 et un facteur nouvellement impliqué POU6F1 activent des programmes géniques spécialisés, par exemple ceux nécessaires aux cils ou à la matrice extracellulaire.
Signaux, chromatine et spécialistes d’action tardive
En intégrant des jeux de données publics sur les lieux de liaison des effecteurs des signaux WNT et NODAL à l’ADN, les auteurs ont montré que la réactivité de l’embryon à ces signaux change dans l’espace avant même que les sources de signaux elles‑mêmes ne se déplacent. Dans la région amorcée pour devenir mésendoderme axial, les sites d’ADN réactifs à NODAL et WNT s’ouvrent tôt, et beaucoup portent des motifs pour FOXA2, Zfp281 et d’autres régulateurs, suggérant un contrôle coopératif. La suppression expérimentale des facteurs d’action tardive NOTO et POU6F1 chez la souris perturbe l’expression des gènes spécifiques du nœud et liés aux cils et raccourcit les cils du nœud, alors que le paysage d’ADN ouvert sous-jacent reste en grande partie intact. Cela indique que des facteurs plus précoces établissent la base épigénétique, tandis que les facteurs tardifs affinent principalement l’expression génique sans remodeler la chromatine.
Pourquoi c’est important pour comprendre le développement
Pour un non‑spécialiste, ce travail peut être vu comme la construction d’un « schéma de câblage » très haute résolution de la manière dont un embryon dispose son plan corporel. Les auteurs montrent que les décisions de destin cellulaire pendant la gastrulation ne sont pas gouvernées uniquement par la présence de signaux, mais aussi par le moment et le lieu d’ouverture des interrupteurs d’ADN et par la séquence d’action des facteurs de transcription. Leurs atlas ST-MAGIC et ST-MAGIC (+) fournissent une ressource pour explorer ces relations dans l’espace et le temps, offrant un cadre qui pourrait éclairer les études sur les malformations congénitales, les modèles embryonnaires dérivés de cellules souches et, à terme, certains aspects du développement humain.
Citation: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Mots-clés: gastrulation, réseaux de régulation génique, multi-omique unicellulaire, patterning embryonnaire, développement de la souris