Clear Sky Science · fr
Autoinhibition inter-monomère de HEXIM1 gouverne la spécificité de liaison à l’ARN 7SK et l’inactivation de P-TEFb
Pourquoi ce petit ARN compte pour le contrôle des gènes
Chaque cellule doit décider quand activer ou désactiver des gènes, et elle le fait en contrôlant soigneusement une enzyme qui pilote la production d’ARN. Cet article révèle comment une petite protéine nommée HEXIM1, travaillant de concert avec un ARN non codant appelé 7SK, fonctionne comme un verrou de sécurité sur cette enzyme. Comprendre ce système moléculaire de sécurité aide à expliquer comment nos cellules empêchent une activité génique incontrôlée, et éclaire aussi la façon dont des virus comme le VIH détournent la même machinerie.
Un frein moléculaire à l’expression des gènes
Dans les cellules humaines, une étape clé de l’expression génétique est contrôlée par un facteur appelé P‑TEFb, qui aide l’ARN polymérase II à passer d’un état de pause à une transcription à pleine vitesse. Les protéines HEXIM, en particulier HEXIM1, jouent un rôle central pour contenir P‑TEFb. Elles le font au sein d’un large assemblage appelé RNP 7SK, construit autour de l’ARN 7SK. Lorsque HEXIM1 et 7SK s’associent, ils séquestrent P‑TEFb afin qu’il ne puisse pas stimuler la transcription. Jusqu’à présent, il manquait la pièce expliquant comment HEXIM1 évite de saisir P‑TEFb trop tôt, et comment l’ARN 7SK transforme HEXIM1 d’un inhibiteur inactif à un inhibiteur actif au bon moment.
Une protéine qui s’enlace elle-même et reste contrôlée
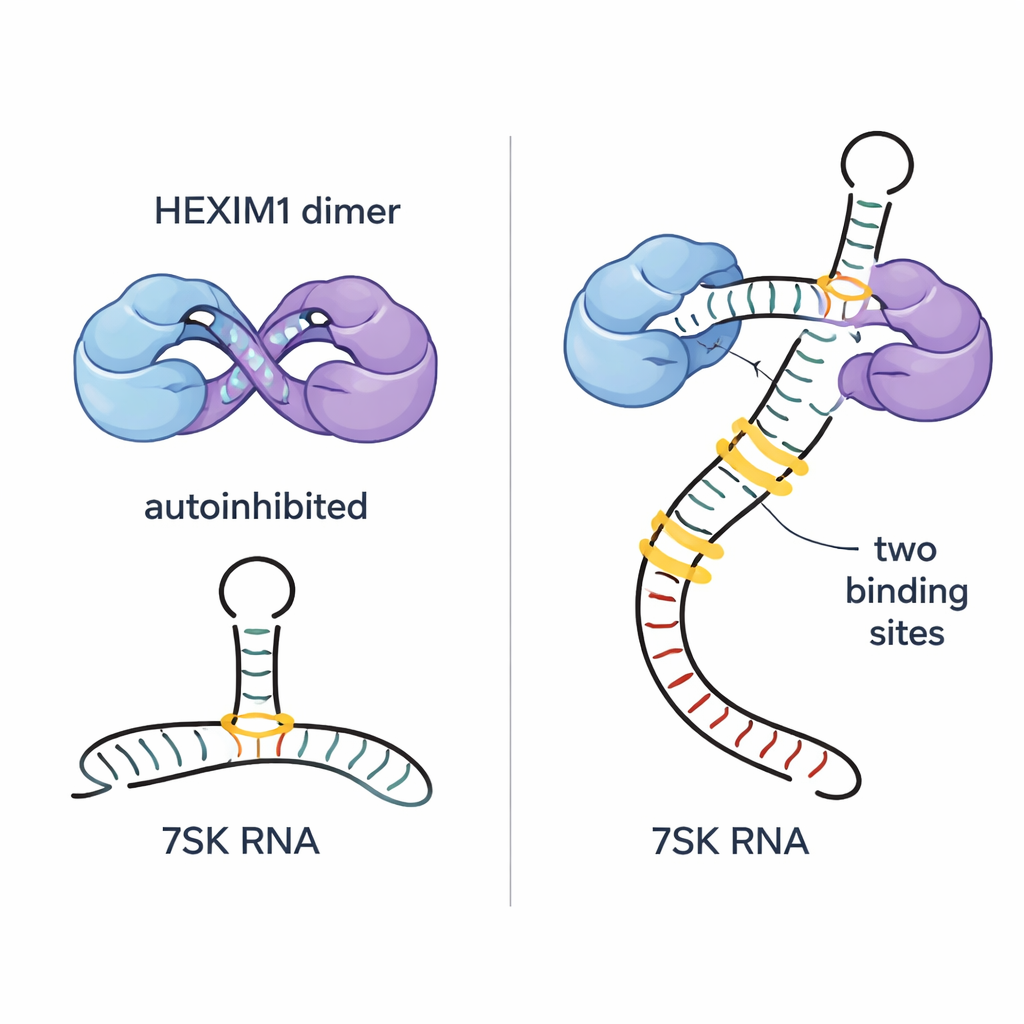
Les auteurs montrent que HEXIM1 forme naturellement un dimère — deux chaînes protéiques identiques appariées — et que les parties centrales flexibles de chaque chaîne s’enroulent l’une autour de l’autre dans une disposition d’« auto‑enlacement ». Dans cet état, un court segment crucial appelé motif PYNT, qui se lie normalement et inhibe la kinase P‑TEFb, est dissimulé à l’interface entre les deux chaînes. Grâce à des techniques NMR sensibles et des méthodes biophysiques, l’équipe a cartographié comment des régions basiques (chargées positivement) et acides (chargées négativement) des deux monomères interagissent pour créer ce dimère autoinhibé. Cette contrainte intégrée empêche HEXIM1 de se fixer de manière aléatoire sur P‑TEFb en l’absence d’ARN 7SK.
Comment l’ARN 7SK déverrouille HEXIM1
L’ARN 7SK contient plusieurs éléments structuraux, dont une longue région en tige-boucle appelée SL1. En découpant cet ARN en fragments plus petits et en suivant des changements subtils des signaux NMR, les chercheurs ont identifié cinq sites potentiels de liaison de HEXIM1 le long de SL1. Deux de ces sites se distinguent comme des points d’ancrage à haute affinité ; tous deux partagent une section hélicoïdale riche en A–U et une excroissance riche en U à proximité pouvant former des interactions particulières à trois bases. L’équipe a constaté que chaque moitié du dimère HEXIM1 se lie à l’un de ces deux sites forts sur l’ARN 7SK linéaire. Lorsque les deux sites sont occupés, la région centrale de HEXIM1 se réarrange, rompt les contacts d’auto‑enlacement et expose les motifs PYNT cachés, préparant ainsi la protéine à capturer P‑TEFb.
Choisir la bonne conformation de l’ARN — et éviter les mauvaises
L’ARN 7SK n’existe pas sous une seule forme ; il peut basculer entre une forme linéaire, qui présente les deux sites à haute affinité, et une forme quasi-circulaire n’offrant qu’un seul site adapté. Les auteurs montrent que l’autoinhibition de HEXIM1 le rend étonnamment sélectif : le dimère se lie faiblement à des sites isolés, mais bien plus fortement et de manière coopérative au segment SL1 linéaire complet qui présente les deux sites forts. Cette exigence de double site empêche HEXIM1 de rester accroché à des ARN aléatoires ailleurs dans la cellule et rend sa liaison très spécifique à la conformation linéaire de 7SK qui assemble le complexe répressif actif. Ils démontrent également que l’ajout de charges négatives proches de la région de liaison à l’ARN (mimant la phosphorylation d’une sérine clé) affaiblit la liaison à l’ARN sans perturber complètement l’autoinhibition, ce qui offre un moyen potentiel pour la cellule de libérer P‑TEFb lorsque nécessaire.
D’un interrupteur moléculaire à un impact cellulaire
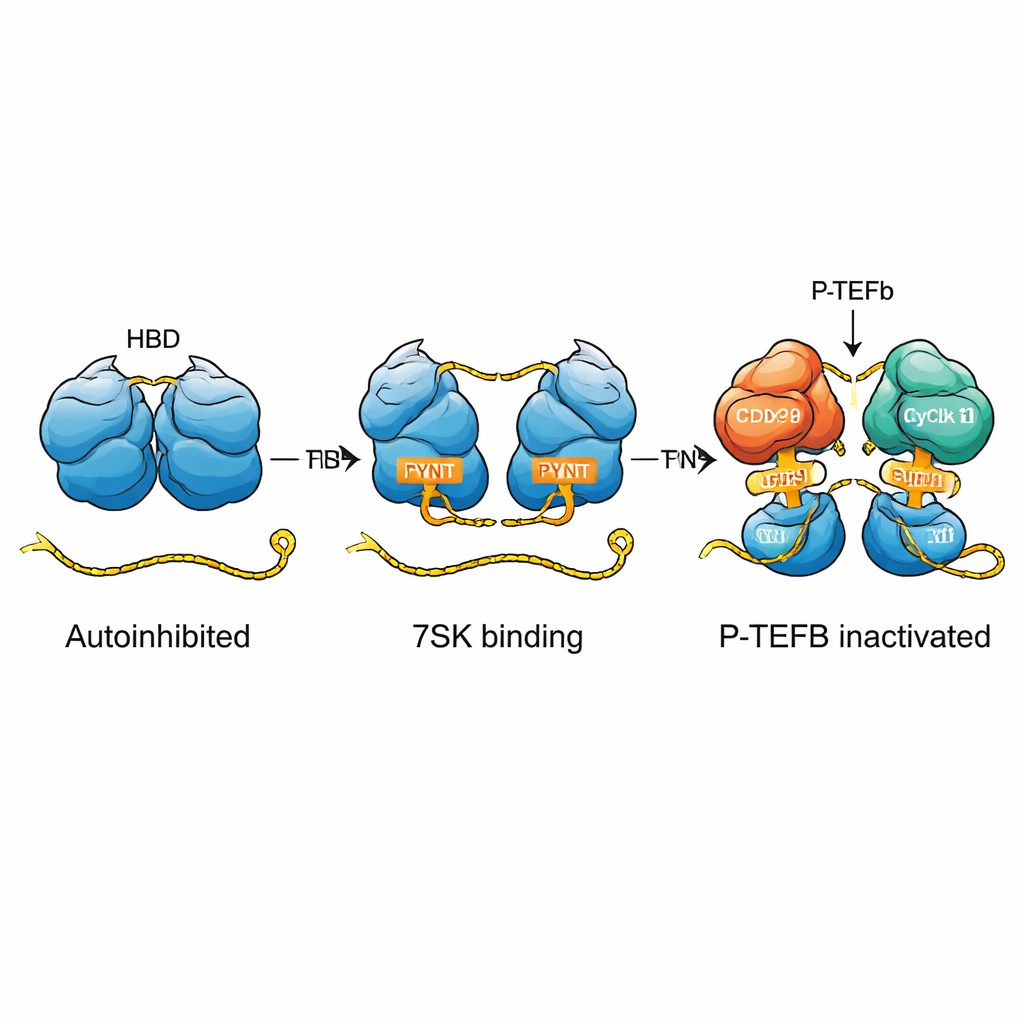
Globalement, l’étude révèle HEXIM1 comme un interrupteur moléculaire finement réglé. Dans son état de repos, d’auto‑enlacement, il garde ses segments PYNT bloquant P‑TEFb cachés. Ce n’est que lorsqu’il rencontre l’ARN 7SK linéaire avec deux sites de liaison correctement arrangés que la protéine bascule en état « activé », exposant ces segments pour capturer et inactiver P‑TEFb — souvent deux copies à la fois. Ce mécanisme explique comment les cellules utilisent un petit ARN et une protéine flexible pour imposer un contrôle précis de la transcription, et fournit un cadre plus clair pour comprendre comment des signaux cellulaires, des modifications chimiques ou des protéines virales comme le Tat du VIH peuvent faire pencher la balance entre expression génique en pause et active.
Citation: Yang, Y., Murrali, M.G., Galvan, S. et al. HEXIM1 inter-monomer autoinhibition governs 7SK RNA binding specificity and P-TEFb inactivation. Nat Commun 17, 1570 (2026). https://doi.org/10.1038/s41467-026-68285-8
Mots-clés: régulation de la transcription, ARN 7SK, HEXIM1, P-TEFb, HIV Tat